-
开放科学(资源服务)标识码(OSID):

-
鱼类生殖发育与配子发生是探究低等脊椎动物繁殖的关键,性腺发育相关基因在其中发挥着至关重要的作用[1-3]。性腺由生殖细胞及其周围的体细胞所组成,因此性别决定也由二者相互构成,而性别分化通常指生殖细胞及其周围体细胞的分化,相较于高等脊椎动物,鱼类性别决定和性腺分化过程具有很强的可塑性[4-5]。目前已经克隆获得很多与性腺分化和发育相关的基因,如nanos3、vasa、dazl、piwi、wt1、zar1、cyp19a1a,foxl2、rspo1、dmrt1、amh和sox9等[6-10]。近年来,dnajb1和dnd1基因也被发现可能参与了鱼类性别分化的调控过程[11-12]。
热休克蛋白(Heat Shock Proteins,HSPs)是多种蛋白折叠的伴侣分子,当温度发生变化时,与其他激素共同作用以防止机体损伤。Jolly等[13]按照分子量大小将热休克蛋白分为6类,其中就有Hsp40家族,该家族拥有3个亚型,分别为DNAJA、DNAJB和DNAJC[14]。DNAJB1作为Hsp40家族中的重要成员,具有高度保守的J结构,该结构与其他蛋白协同作用,共同维持细胞内稳态[15-18]。此外,研究发现HSPs在早期胚胎和生殖细胞发育过程中起重要作用,可能与动物机体生长发育过程中的细胞增殖、分化和凋亡有关[19-20]。Hsp40家族中的dnajb1基因广泛存在于体细胞和生殖细胞中[11, 21-22],然而,关于热休克蛋白基因dnajb1在鱼类性腺中的功能研究相对较少。
dnd1基因是一种脊椎动物特有的种质特异性标记的母源性RNA,其编码的RNA-binding蛋白对原始生殖细胞(Primordial Germ Cells,PGCs)的特化、增殖和迁移至关重要[23]。2003年,dnd1基因首次在斑马鱼(Danio rerio)中被分离鉴定,经深入研究发现,dnd1基因主要参与维持生殖细胞的发育及相关细胞的生理活动[24-26];随后,陆续在青鳉(Oryzias latipes)[27]、异育银鲫(Carassius gibelio)[28]、非洲爪蟾(Xenopus tropicalis)[29]、小鼠(Mus musculus)[30]、原鸡(Gallus gallus)[31]和智人(Homo sapiens)[32]中鉴定了dnd1基因[33]。在非洲爪蟾中,dnd1只在卵巢中表达[29];在小鼠中,dnd1仅在生殖细胞中表达[30],敲降dnd1基因的表达,可导致小鼠卵巢生殖细胞缺失和精巢生殖细胞癌变[34];在斑马鱼中则会导致PGCs的迁移发生紊乱[25]。研究表明,在大菱鲆(Scophthalmus maximus)[35]、稀有鮈鲫(Gobiocypris rarus)[36]以及西斯伯里青鱂(Oryzias celebensis)[37]等鱼类中,dnd1基因在生殖细胞中特异性表达,暗示其在各种鱼类的生殖细胞发育中的功能均具有较强的保守性。基于dnd1在生殖发育过程中的重要性,在鱼类中开展dnd1基因序列分析及表达分布检测,可为后续开展的生殖细胞发育和配子发生等研究提供思路。
尖吻鲈(Lates calcarifer),又名金目鲈、盲曹鱼,隶属于鲈形目、尖吻鲈科,原产于印度太平洋地区,具有较强的繁殖和耐受能力,在淡水与咸水中均能快速生长,是一种重要的水生经济鱼类[38]。尖吻鲈为雌雄同体雄性先熟鱼类,从幼鱼到初次性成熟雄鱼需3~4年,而发育为性成熟雌鱼则需6年。鉴于其特殊的性逆转特征,尖吻鲈被认为是研究鱼类性别分化机制和性控育种的理想模型。本研究以尖吻鲈为研究对象,克隆获得dnajb1和dnd1基因,分析其序列特征,检测其在组织中的表达分布以及在雌雄生殖细胞发育过程中的表达特征,为进一步开展鱼类生殖细胞发生发育及调控机制研究奠定基础。
全文HTML
-
尖吻鲈购自广东珠海某养殖场。采用30 mg/L丁香酚(Solarbio,中国)麻醉,分离肠、脑、心、肝、脾、肾、精巢和卵巢,用于RNA提取的组织在液氮中速冻后保存于-80 ℃冰箱中备用。另取一部分尖吻鲈性腺组织,4%多聚甲醛(Paraformaldehyde,PFA)固定后,转移至甲醇中于-20 ℃冰箱中保存,用于后续冰冻切片。
-
采用TRIzol Reagent(Solarbio)进行尖吻鲈组织总RNA提取,并分别用NanoDrop 2000微量分光光度计和1%琼脂糖凝胶电泳检测RNA的浓度、纯度和完整性。调整总RNA为1 000 ng/μL,使用PrimeScript RT reagent Kit with gDNA Eraser Kit(Takara)进行基因组DNA去除并反转录为cDNA,然后-20 ℃冰箱中保存备用。
-
根据美国国家生物技术信息中心数据库(National Center for Biotechnology Information,NCBI)中预测的尖吻鲈dnajb1(XM_018679787.2)和dnd1(XM_018694390.2)基因序列,设计引物扩增cDNA序列(表 1)。用TaKaRa PrimeSTARⓇ Max DNA Polymerase(Takara)进行PCR扩增。反应体系为:25 μL 2×Master Mix,上下游引物(10 μmol/L)各2 μL,cDNA 1 μg,补充dd H2O使总体积至50 μL。扩增程序为:94 ℃预变性3 min;94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸60 s,循环数为30;最后72 ℃延伸5 min。PCR产物经琼脂糖凝胶电泳检测,然后用TIANgel Midi Purification Kit(天根)进行胶回收,经DNA A-Tailing Kit(Takara)加A后连接pGEM-Teasy载体(Takara),转化大肠杆菌感受态Top 10后,进行菌液PCR扩增,挑选阳性克隆进行测序。本研究中的引物合成和DNA测序均由擎科生物(重庆)科技有限公司完成。
-
根据获得的尖吻鲈dnajb1和dnd1 cDNA序列设计特异性扩增引物Lcdnajb1-rt-F/R和Lcdnd1-rt-F/R(表 1),选用β-actin(XM_018667666.2)作为内参基因,设计引物β-actinF/R(表 1)。以尖吻鲈肠、脑、心、肝、脾、肾、精巢和卵巢组织cDNA为模板(稀释5倍后使用)进行RT-PCR扩增。反应体系为20 μL(10 μL 2×Taq Mix,引物各1 μL,模板1 μL,ddH2O添加至20 μL)。RT-PCR循环条件为:94 ℃预变性2 min;94 ℃变性30 s,60 ℃退火30 s,72 ℃延伸30 s,循环数为32;最后72 ℃延伸5 min。PCR产物进行琼脂糖凝胶电泳检测,并在生物成像系统(Bio-Rad)中进行观察。
按照TB GreenⓇ Premix Ex TaqTM试剂盒(Takara)说明书进行qRT-PCR实验,使用ABI QuantStudio 3 Real-Time PCR检测Lcdnajb1在尖吻鲈不同组织中的表达,每个样品重复数为3。反应体系为10 μL(5 μL 2×TB Green Premix Ex TaqⅡ(Takara),0.2 μL ROX Reference DyeⅡ(50×),上下游引物(10 μmol/L)各0.4 μL,cDNA(稀释成2 ng/μL)1 μL,ddH2O添加至10 μL)。反应条件为:95 ℃预变性2 min;95 ℃变性15 s,60 ℃退火1 min,40个循环。采用2-ΔΔCT法[39]进行不同组织中Lcdnajb1基因分析。qRT-PCR实验数据均采用x±s表示(n=3),并用Prism 9.5.0软件进行单因素方差分析(one-way ANOVA),采用Duncan's法进行多重比较检验组间差异并绘图,设p<0.05为差异有统计学意义。
-
通过NCBI网站上的ORF finder在线工具(ORFfinder Home-NCBI(nih.gov))进行开放阅读框(Open Read Frame,ORF)预测。利用在线工具Interpro(InterProScan-InterPro(ebi.ac.uk))查找基因家族序列和结构域。使用DNAMAN 8.0软件将核苷酸序列翻译成氨基酸序列,并对翻译得到的氨基酸序列进行多重比对分析。使用MEGA 11软件,按邻接法(NeighbourJoining,N-J)构建系统进化树,用自展法(Bootstrap)进行1 000次检验。
-
原位杂交技术具体操作步骤参考相关报道[40]。根据获得的Lcdnajb1序列,利用限制性内切酶Nco1(Solarbio)进行酶切反应;Lcdnd1序列用限制性内切酶SacII(Solarbio)进行酶切反应,进一步回收获得制备探针的线性化模板。分别利用SP6/T7 Enzyme Mix和Digoxigenin(DIG)RNA Labeling Kit合成正义和反义探针,并通过1%琼脂糖凝胶电泳进行检测。洗涤后以抗地高辛抗体标记的碱性磷酸酶和硝基蓝四氮唑/5-溴-4氯-3-吲哚基磷酸(NBT/BCIP)为显色底物进行显色,用碘化丙啶(Propidium Iodide,PI)对细胞核进行染色,经4% PFA固定后用中性树脂封片进行观察。所有图像均使用ZEISS Vert A1显微镜和ZEISS Axiocam 506 color成像系统进行观察和拍照。
1.1. 材料
1.2. 尖吻鲈组织总RNA的提取和cDNA合成
1.3. 全长cDNA克隆
1.4. 组织特异性表达分析
1.5. 生物信息学分析
1.6. 性腺组织切片原位杂交
-
通过基因克隆获得Lcdnajb1和Lcdnd1 cDNA序列,其中Lcdnajb1长度为1 287 bp,与NCBI数据库中预测的Lcdnajb1序列相似性为100%(GenBank登录号为XP_018535303.1),开放阅读框为1 047 bp,编码348个氨基酸,包含1个DNAJ保守结构域和1个DNAJ-C保守结构域(图 1a)。Lcdnd1长度为1 185 bp,与NCBI数据库中预测的尖吻鲈dnd1序列相似性为98.53%(XM_018694390.2),开放阅读框为1 128 bp,编码375个氨基酸,包含1个典型的RRM识别基序结构域(图 1b)。
用DNAMAN 8.0软件对尖吻鲈Dnajb1和Dnd1蛋白与其他物种同源蛋白序列进行多重比对,结果发现,尖吻鲈Dnajb1与大口黑鲈同源性最高,为94.1%;与大菱鲆、尼罗罗非鱼和青鳉的同源性在90.0%~92.8%;与斑马鱼的同源性为76.6%;与两栖动物非洲爪蟾、爬行动物绿海龟和蜥蜴的同源性在70.4%~71.0%;与哺乳动物(智人、小鼠、穴兔)的同源性在69.5%~71.0%;与鸟类原鸡的同源性最低,为66.4%(图 2)。尖吻鲈与其他物种的Dnajb1氨基酸序列具有高度的保守性,即都具有DNAJ结构域和DNAJ-C保守结构域。尖吻鲈Dnd1与鳜的同源性最高,为85.5%;与射水鱼和剑鱼的同源性都是71.0%;与青鱂、虹鳟、异育银鲫、斑马鱼和泥鳅的同源性在48.1%~66.8%;与智人和小鼠的同源性分别为39.3%和36.6%;与非洲爪蟾、中华鳖和绿海龟的同源性在34.0%~38.5%(图 3)。尖吻鲈与其他物种的Dnd1氨基酸具有高度的同源性,即1个RRM识别基序结构域和5个保守结构域(NR、CR1、CR2、CR3、CR4)。
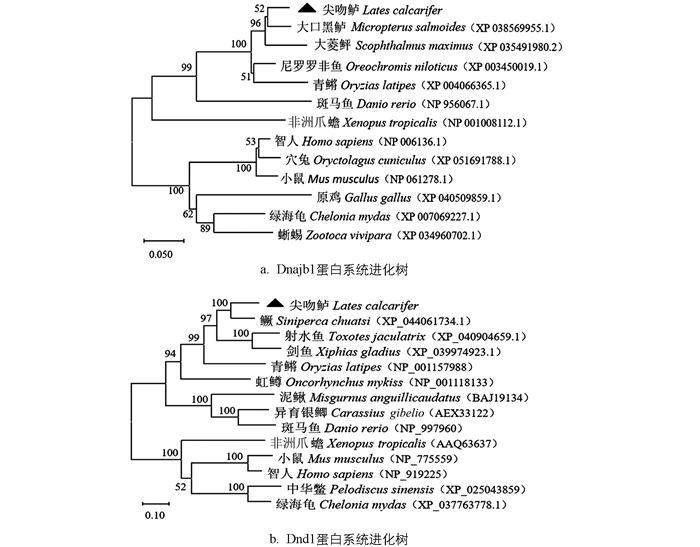
基于尖吻鲈和其他物种Dnajb1和Dnd1的氨基酸序列,通过Mega 11.0采用邻接法构建系统发育进化树,结果显示,尖吻鲈Dnajb1属于Hsp40家族,主要分为低等脊椎动物和高等脊椎动物两大支。Dnajb1与硬骨鱼类聚为一支,与鱼类同源性较高,与鸟类、爬行类和哺乳类同源性较低(图 4a);Dnd1主要聚为四足动物和硬骨鱼类两大分支,尖吻鲈Dnd1属于硬骨鱼类,与鱼类的同源性较高,与哺乳类的同源性较低,与龟、鳖类的同源性最低(图 4b)。
-
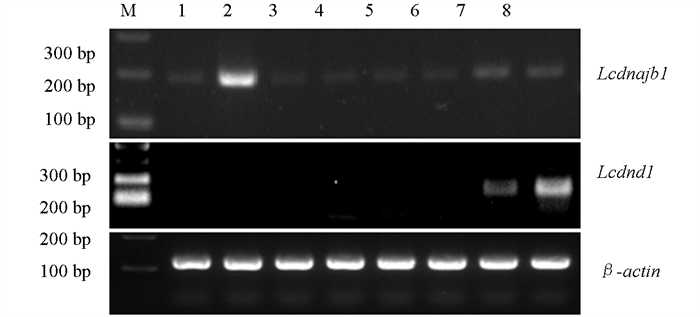
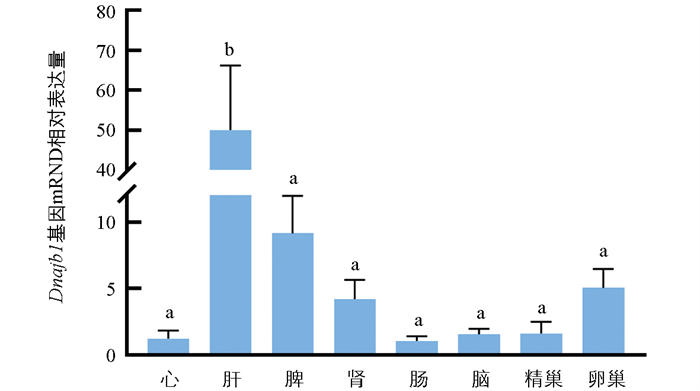
采用RT-PCR检测尖吻鲈Lcdnajb1和Lcdnd1基因在不同组织中的表达,结果显示,Lcdnajb1在心、肝、脾、肾、肠、脑、精巢、卵巢中均有表达,肝中表达量最高,精巢和卵巢中的表达量次之,其他组织中的表达量相对较低;Lcdnd1仅在性腺组织中表达,且卵巢中的表达量高于精巢,其他组织中检测不到(图 5)。进一步采用qRT-PCR检测Lcdnajb1基因的组织表达,结果显示,肝脏中的表达最高(图 6),显著高于其他组织,检测结果同RT-PCR中的结果类似。
-
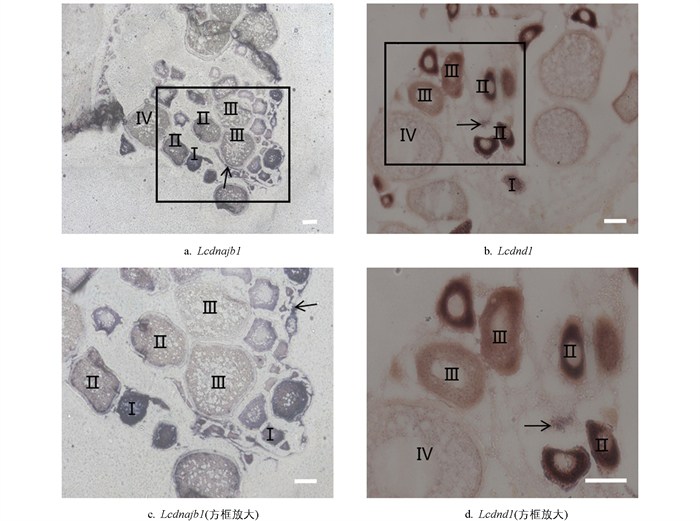
采用化学原位杂交检测Lcdnajb1和Lcdnd1在尖吻鲈卵巢中的表达定位,结果显示,dnajb1基因主要在雌性生殖细胞的第Ⅱ、Ⅲ期表达,而在Ⅳ期表达量开始减弱。有趣的是,成熟尖吻鲈的dnd1基因表达呈现出与Lcdnajb1基因类似的特征,即集中在雌性生殖细胞的第Ⅱ、Ⅲ期表达,Ⅳ期表达减弱。不同的是,Lcdnajb1在体细胞和生殖细胞中均有表达,而Lcdnd1仅在生殖细胞中表达,体细胞中几乎不表达(图 7)。
-
采用化学原位杂交检测Lcdnajb1和Lcdnd1在尖吻鲈精巢中的表达定位,结果显示,Lcdnajb1在雄性生殖细胞和体细胞中均有表达,而Lcdnd1仅在生殖细胞中表达,其他细胞中检测不到。Lcdnajb1在精原细胞和精母细胞中表达强烈,精子细胞中表达减少。Lcdnd1在生殖细胞中也出现相应的表达特征,但在精子中几乎检测不到(图 8)。
2.1. Lcdnajb1和Lcdnd1 cDNA克隆及序列分析
2.2. Lcdnajb1和Lcdnd1 mRNA的组织表达
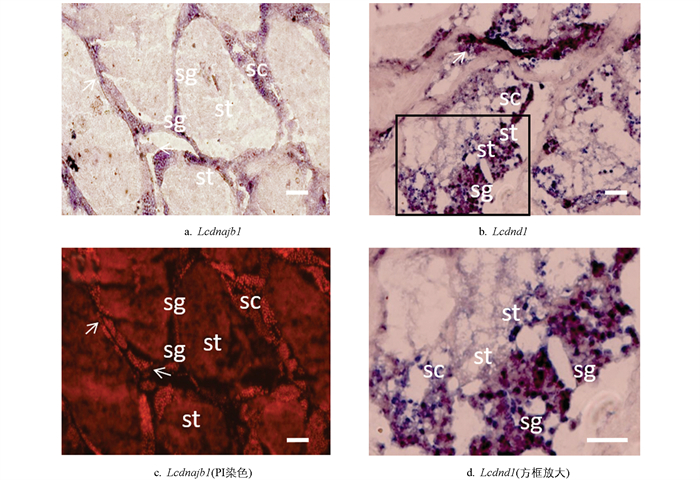
2.3. Lcdnajb1和Lcdnd1 mRNA在卵巢中的表达定位
2.4. Lcdnajb1和Lcdnd1在精巢中的表达定位
-
早在1962年,在果蝇(Drosophila)中就开展了有关热休克蛋白Hsp家族的研究[41]。随着研究的深入,有关其基因家族结构与功能的研究越来越多[42-43]。目前研究大多侧重于大分子热休克蛋白Hsp90和Hsp70等,而对小分子热休克蛋白研究较少[44]。本研究采用基因克隆技术获得尖吻鲈小分子热休克蛋白基因dnajb1,其氨基酸包含DNAJ和DNAJ-C两个保守结构域,与Hsp家族基因的多肽序列具有高度保守性[45-46]。本实验同时也克隆获得了dnd1基因,典型的RRM与大多数硬骨鱼类Dnd1蛋白一样[23, 47],Dnd1隶属于hnRNP-R-Q蛋白家族,包含1个RRM识别基序结构域和5个保守结构域,表明dnd1基因虽然在进化过程中存在着一定的变化,但仍然具有相对的保守性,推测其保守域可能是dnd1基因行使功能的重要结构域[48]。在本研究中,LcDnajb1和LcDnd1蛋白序列都表现出高度的保守性,但不同物种间仍然存在一定的差异。
-
Lcdnajb1的RT-PCR和qRT-PCR结果显示,Lcdnajb1在各组织中均有表达,其中在性腺中呈现差异性表达,即卵巢高于精巢,意味着Lcdnajb1在卵巢中发挥更为重要的作用,可能在雌雄同体雄性先熟鱼类尖吻鲈性逆转过程中发挥着一定的功能。有研究表明,HSPs在胚胎发育过程中具有一定的发育阶段依赖性和组织特异性[19],而Dnajbl与一些细胞过程相关,如蛋白酶体途径[49]、内质网(ER)应激[49]、病毒感染[50]等。在鱼类中,有关小分子热休克蛋白Dnajb1的研究相对较少,大多数集中在Hsp70大分子热休克蛋白上[51]。Hsp70在牙鲆(Paralichthys olivaceus)[52]肠中的表达量最高,而在唐鱼(Tanichthys albonubes)[53]的肝脏中表达量最高。在淞江鲈(Trachidermus fasciatus Heckel)[54]、鲤(Cyprinus carpio)[55]和泥鳅(Oriental weatherfish)[56]组织中均有HSP的表达,与本研究相似;在罗非鱼[11]中,dnajb1基因在精巢中的表达量高于卵巢。在本研究中,Lcdnajb1 mRNA在心、肝、脾、肾、肠、脑、卵巢和精巢中广泛表达,且在性腺中呈现差异性表达,而Lcdnd1只在卵巢和精巢中特异性表达,且卵巢的表达高于精巢,这与异育银鲫(Carassius gibelio)[29]、星斑川鲽(Paralichthy sdentatus)[23]、西斯伯里青鱂[38]、稀有鮈鲫[37]、中华鲟(Acipenser sinensis)[45]和牙鲆(Paralichthys olivaceus)[23]等的表达模式相似;dnd1基因只在小鼠[30]精巢中表达,卵巢中未见表达;而dnd1在非洲爪蟾[29]中的表达与小鼠恰恰相反,即只在卵巢中表达,在精巢中不表达。由此推测dnd1基因可能参与动物性腺发育,但不同物种间其调控性腺发育的作用机制可能存在差异。本研究中,Lcdnajb1和Lcdnd1在尖吻鲈性腺中的表达均表现为在卵巢中的表达水平高于精巢,这种表达模式是否与尖吻鲈性逆转发生有关,有待进一步验证。
化学原位杂交结果显示Lcdnajb1在体细胞和生殖细胞中均有表达,而Lcdnd1于生殖细胞中特异表达。在卵巢中,Lcdnajb1 mRNA在Ⅱ期卵母细胞中的表达最强,随着卵母细胞的生长发育分化,其表达量逐渐减弱。曾有研究报道在斑马鱼[57-58]卵母细胞中检测出了hsp基因的表达,且在海龟[59]、美洲鳄[60]等物种的卵巢组织中均有表达,但具体在哪个卵母细胞时期表达尚不明确。高温刺激尼罗罗非鱼[11]后,卵巢中dnajb1的表达量下降,热刺激恢复后回到正常水平。Lcdnajb1可能参与了卵细胞的发育,且当应激源出现时,可发生较显著的表达变化。Lcdnd1表达情况与Lcdnajb1的相似,主要集中在Ⅱ、Ⅲ期卵母细胞中,随着卵母细胞的发育分化而不断降低。在异育银鲫[28]、中华鲟[47]和稀有鮈鲫[36]卵巢中,dnd1的细胞表达分布情况也与此基本一致。值得一提的是,在西斯伯里青鱂[37]中,dnd1在卵巢发育的整个过程中都存在,并且随着卵子发生的进行,dnd1的表达逐渐减少。在中华鳖卵巢中,dnd1主要集中在Ⅱ期初级卵母细胞的细胞质中,随着卵细胞的发育,信号逐渐减弱,并在Ⅳ期之后的卵母细胞中检测不到[12]。在热带爪蟾成体组织中,dnd1的转录本是在卵巢中特异性表达,在精巢中几乎检测不到[29]。卵巢发育过程中,卵母细胞发育为第Ⅲ期时,细胞质中开始存积大量卵黄[61],所以Lcdnajb1和Lcdnd1基因有可能主要参与卵黄沉积前期,特别是初级卵母细胞向次级卵母细胞的发育过程,并在其中发挥一定作用。
在尖吻鲈精巢中,Lcdnajb1在雄性生殖细胞和体细胞中均有表达,其中在精原细胞和精母细胞中表达水平较高,而精细胞中表达量较低。相较于哺乳动物,水产动物Hsp家族成员的研究相对滞后,主要集中在腔肠动物和软体动物[62]。有研究发现,Hsp27、Hsp86在精子发生和胚胎发育过程中表达量显著升高[63-64]。雄海龟中Hsp72表达显著高于雌海龟[59]。在小鼠中,dnajb1基因[65]主要表达于精母细胞和圆形精细胞,这与本研究结果相似。尖吻鲈dnd1的表达结果显示,其在精巢中的表达集中在精原细胞与精母细胞中,精细胞中表达微弱,精子中未检测到信号。在西斯伯里青鱂[37]精巢中,精原细胞中的表达最为强烈,精母细胞中明显减少,而精子中不表达。在异育银鲫[28]、青鱂[27]、稀有鮈鲫[36]、中华鲟[47]中也呈现出一致的表达。有研究表明,dnd1基因在非洲爪蟾精巢中未见表达[29],而小鼠中dnd1分两种类型,dnd1-α集中在早期胚胎和胚胎性腺中,dnd1-β则在减数分裂起始及减数分裂后的精巢生殖细胞中表达[30],这些发现暗示dnd1在精子生成过程中起到了关键作用。Lcdnajb1和Lcdnd1在尖吻鲈精巢中的表达分析,推测dnd1基因主要在精子发生前期和中期作用,而dnajb1基因则在鱼类精子发生的整个时期都有一定作用,不仅在生殖细胞中表达,周围体细胞中也有表达,表明其在性腺发育过程中发挥着重要作用。
综上所述,本研究通过基因克隆获得了尖吻鲈dnajb1和dnd1的cDNA序列,进一步分析发现,Dnajb1蛋白具有DNAJ和DNAJ-C两个保守结构域;Dnd1蛋白具有1个典型的RRM识别基序结构域和5个保守结构域(NR、CR1、CR2、CR3、CR4)。RT-PCR检测结果显示,dnajb1基因在尖吻鲈各组织中广泛表达,而dnd1特异性地在精巢和卵巢组织中表达。进一步采用化学原位杂交方法检测Lcdnajb1和Lcdnd1在性腺组织细胞中的表达定位,发现dnajb1 mRNA在生殖细胞和周围体细胞中均有表达,而dnd1 mRNA仅在生殖细胞中表达。研究结果表明,dnajb1和dnd1基因可能共同参与了尖吻鲈两性配子发生发育过程,为后续开展雌雄同体鱼类的生殖细胞发育、配子发生和性逆转等研究提供了理论依据。




 下载:
下载: