-
酪蛋白(Casein,简称CS)是一种全价蛋白质,是乳制品中主要的蛋白质成分,具有较高的营养价值和良好的功能特性[1].在乳制品中,酪蛋白通常以酪蛋白-磷酸钙络合物形式的胶束状态存在,通过胶粒之间的静电排斥以及空间位阻的共同作用保持着一种不稳定的平衡,但易受酸、受热、盐类、凝乳酶等加工环境和其他因素的影响.特别是在pH值低于酪蛋白的等电点的酸性乳饮料中,体系中酪蛋白因倾向于聚集而失稳,使得蛋白质沉淀.这一现象已成为制约酸性乳饮料生产和开发的关键问题之一.因此,在酸性乳饮料的生产过程中,常需要加入稳定剂用以提高体系的稳定性.通过多糖与酪蛋白的相互作用可提高体系的稳定性,常用的多糖有果胶、CMC、黄原胶、可溶性大豆多糖、变性淀粉、海藻酸丙二醇酯等多糖高分子[2].
随着人们生活水平及健康意识的不断提高,高纤维、低脂肪、低热量的食品越来越受到人们的青睐.魔芋葡甘聚糖(Konjac glucomannan,简称KGM)作为一种食物纤维,具有高纤维、低脂肪和低热量的特点,同时具有非常强的亲水性、凝胶性、流变学特性以及增稠性等[3-4],常常被作为稳定剂或增稠剂应用于茶饮料、冰淇淋、果冻等食品工业中[5].此外,KGM还具有较多的生物活性,如降低血脂,减肥,抗癌等作用[6-7].因此,KGM的添加既可以提高食品体系的稳定性、改善和控制食品的流变特性和质构特征,还可以提高产品的功能性,为食品加工的多样性提供条件.然而,目前对KGM等中性非离子多糖在乳制品中的应用研究仍然较少.
此外,研究表明食品的稳定性不仅取决于蛋白质和多糖性质,也取决于蛋白质和多糖之间相互作用的本质和作用强度[8].因此,本文对CS与非离子多糖KGM的相行为进行研究,通过建立相图,采用流变仪、紫外可见光谱分析仪来探讨CS-KGM混合体系的相分离机理,利用相分离,优化和控制食品加工条件,达到解决在加工贮藏过程中由于相分离所造成的食品体系不稳定的问题,并为生产中利用蛋白-多糖复合物作为稳定乳状液的重要组分,制备具有一定货架期稳定性的乳状液提供一定的理论基础.
全文HTML
-
酪蛋白(纯度92%),郑州建达化工产品有限公司;魔芋葡甘聚糖(纯度92%,重均分子量为100~200 kDa),云南省昭通市三艾有机魔芋发展有限公司;无水磷酸氢二钠,磷酸二氢钾,氢氧化钠,浓盐酸,均为分析纯,国药集团化学试剂有限公司.
-
MCR301流变仪,奥地利安东帕有限公司;PL402-C电子天平,梅特勒-托利多仪器有限公司;BS224S分析天平,赛多利斯(北京)有限公司;S-2C pH酸度计,上海伟业器械厂;JB200-S数显电动搅拌机,上海标本模型厂;UV-2550紫外可见光谱分析仪,上海精密科学仪器有限公司;SC-3612低速离心机,科大创新股份有限公司中佳分公司.
-
准确称取一定质量的CS和KGM样品,分别溶于0.05mol/L的磷酸盐缓冲液中,于室温下搅拌3 h以上,确保样品溶液充分水化以得到CS和KGM浓度分别为4%和1%的贮备液.将水化好的CS和KGM以一定比例混合,制备出CS质量分数为1%,KGM质量分数为0~0.5%的CS-KGM混合液,室温下搅拌1.5 h,确保CS和KGM充分混匀,4 ℃存放备用.用1 mol/L HCl或NaOH调节体系的pH值.
-
将配制好的含有1%的CS和不同质量分数的KGM(0~0.5%)按不同比例混合制备CS-KGM混合溶液,用1 mol/L HCl或NaOH调节混合体系的pH值,得到一系列CS-KGM混合溶液(pH值为3~7),于室温下静置一段时间,考察KGM的浓度(CKGM)、pH值的变化和静置时间对混合体系的影响.
-
采用MCR301流变仪测定样品的粘度和应力随剪切速率的变化情况.选用平板完成测试,平板直径选用50 mm,间距设定为1 mm.剪切速率测定范围为1~300 s-1,测定温度为25 ℃.
测定不同条件下混合体系的储能(弹性)模量G′、损耗(粘性)模量G″对角频率(ω)的依赖性,扫描频率10-1~103rad/s.
-
将制得样品以4 200 r/min离心90min.用0.05 mol/L磷酸盐缓冲液将得到的上清液稀释30倍后进行近紫外图谱扫描.
-
用Excel 2007和Origin 8.5数据处理软件对结果进行画图分析.
1.1. 材料
1.1.1. 实验材料
1.1.2. 仪器与设备
1.2. 方法
1.2.1. CS-KGM混合溶液的配制
1.2.2. 相图的绘制
1.2.3. CS-KGM混合溶液流变性测定
1.2.4. CS-KGM混合溶液的紫外光谱分析
1.3. 数据处理
-
相分离行为现象普遍存在于食品的加工和生产中,控制生物大分子间的相分离行为对产品微结构设计及工艺具有重要的意义.为了研究CS-KGM混合体系的相变化行为,本文考察室温下静置不同时间、KGM的浓度和pH值的变化对混合体系相行为的影响,并对相变化结果进行拍照.如图 1,这些体系或者为沉淀相,或为发生离散型相分离形成乳白色浑浊的下层相和相对透明的上层相,或形成澄清、均匀的胶体体系,或为乳白色的均一相.
如图 1(1)显示,当混合体系的pH值高于5时,形成的是均一的CS-KGM混合体系,无肉眼可见的相分离现象产生.在pH值为5的条件下,当CKGM≤0.1%时形成的是乳白色均一相,当CKGM≥0.2%时CS-KGM混合体系发生了明显的离散型相分离,形成了乳白色的下层相和半透明的上层相.
当pH值低于5的时候,在CKGM≤0.1%时,体系产生沉淀,CKGM为0.2%时发生明显的相分离,说明过低的CKGM不能提高体系在酸性条件下的稳定性.当CKGM≥0.3%时,形成的是乳白色的均一相.在pH降低过程中,混合体系的絮凝程度随着CKGM的增加而逐渐降低.这也说明在酸性条件下一定浓度的KGM可以增强体系的稳定性.
此外,从图 1还可以观察到,在pH≤5的条件下,随着时间的延长,当CKGM<0.4%时,相分离现象越来越明显,上层透明相的高度逐渐升高;在静置60 h后,CKGM为0.4%才有明显的相分离现象,且pH值为5的混合体系均产生沉淀.另外还观察到,当CKGM为0.5%时,相分离现象并没有随着时间的增加而越来越明显,说明添加一定量的KGM也能在时间上一定程度地提高体系的稳定性.
为了进一步证明,CS和KGM混合体系的相分离是由于排空相互作用所致的,在实验过程中震荡已发生相分离的试管,并且发现富含蛋白质的下层相相对较容易被稀释分散,这说明了相分离过程是可逆的,而后上下层相又混合均匀并重新形成单相体系,这与排空相互作用的机理是一致的[9].
-
流变性是反应物质在力的作用下所呈现出的流动与变形的特性.在流体食品的生产加工过程中,把握其流变性,在控制食品的质量、口感及工艺设计等方面都具有重要的意义[10].
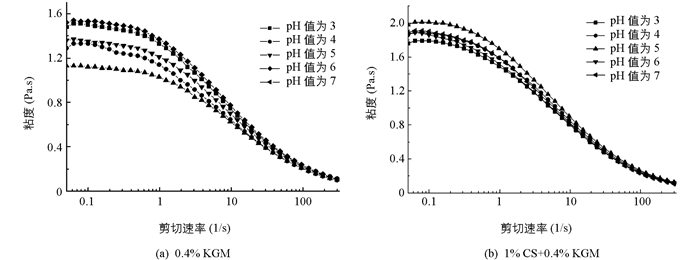
KGM溶于水会形成粘稠溶胶,其具备非牛顿流体的特征,属于假塑性流体,即有剪切变稀的性质[11]. 图 2表示了不同pH条件下,KGM溶液和CS-KGM混合溶液的粘度随剪切速率的变化情况.由图可见,CS-KGM混合体系在流变学上也属于非牛顿流体,其粘度随着剪切速率的增加而降低,并且当剪切速率达到一定程度后,粘度趋于稳定.这是由于随着剪切速率的增加,聚合物的分子间的线团结构被破坏,使得分子定向性更强,导致分子间作用力减小[12].
从图 2还可以看出,CS-KGM混合溶液的粘度高于单纯的KGM溶液. KGM是非凝胶性中性多糖,自身不带电荷,溶液粘性增加的主要原因是KGM的空间占位效应(occupy effect)增加了体系中的CS有效凝胶的形成浓度.随着pH值的降低,KGM的粘度变化不大,显示了KGM在低浓度下具有较好的耐酸性,符合龚加顺等[13]的研究结论.同时可以观察到pH值的降低也未对CS-KGM混合溶液产生显著影响,说明混合溶液在酸性条件下的粘度稳定性得到提高,低浓度的KGM具有作为稳定剂的作用.
同时在实验过程中还观察到,当CS溶液中加入KGM后,CS-KGM混合体系的粘弹性质显著大于单纯的CS体系,这是因为KGM的增加对凝胶网络形成有协同增加效应,从而使得凝胶强度显著增加.
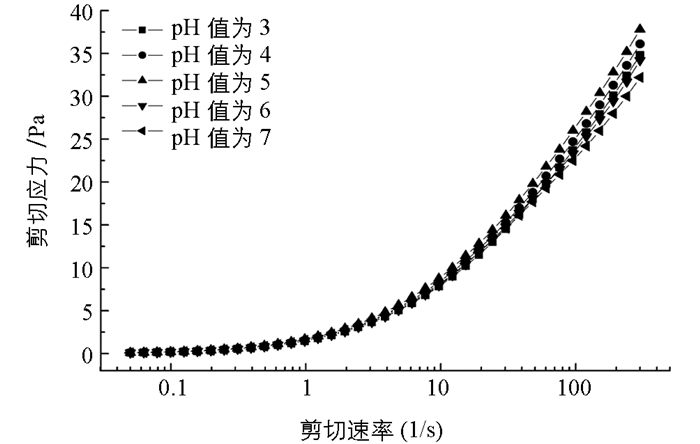
图 3表示了不同pH条件下,CS-KGM混合溶液的剪切应力随剪切速率的变化情况.由图可见,在整个剪切速率范围内,剪切应力随着剪切速率的增大而增大,呈现出非线性关系,属于非牛顿型流体,符合剪切变稀流体,直观地反映了假塑性流体的触变性.可用Herschel-Bukley[14]模型拟合,其方程为
式中,τ为剪切应力,Pa;τ0为屈服应力,Pa;η为粘度,mPa·s;γ为剪切速率,r/min,n为速率指数. n为假塑性流体的量度,n值越小,剪切越易变稀,假塑性程度越大,拟合结果见表 1.
由表 1可以看出,随着pH值的降低,混合体系的τ0值、η值、n值相对稳定无显著变化,对pH值的变化表现出无依赖性,表明pH值对混合溶液的假塑性基本无影响.
-
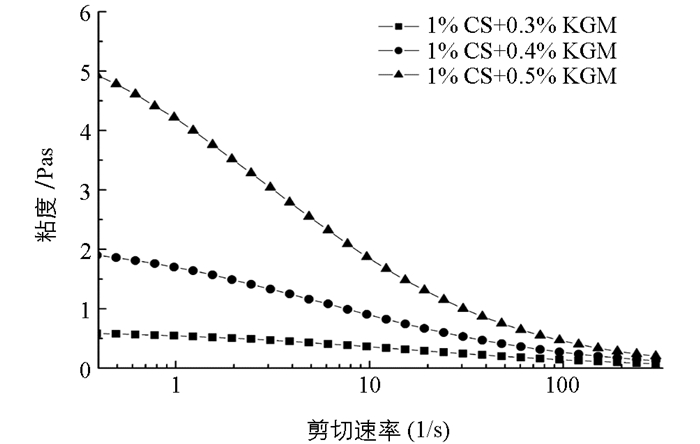
图 4表示在不同KGM浓度条件下,CS-KGM混合溶液的粘度随剪切速率的变化情况.由图可见,随着KGM浓度的增加,混合溶液的粘度也显著提高,这是因为KGM具有很强的增稠性和凝胶特性,因而混合溶液的粘度会随着浓度的升高而升高[15].在低浓度条件下,高分子主要是以无规则线团状态孤立地存在于溶液介质中,随着浓度的不断增大,高分子数目也相应不断地增加,相互接触,继而发生相互覆盖和穿越交叠,使溶液成为各处链段大致均匀的缠结网,因而导致溶液粘度不断增大[16].
-
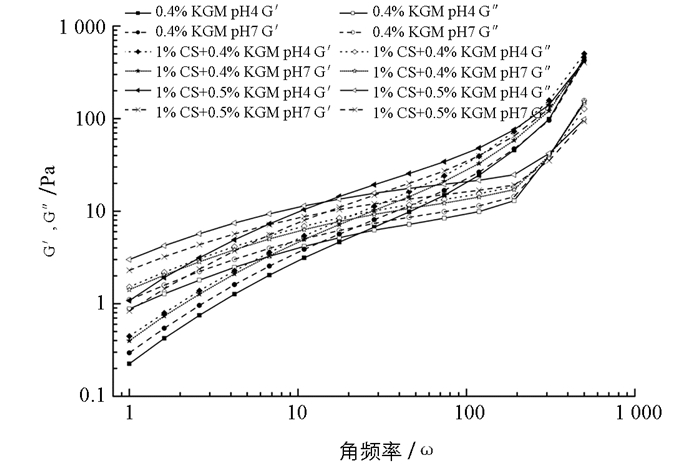
物质所具有的粘弹性,可以用储能模量(G′)和耗能模量(G″)对角频率ω的依赖性来表征.如图 5,在低频区,G″大于G′,说明在较长时间的外力作用下,分子链段的取向是一致的,它易于流动,其网络结构或片段遭到了破坏;而在高频区,在短时间的外力作用下,分子链段还来不及完全取向,其熵弹性产生了回复,从而导致体系呈现弹性,G′始终明显大于G″[17].在整个过程中体系表现出明显的频率依赖性,成溶胶的性质.
-
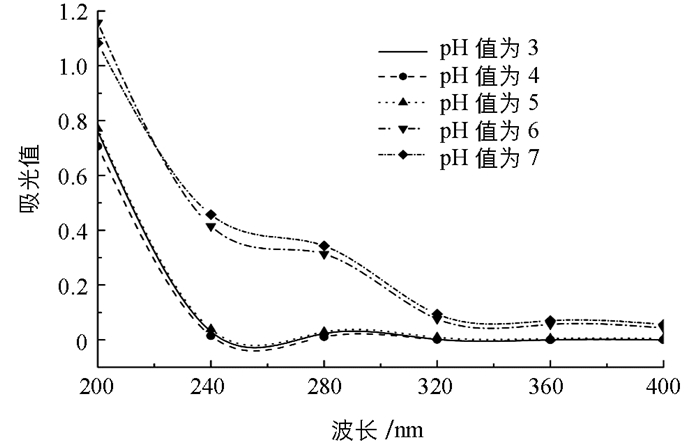
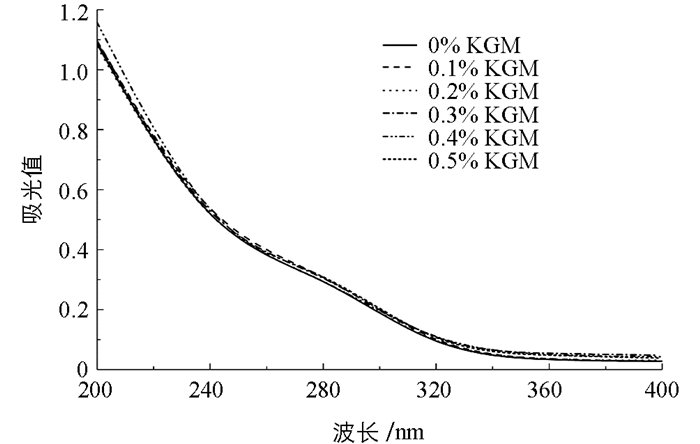
如图 6为不同pH值条件下CS-KGM混合溶液的紫外光谱.从图中可以看出,在pH值为3~5间,样品的上清液中所含的蛋白质在280nm处的吸收强度基本相似,且明显低于pH值为6以上的样品.这可能是由于pH值为6以下体系发生了相分离,蛋白质主要分布在下相,而pH值为6和pH值为7时,形成的是均一稳定的混合溶液,蛋白质分布均匀. 图 7表示在pH值为6的条件下,不同KGM浓度的混合溶液上清液中蛋白质的紫外图谱,发现不同KGM浓度没有对蛋白的吸收造成明显的影响,说明KGM的添加不会影响CS的吸收.
2.1. CS-KGM混合体系相行为分析
2.2. CS-KGM混合体系流变学性质分析
2.2.1. pH值对CS-KGM混合溶液的粘度随剪切速率变化的影响
2.2.2. KGM浓度对CS-KGM混合溶液的粘度随剪切速率的影响
2.2.3. pH值和KGM浓度对CS-KGM混合溶液的粘弹性的影响
2.3. CS-KGM混合体系紫外图谱分析
-
乳制品已经成为日常生活中不可或缺的一种食品,CS作为乳制品中主要的蛋白质成分,以CS-磷酸钙络合物形式的胶束状态存在于乳制品中,具有较高的营养价值和良好的功能特性,然而CS胶束状态易受多种因素(酸碱、盐类、温度等)的影响而不稳定,特别是在酸性乳饮料中易聚集产生沉淀,严重影响酸性乳饮料产业的发展.目前,大部分研究通过添加羧甲基纤维素(CMC)至乳制品体系中,借助于CMC分子链的阴离子基团与酪蛋白上氨基的分子间相互作用来起到稳定剂的作用.虽然CMC能达到很好稳定乳制品的作用,但是产品的口感和风味释放不好[18-19].因此,寻找一种天然安全且效果好的乳制品稳定剂,一直是食品科学领域研究的焦点. KGM作为一种天然的膳食纤维,具有非常强的亲水性、凝胶性、增稠性等功能性质,借助KGM与蛋白质的相互作用,可作为一种很好的乳制品稳定剂.然而目前有关酸性条件KGM与酪蛋白的研究还未见报道,本研究的结果对于KGM在酸性乳制品上的推广与运用有着重要意义.
本文在酸性条件下考察KGM对CS体系的稳定性,通过相分离分析发现当KGM-CS体系(pH值为5)中KGM浓度低于0.1%,KGM-CS能够形成一个均匀的体系,而当KGM浓度高于0.2% CS-KGM混合体系发生了明显的离散型相分离,且这种相分离行为还与静置时间相关.这可能是由于CS胶束表面会形成空位层,由于体系中KGM的浓度较低,存在于空位层中的KGM浓度显著低于存在于溶剂相中的KGM浓度,因而CS-KGM混合体系能够稳定存在.但随着体系中KGM浓度的增加,KGM分子被迫接近CS胶束的表面,致使空位层变薄,CS-KGM混合体系失稳,因而发生明显的离散型相分离现象[9-11].而随着静置时间的延长,蛋白质组分之间相互作用力随之加强,导致富含CS的下层发生聚集,形成较大的颗粒,不利于体系的稳定.对中性条件下,KGM-鲜奶奶冻复配体系、KGM-卵白蛋白复配体系的研究也得到相类似的结果[20-21].对CS-KGM混合溶液的相行为研究还发现低酸性(pH值低于5)条件下CS-KGM混合体系的稳定性随着KGM的浓度增大还有所增加,这可能是低酸性条件下随着KGM浓度的逐渐升高,体系中CS和KGM之间的静电荷随之增加,二者之间的静电排斥作用也变强,使得体系中不稳定的蛋白质进行再次分散,进而防止CS的凝聚作用的发生,从而防止体系产生沉淀[22].
对CS-KGM混合体系的流变学性质分析发现,CS-KGM混合溶液属于假塑性流体,对角频率依赖性强,是一种很好的溶胶体系,且体系中KGM浓度与pH值的变化未能影响混合溶液粘度与粘弹性.这可能与KGM本身的性质有关[23].课题组前期研究发现KGM由于自身特殊的结构,使得其在不同酸性pH下的稳定好[24].紫外光谱分析还发现CS-KGM混合溶液中蛋白质的紫外吸收随着pH值的变化的变化明显,但随KGM浓度的变化不明显,KGM不影响蛋白质的紫外吸收.这进一步验证了CS-KGM间主要靠的是物理相互作用力,不会影响CS原来的结构,同时借助KGM自身结构的特殊性,起到一定程度的稳定CS-KGM混合体系的作用.
-
CS-KGM混合体系的相行为受体系溶液pH值、KGM添加量及静置时间的影响.在酸性条件下,增加KGM的添加量有利于CS-KGM混合体系的的稳定性.通过流变学分析发现CS-KGM混合体系属于假塑性流体,呈溶胶的性质;紫外光谱分析显示CS的紫外吸收随着pH值变化而变化明显,且KGM对CS的紫外吸收无影响.




 下载:
下载: