-
开放科学(资源服务)标识码(OSID):

-
水热液化是一种以水作为溶剂和反应介质在150~400 ℃以及0.5~25 MPa之间将生物质转换成高附加值小分子化合物的化学转化方法,具有成本低、溶剂绿色环保、反应温度低、转化效率高等优点[1]。然而,生物质水热液化反应的机理复杂,反应过程受多种因素影响,这对于优化反应条件、提高液化油品质和产率提出了挑战。
目前,已有学者[2]研究了不同类型的生物质原料以硫酸(H2SO4)作为催化剂的水热液化反应制备5-羟甲基糠醛(5-HMF)过程中的碳稳定同位素分馏特征,以及不同原料的碳稳定同位素比值差异对5-HMF产率的影响。研究结果表明,不同原料在液化过程中生成5-HMF的反应速率存在差异,C3植物生成5-HMF的最大产率所需时间比C4植物少。此外,8种原料生成的5-HMF的13C同位素在反应时间0~60 min内发生了显著的富集,富集程度为淀粉>纤维素>木质纤维原料。结构简单的淀粉和纤维素生成5-HMF的反应速率较快,而木质纤维原料的液化反应速率较慢。不同碳稳定同位素比值的原料通过水热液化生成5-HMF的反应速率存在差异,碳稳定同位素比值越大,则反应过程的碳稳定同位素富集因子越大,即富集程度越大。上述研究通过比较不同碳稳定同位素比值原料在水热液化制备5-HMF过程中的差异,研究了原料类型对产率和碳稳定同位素分馏的影响,但研究中仅使用了H2SO4作为催化剂。然而催化剂在水热液化反应中具有重要的作用,不同类型的催化剂可能会影响碳稳定同位素分馏特征、产物产率和反应速率,因此有必要系统研究不同类型催化剂对反应的影响。
本研究旨在探讨以C3植物源原料(杨木、木薯淀粉)和C4植物源原料(玉米秸秆、玉米淀粉)为对象,通过水热液化反应生成5-HMF到末端产物乙酰丙酸乙酯(EL)的过程中碳稳定同位素分馏机制。研究中选择H2SO4和氯化铝(AlCl3)作为催化剂,分析不同类型催化剂对产物产率和碳稳定同位素分馏机制的影响。
全文HTML
-
旋转蒸发仪(RE-6000A,上海亚荣生化仪器厂);反应釜(50 mL,上海岩征实验仪器有限公司);稳定同位素比值质谱仪(DELTA V Advantage,赛默飞世尔科技公司);气相色谱仪(TRACE GC Ultra,赛默飞世尔科技公司);XS204天平;气相色谱三重四级杆质谱联用仪(GC-QQQ-MS,TQ8040,岛津公司);气相色谱四级杆飞行时间质谱联用仪(GC-Q-TOF MS,7890-7200B,安捷伦公司)。
碳稳定同位素标准物质:C3乙醇,碳稳定同位素比值为(-27.53±0.3)‰;C4乙醇,碳稳定同位素比值为(-10.98±0.3)‰。杨木粉(C3植物源)与玉米秸秆粉(C4植物源),过178 μm筛,在105 ℃干燥6 h;玉米淀粉(C4植物源淀粉)与木薯淀粉(C3植物源淀粉);无水乙醇(分析纯,上海昆山金城试剂有限公司);丙酮(色谱纯,山东禹王实业有限公司);98%的H2SO4(分析纯,南京化学试剂有限公司);无水AlCl3(99%,上海麦克林生化科技公司);5-HMF(97%,标准品H810986,上海麦克林生化科技公司)。
-
将2 g木质纤维生物质原料放入反应釜中,按固液比1∶15(g∶mL)加入蒸馏水和无水乙醇混合溶剂(体积比为1∶1),加入原料质量50%的3 mol/L催化剂。实验反应时间从加热至170 ℃后开始记录,反应完毕后冷却到室温,过滤,将滤液在50 ℃下旋蒸除水。
-
用GC-Q-TOF MS对液化后液相产物中的5-HMF准确定性并确定出峰时间,每个样品连续进样3次。同时在GC-QQQ-MS上利用外标法对5-HMF进行定量分析,称取5-HMF标准品1 g,加无水乙醇溶解配制成浓度为10 g/L的溶液。5-HMF标准品相对分子量为126.11,溶剂为乙醇,保留时间为11.36 min,主要碎片离子m/z为69、97、126[3]。取对照品溶液,加乙醇稀释成一系列浓度为0.2 g/L、0.4 g/L、0.6 g/L、0.8 g/L的对照品,根据目标物的保留时间和特征离子,采用Q3SCAN模式对特征离子进行扫描,以确定离子的峰面积(Y)对浓度(X)进行线性回归,求得线性回归方程[4]。GC-QQQ-MS的色谱条件[5]为:采用Rtx-5M5色谱柱(长×直径×填料粒径:30 m×0.25 mm×0.25 μm),进样量为1 μL,分流比为10∶1,载气为高纯氦气,流速为1.4 mL/min,进样口温度为300 ℃。柱箱温度在50 ℃保持3 min,以10 ℃/min升至260 ℃,保持10 min。GC-Q-TOF MS的色谱条件[6]为:采用HP-5MS色谱柱(长×直径×填料粒径:30 m×0.25 mm×0.25 μm),进样量为0.2 μL,分流比为100∶1,载气为高纯氦气,载气流速为175.42 mL/min,进样口温度为300 ℃。柱箱温度在50 ℃保持3 min,从10 ℃/min升至280 ℃,保持15 min。
-
配制C3乙醇、C4乙醇标准溶液:分别称取8 mg的2种乙醇标准品,用丙酮溶解并定容至10 mL容量瓶中,在0~4 ℃保存备用。乙醇标准样品至少分析5个平行样品,保证标准偏差为±0.3 ‰。
配制液化样品待测溶液:称取12 mg标准样品,用乙醇定容在10 mL容量瓶中,在0~4 ℃保存备用。采用HP-5MS色谱柱(长×直径×填料粒径:60 m×0.25 mm×0.25 μm),载气为高纯氦气,流速为1.5 mL/min。进样口温度为250 ℃,氧化炉温度设定为1 000 ℃,不分流进样,进样量为0.5 μL。气相升温程序为:在50 ℃保持2 min,以5 ℃/min升至260 ℃,保持10 min。每8~10个样品间隔测定1次乙醇标准样品,以检查仪器的准确性。所有液化样品至少分析3个平行样品,保证标准偏差为±0.3 ‰。
-
同位素富集因子ε用来表征反应过程中稳定同位素的分馏程度。在稳定同位素分馏研究中,利用式(1)瑞利方程以及式(2)某元素A的动力学同位素效应来计算ε,不确定度为95%置信区间的统计误差。
其中:δt为液化反应时间在t min时的5-HMF碳稳定同位素比值;δ0为液化反应时间在0 min时的5-HMF碳稳定同位素比值;f为反应时间在t min时5-HMF的浓度Ct与初始反应浓度C0的比值;n为某元素A总反应的点位数;x为某元素A参与反应的点位数。
1.1. 实验仪器与材料
1.2. 样品制备
1.3. 液化产物5-HMF的定性及定量分析
1.4. 产物中碳稳定同位素比值的测定
1.5. 同位素富集因子ε计算
-
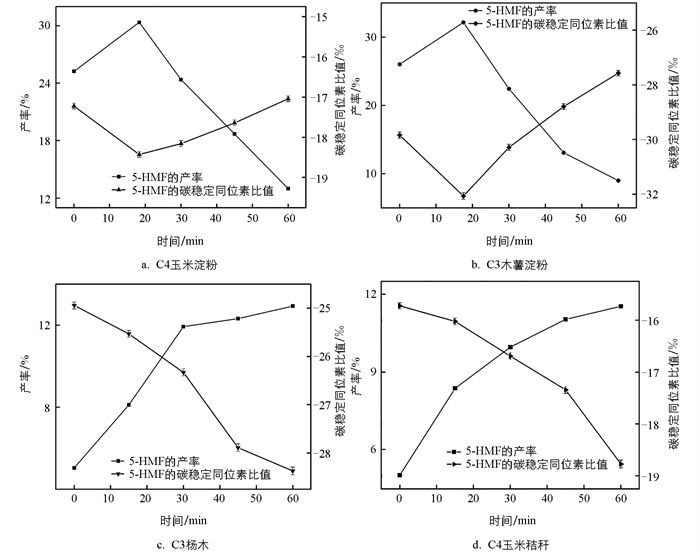
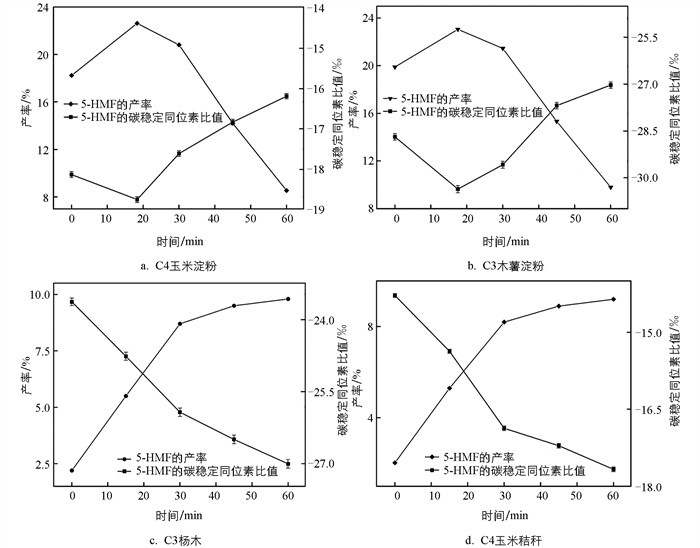
通过对不同催化剂反应所得的产率曲线(图 1、图 2)进行分析,可知在H2SO4和AlCl3 2种催化体系下产物产率及碳稳定同位素比值表现出显著的差异。
如图 1所示,在AlCl3催化条件下,C3木薯淀粉在18 min时的5-HMF产率达到最高值23.36%,碳稳定同位素比值从(-28.694±0.031)‰降低至(-30.370±0.007)‰,表明碳轻同位素12C富集。随后5-HMF开始降解,碳重同位素富集至(-27.030±0.033)‰。该分馏特征体现了5-HMF生成和降解的反应进程:在反应初期,碳轻同位素12C优先参与反应生成5-HMF,具体表现为在反应初期中间产物5-HMF中的12C呈现明显富集趋势,碳稳定同位素比值持续降低;在反应中期,中间产物5-HMF降解速率开始大于生成速率,产率与碳稳定同位素分馏特征曲线表现为产率持续下降,与之对应的碳稳定同位素分馏特征为中间产物5-HMF中12C开始分馏并逐渐贫化,而13C则呈现明显富集趋势,碳稳定同位素比值持续升高;反应后期在45 min到达,此时反应达到平衡状态,产物中碳稳定同位素比值变化趋于稳定,在分馏特征曲线中表现为碳稳定同位素分馏速率降低,斜率变化逐渐平缓,碳稳定同位素比值变化较小。该分馏特征体现了反应到达后期,末端产物EL的生成和积累过程。C3杨木随反应时间的增加5-HMF产率持续上升,在60 min时达到9.80%,碳轻同位素持续富集,在60 min时达到(-27.031±0.035)‰。对于结构复杂的木质纤维生物质原料,5-HMF的生成是一个相对缓慢的过程,反应主要处于反应物在酸性环境中水解为小分子糖类化合物并逐步脱水生成5-HMF的阶段,碳轻同位素12C不断参与反应生成5-HMF,因此碳稳定同位素比值表现为持续降低。C4玉米淀粉在18 min时5-HMF产率达到最高值23.46%,之后逐渐下降至8.55%,碳稳定同位素比值从(-18.151±0.022)‰降低至(-18.771±0.017)‰,随后逐渐增加至(-16.210±0.009)‰。C4玉米秸秆随反应时间的增加5-HMF产率持续上升,在60 min时达到9.20%,碳轻同位素持续富集,在60 min时达到(-17.670±0.006)‰。2种C4原料的碳稳定同位素分馏特征趋势基本与C3原料一致,不同之处在于C3、C4原料的碳稳定同位素的比值不同,因此在后续反应生成的产物中也表现出了碳稳定同位素比值的差异,对比图 1中曲线的不同能够得知反应物碳稳定同位素比值的差异对产物产率、碳稳定同位素分馏以及曲线斜率有一定影响。
如图 2所示,在H2SO4催化条件下,C3木薯淀粉在18 min时的5-HMF产率达到最高值33.11%,碳稳定同位素比值从(-29.837±0.013)‰降低至(-32.065±0.013)‰。随后5-HMF开始降解,碳重同位素富集至(-27.566±0.013)‰。C3杨木生成的5-HMF产率从5.04%逐渐增加,在60 min时达到最高值12.93%,碳稳定同位素比值从(-24.940±0.033)‰降低至(-28.370±0.029)‰。C4玉米淀粉在18 min时的5-HMF产率达到最高值30.07%,之后逐渐下降至13.01%,碳稳定同位素比值从(-17.223±0.023)‰降低至(-18.427±0.003)‰,随后逐渐增加至(-17.042±0.013)‰。C4玉米秸秆的5-HMF产率从2.03%逐渐增加,在60 min时达到最高值11.04%,碳稳定同位素比值从(-15.727±0.012)‰降低至(-18.771±0.017)‰。对比图 1、图 2,在碳稳定同位素分馏趋势及产率变化趋势大致相同的情况下,2种淀粉原料在H2SO4催化体系下的5-HMF最高产率均高于AlCl3催化体系。C3杨木和C4玉米秸秆在H2SO4催化体系下的产率增长趋势也明显高于AlCl3催化体系。在2种催化体系下,碳稳定同位素比值的变化趋势均表明了碳轻同位素在5-HMF生成过程中先于碳重同位素出现分馏现象,H2SO4催化体系下的碳稳定同位素比值变化幅度更大,表明H2SO4催化下的碳稳定同位素分馏现象更为显著。
实验结果表明:淀粉类原料的5-HMF产率普遍高于木质纤维原料,且反应速率更快;H2SO4作为催化剂对淀粉类和木质纤维原料生成5-HMF的催化效率更高,产率更大;H2SO4催化下碳稳定同位素分馏现象更显著,表明催化剂类型影响碳稳定同位素的分馏特征,体现了反应进程。H2SO4是一种强的布朗斯特酸(Brønsted acid)[7],在水热条件下能够电离出大量的氢离子(H+)。H+可以与木质纤维中的糖苷键发生水解反应,促进纤维素降解生成葡萄糖、木糖等单糖。H+还能催化单糖脱水生成5-HMF、糠醛等小分子化合物。而AlCl3是一种路易斯酸(Lewis acid)[8],在水热条件下通过与反应物形成配位化合物并接受电子对。AlCl3可以与木质纤维中的羟基(-OH)配位,削弱糖苷键和醚键的强度,促进反应物的降解。同时,AlCl3还能与水分子配位,生成H+和Al(OH)n+复合物,起到类似布朗斯特酸的作用[9]。结合实验结果,H2SO4更适用于催化水解具有复杂聚合物结构和大量糖苷键结构的木质纤维生物质原料,能够提供大量的H+,有效促进糖苷键的水解断裂,同时对中间产物也具有催化降解的作用。而AlCl3适用于催化结构相对简单,不需要经过复杂水解过程的多糖类化合物生成5-HMF,且AlCl3与糖分子形成的配位复合物能够稳定中间产物,抑制副反应(如聚合、缩合等)的发生。AlCl3的路易斯酸性相对温和,在催化多糖类化合物时能够获得较高的5-HMF产率和选择性。
因此,H2SO4适用于催化水解结构复杂的木质纤维生物质,主要因为其强布朗斯特酸性能够有效促进木质纤维的解聚和糖苷键的断裂;而AlCl3适用于催化多糖类化合物生成5-HMF,主要因为其路易斯酸性与糖分子配位,活化羰基,促进脱水反应并抑制副反应的发生。在实际应用中,可根据原料的特性选择合适的催化剂,以获得最佳的5-HMF产率和选择性。
-
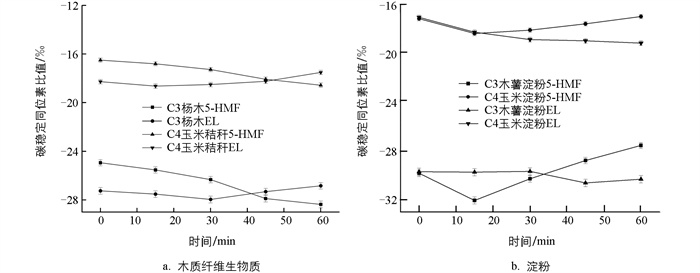
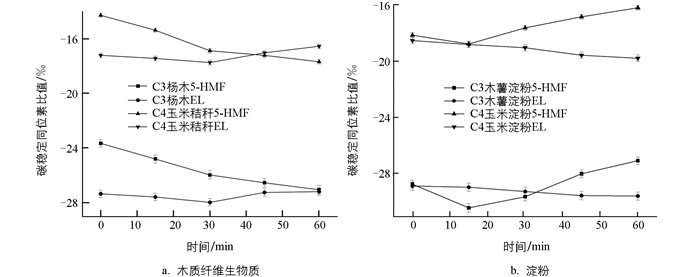
利用同位素比值质谱对反应过程中生成的2种关键化合物5-HMF和EL的碳稳定同位素比值进行测定。图 3、图 4分别展示了C3、C4原料在H2SO4和AlCl3催化反应下的碳稳定同位素比值随反应时间的变化情况。5-HMF和EL在0~60 min内均发生了显著的碳稳定同位素分馏现象。淀粉类原料生成中间产物5-HMF的碳稳定同位素比值从反应初始阶段至反应后期呈现先减小后增加的趋势,末端产物EL的碳稳定同位素比值则表现为随反应时间逐步递减的趋势。由于原子质量的差异,碳轻同位素12C相较于碳重同位素13C在化学反应中形成或断裂化学键所需的能量较低,因此更易参与反应[10]。随着反应时间的增加,动力学同位素效应将导致5-HMF中碳重同位素逐渐富集,而EL中则表现出碳轻同位素的富集现象,这种显著的碳稳定同位素富集现象为反应的进行提供了直接的证据[11-12]。
在某一时间段内,碳稳定同位素的分馏趋势可以作为表示产物产率变化的特征值[13-14]。如图 3所示,淀粉类原料在15 min时,5-HMF的碳稳定同位素比值达到较小值,这表明5-HMF产率达到最高值。在反应开始的20 min内,碳轻同位素的显著富集表明5-HMF在这一时间段内快速生成。同时,AlCl3提供的H+浓度降低,导致反应速率减缓,相同时间内碳键断裂次数减少,从而造成碳稳定同位素分馏趋势较为平缓,分馏特征不明显。相比之下,如图 4所示,木质纤维原料在较高pH值环境下使用H2SO4作为催化剂能够获得更高产率的5-HMF,反应体系内稳定的H+浓度使反应速率更加稳定,因此5-HMF碳稳定同位素分馏特征表现出较为显著的富集趋势。
-
采用瑞利方程对5-HMF、EL在水热液化过程中的转化效率及其碳稳定同位素组成进行讨论(表 1、表 2),以便探究C3、C4生物质原料在液化过程中产物的碳稳定同位素富集程度[15]。通过线性回归评估了相关系数R2与1的接近程度,以此判断同位素分馏过程遵循瑞利分馏模型的程度[16]。富集因子ε和富集系数εrp是表征水热液化过程中碳稳定同位素分馏特征的重要指标[17]。ε越大,表示轻同位素在产物中富集程度越高,反应速率越快;εrp则进一步考虑了反应点位数对分馏效应的影响。通过计算和比较不同原料、产物、催化剂体系下的ε和εrp,可以揭示它们在反应过程中的差异,为优化反应条件、提高目标产物选择性提供理论依据。同时,根据瑞利方程计算出反应过程中碳稳定同位素的富集因子ε。当ε>0时,表明正的动力学同位素效应占主导地位,体现了降解反应的优势;而ε<0时,则表示负的动力学同位素效应更为显著,说明生成反应处于主导地位[18]。值得注意的是,作为一种中间产物,5-HMF在水热液化过程中既可以是生成物也可以是反应物。在分析淀粉和木质纤维生物质液化过程中5-HMF浓度的变化规律时,发现其浓度先升后降,因此在进行线性回归分析时将5-HMF作为生成物进行分析。依据瑞利方程的特性[19],采用强制曲线通过原点的方式对ε进行了校正。
采用瑞利方程获得的ε仅代表重同位素在反应物中富集的平均趋势,而并非单个反应点位的分馏趋势[20]。所以在瑞利方程基础上可对ε进一步计算εrp,结果如表 3所示。
通过计算瑞利方程中的ε,定量描述了产物生成过程中碳稳定同位素的分馏特征[21-23]。结果表明:实验采用原料生成5-HMF和EL的过程都符合瑞利分馏模型,但不同原料和产物之间的ε存在差异。这些差异体现了原料在反应生成产物过程中的行为不同。例如,淀粉类原料生成5-HMF和EL的ε普遍高于木质纤维原料,说明前者的反应速率更快,轻同位素富集程度更高。分析中间产物5-HMF和终端产物EL在反应过程中碳稳定同位素组成的变化,发现两者虽然都符合瑞利分馏模型,但在轻、重同位素富集趋势上有所不同。碳轻、重同位素在反应物、中间产物和最终产物之间的不断分配和富集,形成了复杂而有规律的同位素分馏特征。
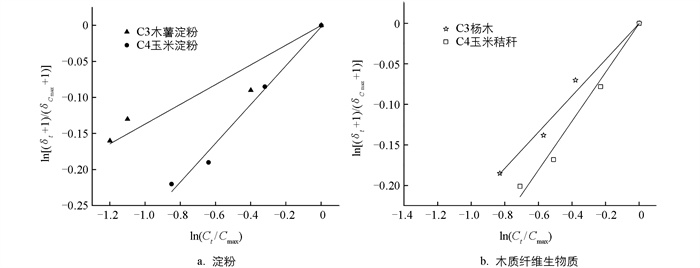
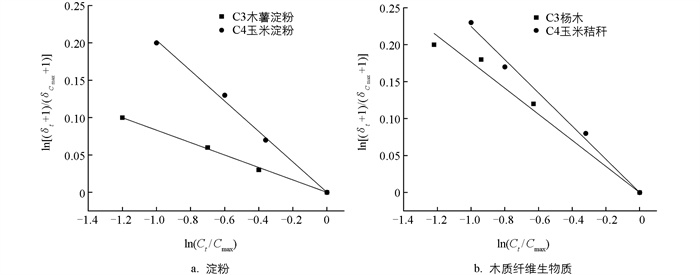
在水热液化过程中,5-HMF是一种重要的中间产物,它既可以由淀粉、纤维素等原料经脱水反应生成,也可以进一步转化为EL等终端产物。由2.1节中的数据可知,5-HMF的生成和转化过程都伴随着显著的碳稳定同位素动态分馏效应。例如,在5-HMF的生成阶段,碳轻同位素12C优先参与反应,导致在反应初期产物中12C富集。以C4玉米淀粉为例,在AlCl3催化下,5-HMF的碳稳定同位素比值从反应初始的(-18.151±0.022)‰降低至18 min时的(-18.771±0.017)‰(图 1a),表明12C在产物中不断富集。这是因为12C参与形成C-C键和C-O键的能垒较低,反应速率更快。随着反应的进行,5-HMF进一步转化为EL等产物。在这一过程中,5-HMF分子中的12C逐渐分馏,导致残留的5-HMF逐渐富集13C。5-HMF的碳稳定同位素比值从18 min的(-18.771±0.017)‰上升至60 min的(-16.210±0.009)‰(图 1a),反映了碳重同位素逐步富集的趋势。此时,生成的EL产物则表现出明显的12C富集特征(碳稳定同位素比值持续降低,图 3b)。通过对比不同反应时间下5-HMF和EL的碳稳定同位素比值,可以清晰地看出碳稳定同位素在这2个关键产物之间的动态分馏过程。图 5和图 6分别展示了淀粉类原料和木质纤维生物质在生成5-HMF和EL过程中的瑞利分馏特征模型曲线,该曲线图是通过将实验中测得的不同时间点的产物浓度比(Ct/Cmax)与其对应的碳稳定同位素比值进行关联分析所得。瑞利分馏模型分析方法能够有效揭示反应过程中碳稳定同位素的分馏机制和动力学特征,拟合结果也证实了这一规律的普适性[24]。
不同催化剂和原料体系下5-HMF的碳稳定同位素组成变化趋势虽然相似,但在富集因子ε和反应速率上存在差异。例如,由表 1可知,H2SO4催化下C3木薯淀粉生成5-HMF的ε值低于C4玉米淀粉,但前者的反应速率却高于后者,这表明原料结构和催化剂性质等因素影响了5-HMF生成过程中的碳稳定同位素分馏效应。
2.1. 不同催化体系下产物的5-HMF产率及碳稳定同位素比值差异分析
2.2. 中间产物5-HMF及末端产物EL的碳稳定同位素分馏特征
2.3. 碳稳定同位素富集因子及表观动力学比较
-
催化剂类型对5-HMF、EL产率和碳稳定同位素分馏产生影响,H2SO4作为催化剂对木质纤维原料生成5-HMF的催化效率更高,产率更大;AlCl3更适用于多糖类化合物(如淀粉等原料)生成5-HMF的反应。2种催化体系下碳轻同位素12C在5-HMF生成过程中均先于碳重同位素13C出现分馏现象。H2SO4催化下碳稳定同位素分馏现象更显著,且催化剂类型影响碳稳定同位素分馏特征并能够体现反应进程。5-HMF作为中间产物,其生成和转化过程都伴随着显著的碳稳定同位素动态分馏效应。在5-HMF的生成阶段,碳轻同位素12C优先参与反应,导致在反应初期产物中12C富集。同时,瑞利分馏模型能够描述5-HMF和EL生成过程中碳稳定同位素组成的变化规律,原料结构和催化剂性质等因素也会对5-HMF生成过程中的碳稳定同位素分馏效应产生影响。
本研究系统地比较了H2SO4和AlCl3 2种催化剂对不同类型生物质原料在水热液化过程中碳稳定同位素分馏机制的影响,解释了催化剂类型和原料性质对碳稳定同位素分馏和产物生成的作用机制以及不同原料、产物、催化剂体系在水热液化反应过程中碳稳定同位素分馏的差异,为优化反应条件、提高目标产物选择性以及探究反应机理提供了新的视角和理论依据。



 下载:
下载: