-
开放科学(资源服务)标识码(OSID):

-
菠菜(Spinacia oleracea L.)是我国各省区均有栽培的苋科1年生草本植物,富含丰富的蛋白质、铁、维生素和矿物质,具有丰富的营养价值,深受广大消费者的喜爱。近几年来,随着菠菜鲜食、加工业市场的不断发展,菠菜的价值也在不断提升。菠菜种植面积的扩大、化肥农药的不合理使用导致其抗性降低,因此菠菜生产中面临的病害问题也日趋严重,其中菠菜炭疽病、霜霉病和叶斑病等已成为目前制约菠菜高产优质的重要病害[1]。
菠菜炭疽病主要危害菠菜的叶片和茎,也危害叶柄、花和果皮[2]。病害通常从基部叶片开始发生,叶片染病时,初生水渍状淡黄色小斑,扩大后呈黄褐色、椭圆形或不规则形轮纹状病斑,中央有黑色小点,病斑中央呈灰白色,半透明,易穿孔,病斑连接成片,使叶片枯黄[3]。成株期染病主要发生于茎部,病斑为纺锤形或梭形,凹陷较深,中间灰白色,边缘灰褐色,密生黑色轮纹状排列小粒点,病部组织逐渐干腐,造成上部茎叶折倒,叶片变黄早枯,影响产量[4]。在陕西省,秋季高湿多雨,地势低洼、田间湿度大的田块发病早且严重。此外,反季节栽培、早播、密植等农事操作易造成田间通风透光不良、植株抗性下降,从而加剧病害的流行。
菠菜炭疽菌(Colletotrichum spinaciae),属半知菌类真菌。近年来,C. spinaciae被认为是菠菜炭疽病的主要致病菌,也有报道球炭疽菌(C. coccodes)和平头炭疽菌(C. truncatum)可引起菠菜的炭疽病[5]。目前对于菠菜炭疽病的防治仍以化学防治为主。为了明确陕西省菠菜炭疽病的病原菌,筛选低毒高效的杀菌剂,本研究对陕西省菠菜炭疽病的病原菌进行了分离鉴定,同时还进行了室内生物活性测定和防效验证,旨在筛选出高效杀菌剂,为该病的研究与防治提供理论依据。
全文HTML
-
菠菜炭疽病病样,采集于陕西省咸阳市武功县武功镇洛阳村。
-
大叶菠菜,河南农家旺种业有限公司;优菠66,河南鼎优农业科技有限公司。
-
250 g/L吡唑醚菌酯乳油(EC),巴斯夫植物保护(江苏)有限公司;560 g/L嘧菌·百菌清悬浮剂(SC),325 g/L苯甲·嘧菌酯悬浮剂(SC),先正达南通作物保护有限公司;45%咪鲜胺悬浮剂(SC),深圳诺普信农化有限公司;29%戊唑·嘧菌酯悬浮剂(SC),安道麦马克西姆有限公司;40%苯甲·吡唑酯悬浮剂(SC),广东真格生物科技有限公司;16%二氰·吡唑酯水分散粒剂(WG),巴斯夫欧洲公司;10%苯醚甲环唑水分散粒剂(WG),东莞市瑞德丰生物科技有限公司;70%甲基硫菌灵可湿性粉剂(WP),允发化工(上海)有限公司;50%多菌灵可湿性粉剂(WP),四川润尔科技有限公司。
-
用接种针直接挑取病斑表面黑色分生孢子盘,置于2 mL离心管中,采用稀释分离法[6]获得分离株单菌落。将纯化后的菌株编号,4 ℃冰箱保存。
-
将分离获得的菌株经PDA活化后,用直径6 mm打孔器于菌落边缘打取菌饼接种于新的PDA平板上。21 ℃黑暗培养7 d后测菌落直径,观察并记录菌落形态、颜色、质地等。在光学显微镜下观察其产孢结构、分生孢子形态与大小、附着胞形态等微观特征,3次重复。
-
采用CTAB法提取真菌DNA,采用陕西擎科生物科技有限公司合成的引物对致病菌株DNA进行PCR扩增(表 1)。扩增体系(50 μL)包括Tap PCR Master Mix 25 μL、上下游引物各2 μL、模板DNA 2 μL、dd H2O 19 μL。1%琼脂糖凝胶电泳检测DNA和PCR扩增产物。将合格产物送至陕西擎科生物科技有限公司进行测序。测序结果在NCBI中进行BLAST比对,将每个基因结合模式菌株的参考序列用软件MEGA 7.0中的Clustal W对齐、切除两端,之后按照ITS、ACT、CHS1、GAPDH、TUB2、HIS3的顺序首尾相连,与已知炭疽病菌种的标准序列进行比对(表 2),以Monilochaetes Infuscans为外群[7],用MEGA 7.0以最大似然法(Maximum Likeli-Hood)构建系统发育树。
-
选择代表性分离株在PDA平板上21 ℃培养7 d,用无菌涂布器刮擦菌落表面菌丝,均匀涂抹至新的PDA平板内,继续培养10 d,待产孢后配制成1×106个/mL的孢悬液(吐温20质量分数为0.01%)。将孢悬液均匀喷于60日龄的大叶菠菜叶片表面,接种后置25 ℃育苗箱内保湿培养48 h,后取出25 ℃、14 h光照/10 h黑暗温室中继续培养,早晚各喷水1次。观察记录发病情况,待叶片发病后,根据柯赫氏法则,采用组织分离法于病健交界处再次分离病原菌,与初次分离菌对比,确定是否为该致病菌。
-
采用菌丝生长速率法[13],每个处理4次重复,21 ℃培养10 d后测量各药剂处理的菌落直径,计算不同药剂处理对菌丝的生长抑制率。用DPS数据处理系统建立毒力回归方程,计算相关系数r和抑制中浓度EC50。
-
菠菜种植前先在室内进行催芽,待种子萌发后,种植于育苗盘中,培养35 d,移植到型号为10 cm×10 cm×10 cm的花盆内,每盆留苗1株,培养至45 d用于接菌。分生孢子悬浮液的配置方法和接种方法同1.2.4。药剂设16%二氰·吡唑酯WG 500倍液、50%多菌灵WP 500倍液,250 g/L吡唑醚菌酯EC 1 000倍液、45%咪鲜胺SC 1 000倍液,40%苯甲·吡唑酯SC 2 000倍液5个处理,以喷施无菌水为对照。使用喷壶(型号250 mL)向菠菜幼苗分别喷10 mL的病原菌和10 mL药剂,每处理喷8株菠菜,4次重复。盆栽试验分保护试验和治疗试验,保护组先喷药24 h后再喷菌,治疗组先喷菌24 h后再喷药。所有处理25 ℃保湿培养48 h,然后摘除保湿盖,14 h光照/10 h黑暗温室继续培养。接种后10 d,依据菠菜炭疽病分级标准检查各处理的病情严重度,计算病情指数和防效。病害分级标准[7]:0级,叶片无病斑;1级,病斑占叶面积的1%~25%;2级,病斑占叶面积的26%~50%;3级,病斑占叶面积的51%~75%;4级,病斑占叶面积的76%~100%。
-
采用随机区组设计,在优菠66菠菜田自然发病条件下进行试验。小区面积6 m2,小区间隔0.8 m。供试5种药剂分别设置1 000倍液和2 000倍液2个浓度,喷清水为空白对照,共12个处理,每处理3次重复,在田间植株叶片上出现零星水渍状病斑时开始喷药(出苗后60 d),间隔10 d喷药1次,共喷施3次。末次喷药后30 d,每处理各随机调查30株,统一检查最下层4~5片叶的发病情况,记录病害等级,并据此计算发病率、病情指数和防效。
-
数据用SPSS 19.0软件进行统计分析,采用Duncan氏新复极差法进行各处理间的差异显著性检验,p<0.05表示差异有统计学意义。
1.1. 材料
1.1.1. 供试病样
1.1.2. 供试菠菜品种
1.1.3. 供试药剂
1.2. 方法
1.2.1. 分离与纯化
1.2.2. 病原物的形态学观察
1.2.3. 病原物的分子生物学鉴定
1.2.4. 致病性测定
1.2.5. 菠菜炭疽病菌对10种药剂的敏感性测定
1.2.6. 不同药剂对菠菜炭疽病的盆栽防效
1.2.7. 不同药剂对菠菜炭疽病的田间防效
1.3. 数据处理
-
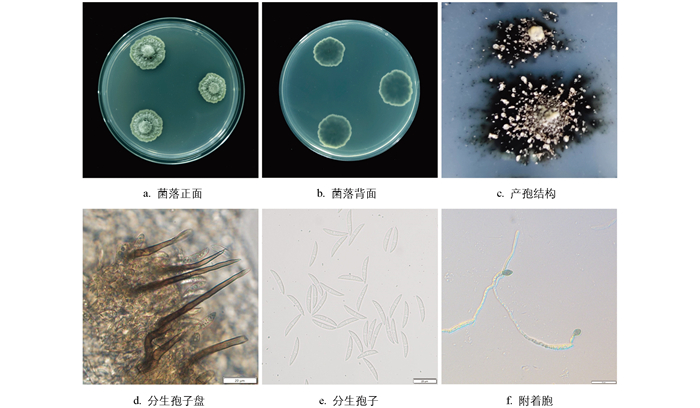
菠菜炭疽菌主要危害菠菜叶片,也危害茎、花和果实(图 1)。苗期叶片染病时,初生水渍状淡黄色小斑,病斑半透明;扩大后呈黄褐色,椭圆形、纺锤形、梭形或不规则形轮纹状病斑,中央有黑色小点,其为病菌的分生孢子盘;后期易穿孔;危害严重时病斑连接成片形成孔洞,造成叶片枯黄(图 1a)。成株期染病时,病害通常从基部叶片开始自下而上发生,主要危害叶片、茎、花和果实;病斑为纺锤形或梭形,凹陷较深,中间灰白色,边缘灰褐色,密生黑色轮纹状排列小粒点,严重时病组织干腐,造成上部茎叶折倒,叶片变黄早枯(图 1b),影响种子的品质和产量。
-
病原菌在PDA平板上21 ℃黑暗培养7 d,菌落平均直径为19.8 mm。菌落边缘不规则,气生菌丝白色或灰白色,致密(图 2a,2b)。7 d后,将菌丝刮除,21 ℃黑暗继续培养7 d,可见菌落表面生出白色的“脓状物”(图 2c),其为大量的分生孢子盘和分生孢子。分生孢子盘上着生刚毛和分生孢子;刚毛直立,末端尖锐,褐色或深褐色,有隔,大小为(52.0~83.5) μm×(4.0~5.5) μm(图 2d)。分生孢子单胞,镰状,向两端渐尖,无色,具油球,大小为(22.0~25.5) μm×(3.0~4.5) μm (n=50)(图 2e)。附着胞末端膨大,颜色较深,褐色至黑褐色,近球形,边缘光滑(图 2f)。
-
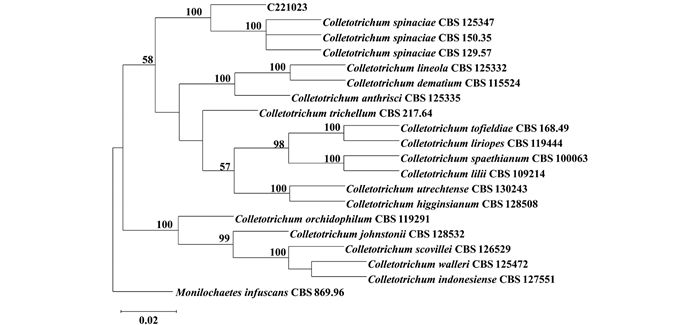
基于ITS、ACT、CHS1、GAPDH、TUB2和HIS3 6个多基因位点对病原菌进行分子鉴定与系统发育分析,其PCR扩增片段长度分别为541、297、327、268、509、400 bp。图 3显示,菌株C221023与Colletotrichum spinaciae聚在同一分支上,节点支持率为100%。结合形态学将菌株C221023鉴定为菠菜炭疽菌C. spinaciae。
-
将分离纯化后的菌株编号为C221023,培养至产孢(图 4a),将孢悬液均匀喷于60日龄的菠菜叶片表面。室内接种孢悬浮液48 h后,可见水渍状褪绿斑(图 4b);接种8 d后,表现出与田间相同的症状(图 4c)。从接种发病的病叶重新分离的病原物与第一次分离物相同,证明该分离物是引起菠菜炭疽病的病原菌。
-
敏感性测定结果表明,供试10种杀菌剂对菠菜炭疽菌均有一定的抑制作用(表 3),其中45%咪鲜胺SC、250 g/L吡唑醚菌酯EC、16%二氰·吡唑酯WG、40%苯甲·吡唑酯SC对菌丝生长具有明显的抑制效果,其EC50分别为0.055 9、0.092 9、0.162 9、0.307 5 mg/L,均小于1.0 mg/L。50%多菌灵WP、560 g/L嘧菌·百菌清SC等6种药剂EC50为1.291 9~6.264 2 mg/L,均大于1.0 mg/L。
-
供试5种杀菌剂对菠菜炭疽病的保护和治疗效果如表 4。40%苯甲·吡唑酯SC室内盆栽防效最好,对菠菜炭疽病同时具有治疗作用和保护作用,且治疗作用效果(73.06%)强于保护作用效果(68.55%)。其次,250 g/L吡唑醚菌酯EC和16%二氰·吡唑酯WG防效也较佳,45%咪鲜胺SC和50%多菌灵WP防治效果基本相同。
-
供试的5种杀菌剂除45%咪鲜胺SC外,田间防效均高于55%(表 5)。250 g/L吡唑醚菌酯EC防效最佳,1 000倍液和2 000倍液对菠菜炭疽病的防效分别为88.67%和87.86%,与其他处理间差异有统计学意义;50%多菌灵WP和40%苯甲·吡唑酯SC防效较好,1 000倍液的防效均为68.67%,二者差异无统计学意义;45%咪鲜胺SC和16%二氰·吡唑酯WG防效低于以上3种药剂。
2.1. 菠菜炭疽病田间症状
2.2. 菠菜炭疽病病原菌形态鉴定
2.3. 菠菜炭疽病病原菌分子生物学鉴定
2.4. 致病性测定
2.5. 菠菜炭疽菌对10种药剂的敏感性测定
2.6. 不同药剂对菠菜炭疽病的室内盆栽防效
2.7. 不同药剂对菠菜炭疽病的田间防效
-
菠菜炭疽病是菠菜生产上主要叶斑病之一,在加拿大[14]、美国[15]、澳大利亚[16]、土耳其、加利福尼亚等菠菜产区均有报道,造成了严重的产量和经济损失。C. dematium f. sp. spinaciae通常被认为是菠菜和甜菜的一种病原体[17]。Von Arx[18]将菠菜炭疽病的致病菌描述为C. dematium,考虑到宿主特异性,将菠菜炭疽菌的病原菌命名为C. dematium f. sp. spinaciae。
病原菌在PDA平板上生长速度较慢,培养7 d的菌落呈圆形或不规则形,白色、灰白色至灰色,培养21 d的病原菌在PDA平板上产孢量较少或不产孢。本研究显示,玻片刮除菌丝或菌饼在平板上涂布接种可产生大量的分生孢子。分生孢子单孢无色,镰状,具有油球,附着胞末端膨大,颜色较深,褐色至黑褐色,与国外Damm等[17]、Kurt等[19]描述的菠菜炭疽菌,国内侵染线辣椒[20]、箭筈豌豆[21]的菠菜炭疽菌菌落形态、分生孢子形态特征基本一致。综合病原菌形态与分子生物学鉴定结果,认为陕西省菠菜炭疽病的致病菌为C. spinaciae。
目前已经有很多炭疽病药剂筛选的研究报道[22-23],但是引起炭疽病的病原菌种类很多[24],同种药剂对不同病原菌室内生物活性的抑制仍然存在较大差异。在菠菜炭疽病的防治上,应选择抑菌效果好的药剂。本研究测定了菠菜炭疽菌对10种杀菌剂的敏感性,筛选出45%咪鲜胺SC、250 g/L吡唑醚菌酯EC、16%二氰·吡唑酯WG、40%苯甲·吡唑酯SC等4种EC50小于1.0 mg/L的高效药剂,这与王琼[25]的研究结果一致。在室内盆栽防效试验中,40%苯甲·吡唑酯SC、250 g/L吡唑醚菌酯EC防效较好,兼具治疗作用和保护作用。菠菜炭疽病田间防效试验结果与盆栽防效结果不同,250 g/L吡唑醚菌酯EC和50%多菌灵WP田间防效优于40%苯甲·吡唑酯SC,产生差异的原因可能与光照、温湿度、土壤条件、病菌接种量、植株生长差异、药剂喷雾量等有关。Uysal等[26]研究表明,接种量、温度、保湿时间、植株叶龄对菠菜炭疽病发病都有影响,且老叶发病比嫩叶发病更为严重,这与本研究田间试验菠菜炭疽病老叶发病较新叶发病严重结果一致。250 g/L吡唑醚菌酯EC、50%多菌灵WP、40%苯甲·吡唑酯SC可有效防治不同炭疽菌引起的多种作物炭疽病,这与周洁等[27]的研究结果一致,为此,菠菜炭疽病发生时可交替使用这3种药剂进行防治。这3种药剂对菠菜炭疽病虽表现出良好的田间防效,但其高效且安全的应用方案,如施用剂量、施药时期、施用频率和安全间隔期等,仍需结合田间管理并经多年试验验证,以兼顾药效与农药减量。




 下载:
下载: