-
开放科学(资源服务)标识码(OSID):

-
随着全球工业化进程的快速推进,重金属污染已成人类面临的严峻挑战。污水灌溉、化肥滥用及工业废物的过量排放,导致重金属在土壤中大量沉积[1]。这些重金属通过农作物的根系作用被吸收,并最终通过食物链进入人体。重金属(如Cd2+、Pb2+)即使处于痕量水平也会对人体器官构成严重损害,过量的Zn2+、Cu2+等同样也会对作物以及人体造成一定的伤害[2-3]。因此,开发快速、灵敏、准确的土壤重金属检测技术,对于环境监测和农业安全具有重要意义。
目前,实验室常用的重金属检测方法主要包括原子吸收光谱法(Atomic Absorption Spectroscopy,AAS)、电感耦合等离子体质谱法(Inductively Coupled Plasma Mass Spectrometry,ICP-MS)、电感耦合等离子体原子发射光谱法(Inductively Coupled Plasma Atomic Emission Spectrometry,ICP-AES)等。这些方法尽管具有灵敏度高、准确度高的优势,也通常作为国家或行业标准分析方法[4-5],但存在仪器价格昂贵、体积大、样品前处理要求高、操作复杂等不足[6],难以满足现场快速检测的需求。电化学分析方法,尤其是方波阳极溶出伏安法(Square-Wave Anodic Stripping Voltammetry,SWASV),具有灵敏度高、设备便携、成本低、可同时分析多种重金属等优势,可以用于土壤中痕量重金属的现场快速检测[7-9]。
传统的电化学分析方法通常使用一元线性回归(Univariate Linear Regression,ULR)模型进行定量分析,即假设电化学溶出电流信号(峰电流强度)与目标离子浓度之间存在简单的线性关系[10-11]。在单一组分或理想的样品溶液环境中,这种方法可取得良好的检测效果。然而,土壤的成分复杂,含有丰富的有机物、无机阴离子、金属阳离子[12],均会影响电化学溶出伏安法的检测精度。已有学者开展了电化学干扰因素研究,提出了多种干扰抑制方法,有效解决了土壤溶解性有机物(例如腐殖质、活性剂)、无机离子的干扰[13]。但是,多种重金属之间的交互干扰问题尚未得到有效解决。在电化学分析过程中,重金属离子之间会发生复杂的相互作用(例如生成复杂合金、竞争活性位点、置换反应等)[14-16]。在沉积阶段,多种重金属离子会一起被还原到电极表面,影响目标重金属的沉积量;在溶出阶段,形成复杂的合金会阻碍目标重金属的溶出,导致信号减小或电位偏移,最终干扰SWASV检测[17-18]。因此,目标重金属的溶出伏安信号不仅取决于其自身浓度,还受到共存重金属种类和浓度的影响,信号与浓度之间呈现出复杂的非线性关系。传统的ULR模型无法有效解析这种复杂的交互干扰信息,导致检测结果严重偏离真实值[13]。
针对上述问题,已有研究尝试将机器学习(Machine Learning,ML)算法与电化学分析方法相结合,提升土壤样品中重金属的检测精度。例如,Liu等[19]分析了土壤中Cu2+对Pb2+的干扰,以峰电流作为输入特征建立支持向量回归(Support Vector Regression,SVR)模型,相比ULR模型,提高了Cu2+存在时Pb2+的检测准确度。这是因为ML算法具有强大的数据挖掘和非线性映射能力,能够从多维数据中学习输入信号与输出浓度之间的复杂关系,可以为电化学检测中的多种重金属共存导致的非线性干扰提供新的解决思路。
但现有研究大多局限于某一种重金属的干扰分析和单一目标重金属的检测,多种重金属交互干扰和同步检测问题尚未得到有效解决[20-23]。受污染的土壤样品往往同时存在多种重金属,且不同重金属含量的差异性大[24-25],这进一步加剧了电化学检测准确性差的问题。实际上,溶出伏安曲线中除常规的峰电流强度外,还蕴含着峰宽、峰面积等多维特征信息[26],充分挖掘并利用这些信息,有望为复杂体系下检测精度的提升提供新方式。例如,Kayali等[27]将方波伏安正反向扫描的8个峰值参数(包括峰高、峰宽、峰面积等)输入随机森林模型进行数据分类,可在25 s内对K2Fe(CN)6的5种浓度实现100%准确分类;Xu等[28]则进一步证实了在多种组分共存的复杂体系中,引入峰高、峰面积、峰电位等多维特征可以有效解决仅依赖单一峰高特征导致的严重误判问题(误差大于30%),实现精准检测。这些研究表明构建多维特征输入的机器学习模型是提升复杂体系下检测精度的有效途径。
基于此,以重金属离子Cu2+、Zn2+、Cd2+、Pb2+为研究对象,提出机器学习辅助电化学溶出伏安检测方法。首先,分析重金属之间的干扰规律;其次,设计溶出电流特征信号提取算法,以准确获取不同重金属溶出电流的峰高、峰宽和峰面积信息;然后,建立多元非线性机器学习模型,以实现4种重金属的同步准确检测;最后,采集真实土壤样品,验证方法的实用性。研究成果有望为复杂土壤基体中多种重金属的同步准确检测提供新的技术支撑。
全文HTML
-
所有的电化学测量均在MultiEmStat4电化学工作站(Palmsens,荷兰)上进行,并连接电脑进行数据采集。实验采用标准的三电极体系:玻碳电极(Glass Carbon Electrode,GCE)作为工作电极,铂柱(Pt)电极(Φ 1 mm×15 mm)作为对电极,银氯化银(Ag/AgCl)电极作为参比电极,所需电极均购自武汉高仕睿联科技有限公司。
实验所用的重金属标准溶液(Cu2+、Zn2+、Cd2+、Pb2+)和硝酸铋溶液(Bi(NO3)3),浓度均为1 000 mg/L,购自国家标准物质中心;配置支持电解质所需的乙酸-乙酸钠缓冲液(NaAc/HAc),浓度为2 mol/L(稀释10倍后pH=5.0),购自北京奥博来科技有限公司;所有化学试剂均为分析纯;实验用水均为去离子水(电阻率为18.2 MΩ·cm)。
实验选取4份土壤样品进行方法验证,均取自湖南省长沙市。4份样品均作为外部验证集,不参与模型训练。
-
由于GCE表面洁净状态对检测结果存在影响,因此每次测量前对工作电极进行物理抛光和超声清洗,具体步骤如下:首先,将GCE在氧化铝(Al2O3)粉末与去离子水润湿的抛光布上呈“8”字形打磨80~100次,直至电极表面呈镜面光泽[29];然后,用去离子水冲洗掉Al2O3残留,将电极依次在稀硝酸、乙醇和去离子水中超声清洗各2 min,以彻底去除表面残留的杂质;最后,吹干备用。对电极和参比电极使用去离子水冲洗并晾干备用。
-
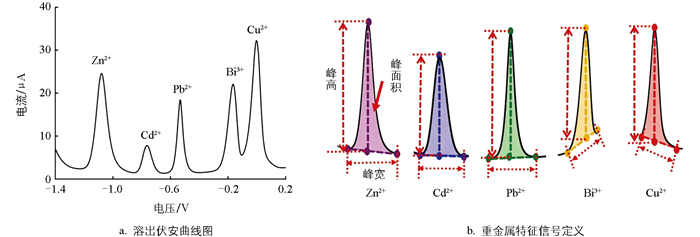
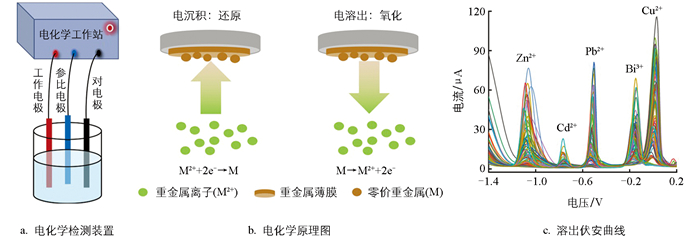
采用SWASV结合原位镀铋膜修饰GCE进行重金属离子的同步检测。首先,向电解池中添加9 mL去离子水,再添加1 mL乙酸缓冲液(0.2 mol/L、pH=5.0),得到支持电解质溶液;其次,将处理好的三电极插入电解池中;然后,向溶液中同时加入一定量的Bi3+溶液和目标重金属离子溶液,进行SWASV检测。其中,Bi3+和重金属离子同时被电化学沉积到GCE表面,形成原位电镀铋膜修饰电极[30-31]。SWASV检测装置与工作原理如图 1所示。
测试参数设置如下:首先,在搅拌条件(600 r/min)下,应用设定的沉积电位执行电沉积180 s,使Bi3+与目标金属离子共同沉积于电极表面并形成金属薄膜;随后,停止搅拌并静置10 s,使溶液能够达到平衡;接着,执行电溶出,在-1.4 ~ 0.2 V电位范围内进行方波阳极扫描,并记录溶出伏安曲线(如图 1c所示)。每次测量完成后,为去除电极表面残留的重金属,在0.35 V的电位下清洗120 s,以保证后续测试的重复性[32]。为保证测量数据的可靠性,每组测量均重复5次,取平均值作为测量结果。
-
为了高灵敏测量Cu2+、Zn2+、Cd2+、Pb2+ 4种重金属离子,分别优化了Bi3+离子浓度、沉积电压、沉积时间,确定最佳的测量参数。Bi3+离子浓度梯度设置为:0、100、200、300、400、500、600、700、800 μg/L;沉积电压梯度设置为:-0.2、-0.3、-0.4、-0.5、-0.6、-0.7、-0.8、-0.9、-1.0、-1.1、-1.2、-1.3、-1.4、-1.5 V;沉积时间梯度设置为:60、90、120、150、180、240、300 s。
-
对4种重金属离子分别进行浓度梯度实验,得出其溶出电流峰值随浓度变化的曲线,由此计算出4种重金属的灵敏度、检测限。4种重金属均设置9个浓度梯度。其中,Cu2+浓度梯度为:5、25、50、75、100、125、150、200、250 μg/L;Zn2+浓度梯度为:10、50、100、150、200、250、300、400、500 μg/L;Cd2+浓度梯度为:2、5、10、15、20、25、30、40、50 μg/L;Pb2+浓度梯度为:5、25、50、75、100、125、150、200、250 μg/L。接着,分析峰电流y与浓度x的关系,并进行线性拟合。其中,斜率k即灵敏度,拟合公式为:
检测限的计算公式为:
式中:σ为最低浓度重金属溶液重复测量5次所得溶出峰电流的标准差。
-
为了研究多金属共存体系下的交互干扰现象,将4种重金属溶液混合,记录各重金属离子溶出电流峰值随浓度变化的曲线。混合溶液的重金属浓度梯度与1.4.2节保持一致,建立线性校正曲线,计算4种重金属离子的检测限,并与单独溶液体系下的结果进行对比,据此判断共存条件下重金属离子之间是否存在相互影响。
为探究单一重金属离子对其他3种重金属离子的干扰效果,进一步开展了干扰离子实验。实验方法为:固定其他3种重金属离子的浓度,让干扰重金属离子的浓度逐渐增高,观察其对另外3种重金属离子电流信号的影响。其中,Cu2+、Zn2+、Cd2+、Pb2+分别作为干扰离子时,其自身浓度梯度设置如下:Cu2+浓度为0~400 μg/L、Zn2+浓度为0~800 μg/L、Cd2+浓度为0~120 μg/L、Pb2+浓度为0~250 μg/L。Cu2+作为干扰离子时,其余重金属浓度固定为:Zn2+ 300 μg/L、Cd2+ 50 μg/L、Pb2+ 200 μg/L;Zn2+作为干扰离子时,其余重金属浓度固定为:Cu2+ 25 μg/L、Cd2+ 30 μg/L、Pb2+ 200 μg/L;Cd2+作为干扰离子时,其余重金属浓度固定为:Cu2+ 25 μg/L、Zn2+ 200 μg/L、Pb2+ 100 μg/L;Pb2+作为干扰离子时,其余重金属浓度固定为:Cu2+ 25 μg/L、Zn2+ 200 μg/L、Cd2+ 25 μg/L,具体如表 1所示。
-
为建立机器学习模型,设计4因素(Cu2+、Zn2+、Cd2+、Pb2+ 4种重金属离子)、9水平(每种重金属设置9个浓度)实验。全组合实验需要采集6561(94)组数据,实验量过大,而且数据间存在大量重复。综合考虑浓度覆盖范围与实验成本,根据L81(94)正交表,采集81组样品数据用于建模分析。所有SWASV测量均在最佳实验参数下进行,每组样品重复测量5次,得到405条溶出伏安曲线。将每组数据取平均值,获得81组溶出伏安曲线,如图 1c所示。
为了提高数据分析效率,利用Python编程语言编写数据处理程序。针对原始伏安信号中存在的噪声干扰,采用S-G(Savitzky-Golay)滤波算法对数据进行平滑处理。在此基础上,设计自动寻峰算法,通过溶出电流峰的电位、峰与峰之间的相对距离来识别重金属种类。在峰识别完成后,进一步获取峰电流、峰面积及峰宽等特征信号,用于后续建模分析。重金属溶出伏安曲线及其特征信号如图 2a所示,其中,各重金属峰高、峰宽和峰面积的定义如图 2b所示。
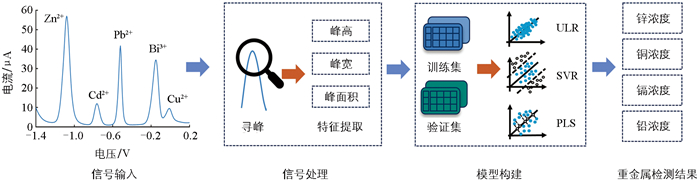
利用软件所提取的特征信号,采用3种算法,建立检测模型,试图校正重金属间的交互干扰,提高Cu2+、Zn2+、Cd2+、Pb2+ 4种重金属离子的检测精度。所建立的模型包括传统一元线性回归(Univariate Linear Regression,ULR)、偏最小二乘回归(Partial Least Squares Regression,PLS)、支持向量回归(Support Vector Regression,SVR)。模型为每种重金属独立训练,并分别评估性能以获得每种重金属的最优检测模型。整体模型构建框架如图 3所示。
为了确保模型性能对比的公平性与客观性,对输入变量、数据集划分和验证方式进行了统一设置。首先,在输入特征方面,ULR模型仅以溶出峰峰值电流(峰高)作为单一输入变量;而PLS和SVR模型均采用“峰高+峰宽+峰面积”三维特征作为输入。其次,在数据集划分及模型训练过程中,固定随机种子为774,数据集以8∶2的比例进行划分:在总计81个样品中,选取64个作为训练集用于模型构建,剩余的17个作为验证集用于性能评估。最后,在模型内部验证过程中统一采用5折交叉验证,以消除偶然误差,确保不同算法处理相同数据集的结果具有可比性。
-
为了评价不同模型对Cu2+、Zn2+、Cd2+、Pb2+ 4种重金属离子的检测性能,采用决定系数R2、均方根误差RMSE以及相对均方根误差rRMSE作为评价指标。Rc2、RMSEc、rRMSEc分别表示训练集的决定系数、均方根误差和相对均方根误差;Rv2、RMSEv、rRMSEv分别表示验证集的决定系数、均方根误差和相对均方根误差。
设样品的真实浓度为yi,模型预测值为$\hat{y}_i$,样品数为n,则3种指标定义如下:
1) 决定系数R2
式中:y为真实值均值。
R2反映了模型对浓度变化趋势的解释能力,越接近1表明拟合效果越好。
2) 均方根误差RMSE
RMSE反映了预测值与真实值之间的绝对偏差大小,单位与浓度一致,数值越小越好。
3) 相对均方根误差rRMSE
由于不同重金属的浓度范围存在显著差异,仅依赖R2和RMSE作为评价指标会使结果不够准确。因此,引入相对均方根误差rRMSE作为第3个评价指标,使得不同重金属之间的误差具有可比性。
rRMSE定义为RMSE与真实值的均值y之比,数值越小越好,其计算公式为:
-
为了评估机器学习辅助溶出伏安法的实用性,在湖南长沙采集了4份受污染土壤样品,开展加标回收验证。每份准确称量1 g,按照1∶10的固液比加入0.2 mol/L乙酸缓冲液,混合液以2 000 r/min的速度经振荡器振荡30 min,以充分溶解土壤。然后以8 000 r/min的速度离心10 min,静置后取上清液,经0.45 μm的滤膜过滤去除杂质[33]。为了消除土壤浸提液中可溶性有机质对溶出伏安信号的干扰,对上清液进行15 min的紫外光解处理[34],得到土壤待测液。
应用优化后的实验条件,采集样品的溶出伏安信号,随后对每份样品进行2次加标,并采集每次加标后的溶出伏安信号。将溶出伏安信号输入已训练好的模型,计算加标前后重金属的浓度以及加标回收率,评价模型的实用性。加标回收率的计算公式为:
式中:P为加标回收率;c1为样品原始浓度值;c2为加标后测定的总浓度值;Δc为加标量。
1.1. 仪器与试剂
1.2. 电极预处理
1.3. 电化学检测与参数设置
1.4. 电化学参数优化及重金属间干扰实验设计
1.4.1. 电化学检测关键参数优化
1.4.2. 灵敏度和检测限计算
1.4.3. 重金属交互干扰实验
1.5. 数据集采集和模型构建
1.6. 模型评价指标
1.7. 真实样品验证与加标回收率计算
-
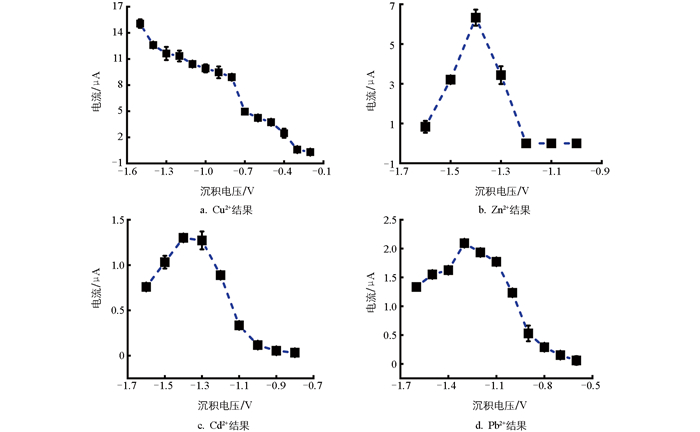
分析了Bi3+浓度、沉积电压和沉积时间3个关键参数对4种重金属溶出电流的影响,如图 4-图 6所示。
如图 4所示,除Zn2+的信号随Bi3+离子浓度增加而持续增强外,Cu2+、Cd2+、Pb2+的溶出电流均在Bi3+离子浓度小于400 μg/L时,随着Bi3+离子浓度的增加而增强,这是因为铋可以和待测金属形成合金,促进了待测离子在电极表面的富集。但当Bi3+的浓度过高时,Cu2+、Cd2+、Pb2+的信号强度都略有一定程度的下降,一方面,这可能是因为过高浓度的Bi3+导致电极表面形成的铋膜过厚,阻碍了电子传递[35];另一方面,过量的铋原子会占据有限的电极表面沉积位点,与待测离子产生竞争吸附[19],从而不利于目标重金属离子在电极表面的沉积。综合考虑,选择500 μg/L作为最佳Bi3+浓度。
如图 5所示,沉积电压对重金属离子的溶出电流也存在一定的影响,这是因为沉积电压的降低有利于重金属离子的电还原富集,但沉积电压过负时,除Cu2+的信号持续增强外,Zn2+、Cd2+、Pb2+的溶出信号均呈现明显的下降趋势。由于在过负的电位下,H+会发生析氢反应,氢气泡附着在电极表面阻碍了重金属离子的沉积[36],还可能破坏Bi3+膜的稳定性,导致检测灵敏度降低[37]。具体而言,不同的重金属离子所需的最佳沉积电压不同,Pb2+和Cd2+均在-1.3 V处取得最大值,而Zn2+的最大值出现在-1.4 V处。为了综合考虑在多离子共存的情况下各金属离子的还原效率,同时避免析氢反应的发生,最终确定最佳的沉积电压为-1.4 V。
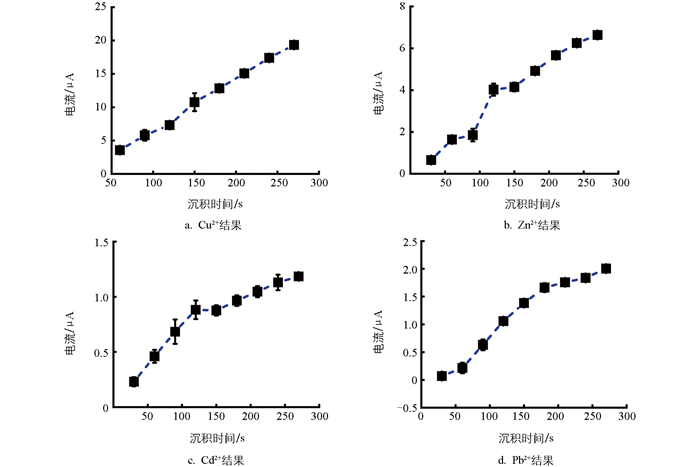
沉积时间的优化结果如图 6所示。沉积时间在50~300 s的范围内,溶出电流几乎表现出线性增加,这表明延长沉积时间能增加金属的富集量,并增加信号强度。为了同时考虑检测灵敏度和检测效率,最终选取180 s作为沉积时间。
-
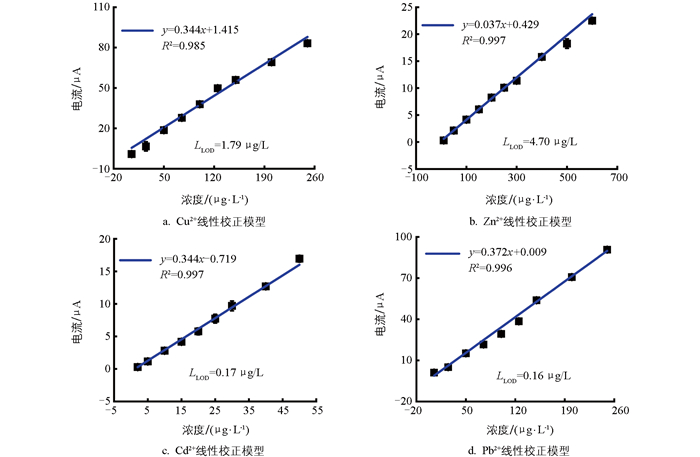
在最佳实验条件下,分别测定每种金属的溶出伏安曲线,如图 7所示。在单一重金属存在的情况下,Cu2+、Zn2+、Cd2+、Pb2+的溶出伏安响应信号与浓度均呈现出良好的线性关系,R2均高于0.985。4种重金属离子的检测限分别为:Cu2+ 1.79 μg/L、Zn2+ 4.70 μg/L、Cd2+ 0.17 μg/L、Pb2+ 0.16 μg/L,证明了溶出伏安法在单独检测1种重金属时具有优异的灵敏度和定量分析能力。
溶出伏安法对不同重金属的检测灵敏度(即线性回归方程的斜率)不尽相同。例如,Zn2+的灵敏度(0.037 μA/(μg·L-1))相对于其他重金属(Cu2+:0.344 μA/(μg·L-1)、Cd2+:0.344 μA/(μg·L-1)、Pb2+:0.372 μA/(μg·L-1))较低。这可能是因为与其他重金属相比,Zn2+的活泼性较高,不容易被电化学还原至电极表面,从而导致其溶出电流信号灵敏度较低[36]。
-
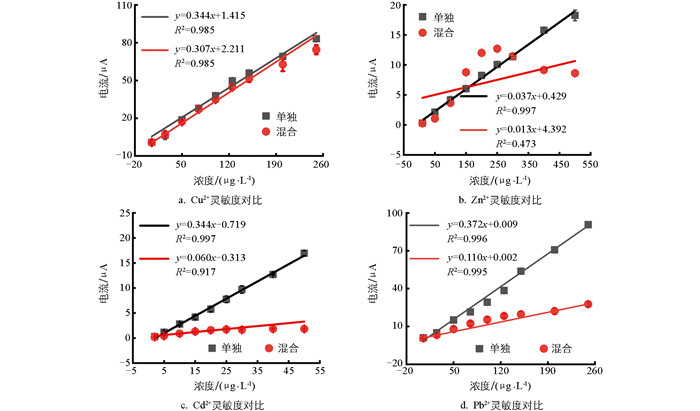
与单独溶液体系相比,混合体系下各重金属的线性校正曲线均发生了一定的偏移,灵敏度k(校正曲线斜率)和R2也大幅度下降,结果如图 8所示,证明了4种重金属离子之间存在严重的交互干扰。
在多种重金属共存的体系下,4种重金属离子的检测限、灵敏度和线性校正曲线R2均受到一定程度的影响。受干扰程度最严重的是Zn2+,其检测灵敏度从0.037 μA/(μg·L-1)降低到0.013 μA/(μg·L-1),检测限从4.70 μg/L增加至13.38 μg/L,是单独溶液体系下的3倍,线性校正曲线R2从0.997降低至0.473。Cd2+灵敏度从0.344 μA/(μg·L-1)降低到0.060 μA/(μg·L-1),检测限从0.17 μg/L大幅增加至1.00 μg/L,几乎是单独溶液体系下的6倍,线性校正曲线R2从0.997降低至0.917。Pb2+灵敏度从0.372 μA/(μg·L-1)降低到0.110 μA/(μg·L-1),检测限从0.16 μg/L增加至0.55 μg/L(约为单独溶液体系下的3倍),但其线性校正曲线R2仍维持在0.995的较高水平。Cu2+受干扰程度最小,其灵敏度从0.344 μA/(μg·L-1)稍微降低到0.307 μA/(μg·L-1),检测限和R2基本保持稳定。
综上所述,在混合溶液中重金属离子受干扰程度由大到小依次为Zn2+>Cd2+>Pb2+>Cu2+,这意味着在多种重金属共存的情况下,溶出伏安法对重金属的检测能力大幅减弱,难以满足对痕量重金属的准确检测需求。
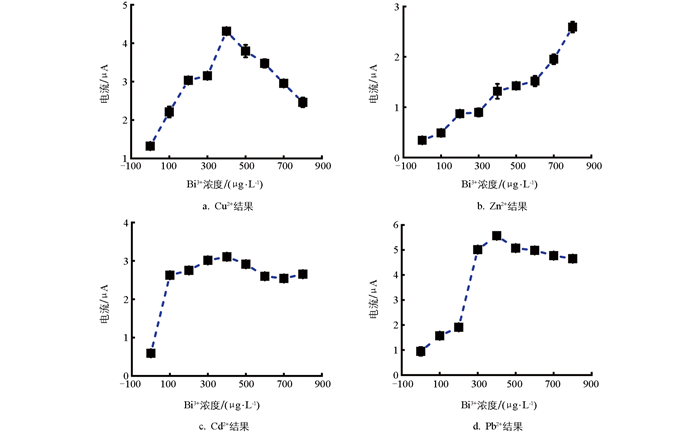
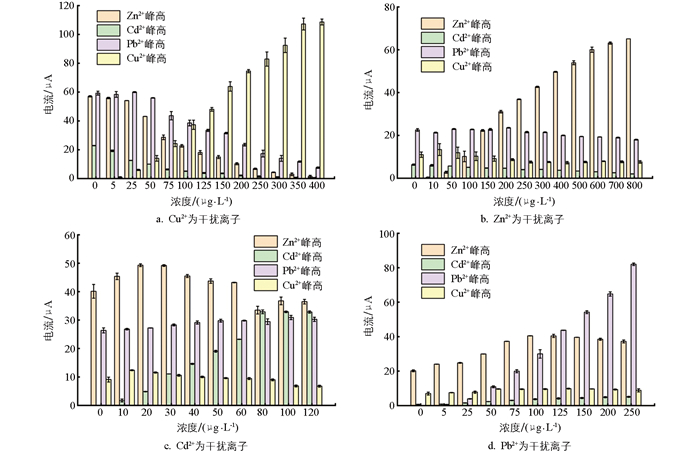
某种重金属对其他3种重金属的干扰实验结果如图 9所示。
如图 9a所示,随着Cu2+浓度的升高,其他重金属的电流信号均显著降低,尤其是Zn2+和Cd2+信号所受抑制最严重。当Cu2+的浓度达到400 μg/L时,Zn2+和Cd2+的电流信号降低至0,Pb2+的电流信号也衰减至初始值的四分之一。出现这种现象的原因可能是铜离子与其他重金属离子形成了复杂的合金,导致待测金属难以正常溶出[38]。
如图 9b所示,随着Zn2+浓度的升高,其他重金属的电流信号均呈现下降趋势,其中Cd2+信号所受抑制最为显著。当Zn2+浓度达到800 μg/L时,其电流信号衰减至初始值的三分之一;Cu2+和Pb2+的电流信号虽然有一定程度的降低,但是下降幅度相对较缓。
如图 9c所示,随着Cd2+浓度的升高,Pb2+电流信号强度呈缓慢增长趋势,Zn2+和Cu2+信号均先增强再缓慢降低。当Cd2+浓度大于10 μg/L后,Cu2+的电流信号开始下降,而Zn2+的电流信号在Cd2+浓度大于20 μg/L后开始下降。
如图 9d所示,随着Pb2+浓度的升高,Cd2+电流信号强度呈缓慢增长趋势;当Pb2+浓度小于100 μg/L时,Zn2+电流信号有所升高;当Pb2+浓度大于100 μg/L后,Zn2+电流信号呈现缓慢下降趋势;Cu2+的电流信号强度基本保持稳定。
上述结果表明,在多种重金属共存的体系中,各离子的峰电流不仅取决于自身浓度,还受到其他离子浓度的非线性影响,证实了传统ULR模型在混合溶液体系检测中具有一定的局限性。
-
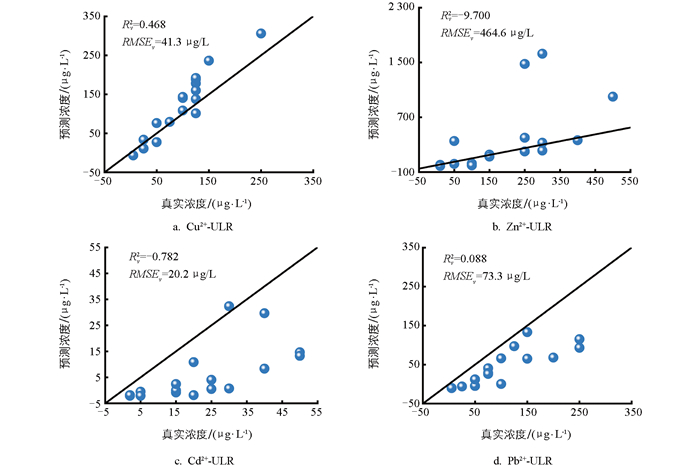
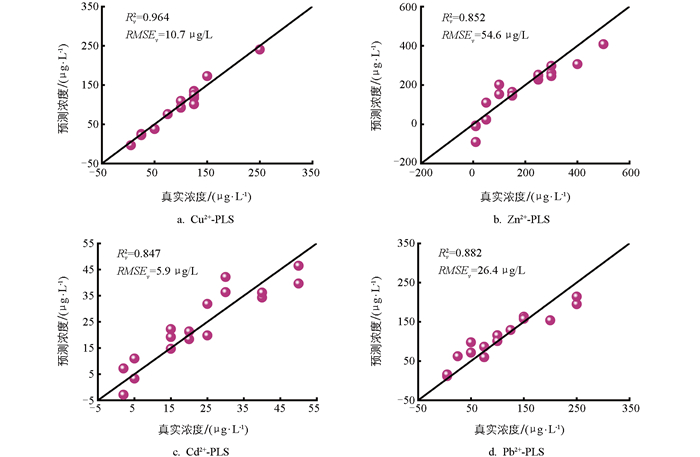
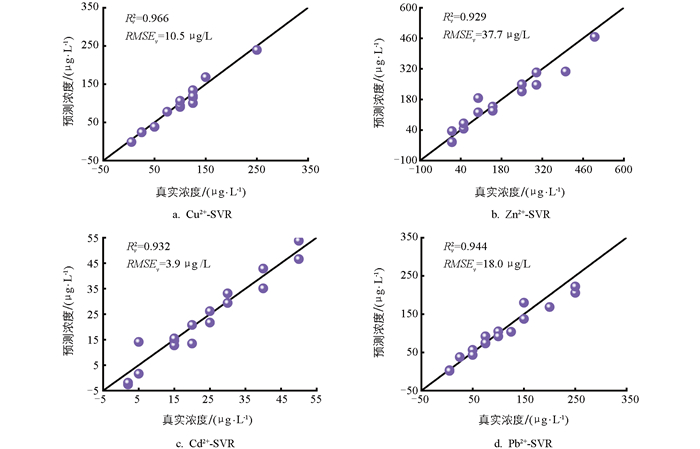
为了提高多种重金属同步检测的准确度,基于81组交叉正交实验数据,构建ULR、PLS、SVR 3种模型,并对比了模型在验证集上的检测值与真实值的差异,如图 10-图 12所示。
如图 10所示,ULR模型的检测精度整体较低,4种重金属的检测值与真实值偏差明显,尤其是Zn2+和Cd2+,其验证集决定系数Rv2出现负值,意味着模型无法有效检测这2种重金属离子的浓度。这一现象证明了在多种重金属共存的体系中,由于离子间存在严重交互干扰,溶出峰峰值电流与浓度之间不再遵循简单的线性关系,传统的ULR模型完全失效,无法满足准确检测的需求。引入了峰宽和峰面积特征后,建立的PLS模型检测精度相比于ULR有所提升,4种重金属的Rv2均达到0.8以上,如图 11所示,说明考虑溶出伏安信号的多维特征在一定程度上能够补偿多种重金属共存导致的信号干扰。但由于PLS本质上仍然属于线性回归模型,在处理严重的非线性干扰时,其校正能力仍然有限。从检测结果来看,除了Cu2+的rRMSEv为10.9%以外,Zn2+、Cd2+、Pb2+ 3种重金属离子的rRMSEv均大于25%,说明模型的检测精度仍有待提高。相比之下,SVR模型表现出最优的检测性能,其Rv2均达到0.9以上,rRMSEv降低至21%以下,4种金属离子的数据点均分布在1∶1线附近,如图 12所示,这一结果表明SVR模型能更好地拟合多维非线性关系,实现对重金属浓度的准确检测。
对比3个模型的训练集和验证集指标,如表 2所示。从R2、RMSE、rRMSE 3个指标综合考虑,模型性能均呈现出SVR最佳、PLS次之、ULR较差的趋势。此外,对比了SVR在训练集与验证集上的指标差异,两者的R2和RMSE差别较小,说明SVR模型未出现明显的过拟合现象,具备良好的泛化能力。综上,相比于ULR和PLS模型,SVR模型具有更强的多维非线性拟合能力,能够克服多种重金属交互干扰对检测结果的影响,进而有效提高了多种重金属同步检测的准确度。
-
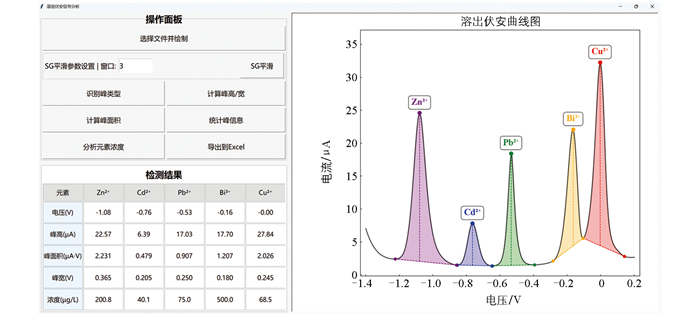
针对采集到的大量原始溶出伏安曲线,利用Python设计了一套重金属溶出伏安信号处理软件,旨在快速地实现数据处理和重金属浓度分析,软件界面如图 13所示。该软件集成了数据加载、S-G平滑滤波、自动寻峰以及特征提取等核心功能模块,能够快速提取溶出伏安信号的峰高、峰宽、峰面积等关键特征信号。软件内嵌了SVR模型,可同步检测Cu2+、Zn2+、Cd2+、Pb2+的浓度,并将结果导出到Excel表格中。该软件能够完成从原始信号到重金属浓度的全过程分析,为后续的土壤重金属检测提供了便捷的工具。
-
为了进一步验证所提方法的实用性,选取4份真实土壤样品进行浸提,开展加标实验。采集样品的溶出伏安信号,利用所设计的信号处理与分析软件对采集到的原始信号进行处理,完成重金属种类识别和特征信号提取,并调用内嵌的SVR模型对重金属浓度进行检测。分别检测样品加标前后的重金属离子浓度,计算出Cu2+、Zn2+、Cd2+、Pb2+的加标回收率。
如表 3所示,所设计的软件不仅能够准确地识别目标重金属的种类,还能较为准确地检测重金属的浓度,4种重金属的加标回收率均在70%~110%范围内。Cu2+的加标回收率在77.9%~109.8%,平均加标回收率为93.6%;Zn2+的加标回收率在71.7%~102.9%,平均加标回收率为91.9%;Cd2+的加标回收率在70.7%~107.7%,平均加标回收率为86.9%;Pb2+的加标回收率在70.2%~101.1%,平均加标回收率为90.2%。上述结果表明,提出的方法具有良好的实用性,可以用于检测土壤重金属的含量。
2.1. 优化参数结果
2.2. 重金属灵敏度和检测限分析
2.3. 重金属间干扰分析
2.4. 不同模型性能对比
2.5. 重金属溶出伏安信号处理与浓度分析软件设计
2.6. 实际土壤样品验证
-
提出了机器学习辅助电化学溶出伏安检测方法,有效抑制了多种重金属交互干扰的影响,实现了Cu2+、Zn2+、Cd2+、Pb2+ 4种重金属的同步准确检测。主要结论如下:
1) 确定了最优的实验参数(Bi3+浓度、沉积电压、沉积时间),对单一重金属离子的检测限分别为:Cu2+ 1.79 μg/L、Zn2+ 4.70 μg/L、Cd2+ 0.17 μg/L、Pb2+ 0.16 μg/L。
2) 开展了重金属交互干扰实验,证明了多种重金属之间存在显著的非线性干扰,导致传统的ULR模型失效。
3) 建立了机器学习检测模型,相较于ULR模型,将Cu2+、Zn2+、Cd2+、Pb2+ 4种重金属的Rv2分别从0.468提高到0.966、-9.700提高到0.929、-0.782提高到0.932、0.088提高到0.944;4种重金属的rRMSEv均降低至21%以下。
4) 开展了真实样品的实验验证,所提出的方法对Cu2+、Zn2+、Cd2+、Pb2+ 4种重金属的平均加标回收率分别为93.6%、91.9%、86.9%、90.2%,证明了该方法的实用性。
结果表明,机器学习可以克服复杂土壤基体的影响,有效提升电化学溶出伏安法对重金属的检测准确性,为土壤中多种重金属的同步、快速、准确检测提供了有力支持。



 下载:
下载: