-
开放科学(资源服务)标识码(OSID):

-
我国是世界重要的柑橘种植地区之一,拥有丰富的柑橘种质资源。柑橘溃疡病是由柑橘黄单胞菌柑橘亚种(Xanthomonas citri pv. citri,Xcc)引起的一种细菌性检疫病害,在中国、美国、澳大利亚和巴基斯坦等柑橘主产区均有报道,并造成严重的经济损失[1-5]。目前,柑橘溃疡病的主要防控措施包括检验检疫、选育和推广抗病品种、加强田间管理以及施用含铜化学药剂,其中含铜制剂被认为是防治柑橘溃疡病最为有效的化学手段[6-8]。然而,化学药剂的长期使用不仅存在环境污染和安全隐患,也不符合当前农业绿色防控的发展方向。近年来,生物防治被认为是替代化学防治的最具潜力的方法之一,越来越多的益生菌被研究并应用于植物病害防控[9]。用于防治柑橘溃疡病的有益微生物来源广泛,包括柑橘自身、土壤及其他植物等,其作用机制多样(如拮抗作用、营养竞争以及诱导植物防御反应等[7, 10])。深入解析益生菌的作用机制,有助于优化生物防治策略,并为阐明生防微生物、病原菌与寄主植物之间的互作关系提供理论支持,从而改进其应用方式和施用效果,维护柑橘产业的健康与可持续发展。本文围绕影响柑橘溃疡病发生的因素、生防微生物的种类及其作用机制,以及柑橘溃疡病生物防治面临的问题与挑战进行综述,旨在总结该领域的研究进展与发展趋势,为后续深入研究提供参考。
全文HTML
-
植物病害的发生是一个复杂的过程,涉及病原体、寄主植物、环境条件及人类活动等多种因素的相互作用。柑橘溃疡病的发生与流行不仅直接影响果实产量和品质,还对柑橘产业造成巨大经济损失。其发生与流行程度主要取决于病原菌的种群密度、柑橘品种的抗病性、气候环境条件以及生态系统状态等因素。
-
柑橘溃疡病菌(Xanthomonas citri pv. citri)是柑橘溃疡病发生的必要条件,病原菌主要通过雨水飞溅和风力进行短距离传播,而人为活动则是其远距离传播和区域扩散的重要因素[11]。柑橘溃疡病的病残体是病原菌的重要来源。研究表明,柑橘溃疡病菌的最适生长温度为20~30 ℃,在5~40 ℃均可存活和生长[12]。Hameed等[13]的研究发现,温度27~37 ℃、相对湿度55%、降雨量4.7~7.1 mm以及风速8 km/h等条件有利于柑橘溃疡病的发生。此外,柑橘叶部害虫取食造成的伤口可显著促进病原菌侵染,加剧病害发生。7~9月有效控制柑橘潜叶蛾的发生,可显著降低柑橘溃疡病的危害程度[7, 14-19]。
-
不同柑橘品种对柑橘溃疡病的抗性存在显著差异。香橙、金橘等品种抗性相对较强,而脐橙、柠檬和血橙等品种则较为易感[1, 20-21]。研究表明,幼龄柑橘树由于抽梢频繁、叶片组织幼嫩,更易受到柑橘黄单胞菌的侵染[1, 6, 22];人工接种试验也表明,柑橘溃疡病可贯穿果实整个发育周期,其中幼果期对病原菌最为敏感[23]。
-
植物微生物组的稳定性对维持植物健康具有重要意义。植物微生物群落在激活植物免疫系统、抑制病原菌侵染、促进养分吸收以及提高植物生长和产量等方面发挥着关键作用[24-26]。稳定的微生物群落具有较强的抗干扰能力,有助于植物抵御病害侵染[27-28]。研究表明,通过微生物网络分析可筛选出在植物生长、抗病和耐逆过程中发挥关键作用的核心微生物[29]。目前的研究发现,柑橘根际微生物群落中假单胞菌属(Pseudomonas)、农杆菌属(Agrobacterium)、根瘤菌属(Rhizobium)和伯克霍尔德菌属(Burkholderia)等是重要的核心成员,在不同条件下可抑制柑橘病害的发生[25, 30]。Huang等[31]在研究柑橘溃疡病叶际微生物群落时发现,内生微生物中肠杆菌属(Enterobacter)、假单胞菌属和泛菌属(Pantoea)与病原菌之间的竞争作用显著增强。在叶表微生物群落中,寡养单胞菌属(Stenotrophomonas)、假单胞菌属和鞘氨醇单胞菌属(Sphingomonas)的丰度与黄单胞菌属(Xanthomonas)呈正相关,可能在病害发生中发挥协同或伴生作用,而不动杆菌属(Acinetobacter)则与黄单胞菌属呈负相关[32]。此外,多项研究表明,不同来源的生防微生物在防治柑橘溃疡病方面具有良好潜力,例如,来自柑橘叶片的铜绿假单胞菌(Pseudomonas aeruginosa LV)和解淀粉芽孢杆菌(Bacillus amyloliquefaciens QC-Y),以及来自土壤的假单胞菌(Pseudomonas sp. SJ01)和链霉菌(Streptomyces sp. A16)等[33-35]。
上述因素既是柑橘溃疡病发生的重要驱动因素,也是制定防控策略时必须重点考虑的因素,直接影响防治效果。植物病害防控的本质在于通过改变病害发生条件,打破病原菌、寄主植物和环境之间的“病害三角”关系,从而实现有效防控。因此,柑橘溃疡病发生因素同样会制约生防微生物的防治效果。
1.1. 环境因子
1.2. 柑橘品种及生育期
1.3. 柑橘微生物的变化
-
在减少化学药剂使用、推动绿色防控的背景下,开发和应用高效、安全的生物防治策略已成为植物病害管理的重要发展方向。以细菌和真菌为代表的新型微生物制剂,在植物病害的可持续治理中发挥着越来越重要的作用[36-37]。目前的大量研究表明,细菌、真菌及噬菌体等多种微生物均可对柑橘溃疡病产生显著的防控效果。已有报道的柑橘溃疡病生防微生物种类及其相关信息汇总见表 1。
-
研究表明,芽孢杆菌属(Bacillus)、假单胞菌属(Pseudomonas)、肠杆菌属(Enterobacter)和链霉菌属(Streptomyces)等多种细菌类群中的特定菌株,对植物真菌性和细菌性病原具有显著抑制活性[81]。其中,芽孢杆菌属、假单胞菌属和链霉菌属是目前研究较多、在柑橘溃疡病防治中应用潜力最大的生防微生物菌属[10]。
-
芽孢杆菌分布广泛,生理特性稳定,能够形成耐逆性的内生孢子以适应不良环境条件,是柑橘溃疡病生物防治中最具应用潜力的菌属之一。Rabbee等[49-50]从不同柑橘品种的内生微生物中筛选获得21株芽孢杆菌,其中Bacillus velezensis EB-39对病原菌表现出最强的拮抗活性,其田间应用可使柑橘溃疡病发病率降低38%。此外,来源于其他植物的枯草芽孢杆菌(Bacillus subtilis LE24)、解淀粉芽孢杆菌(Bacillus amyloliquefaciens LE109)和苏云金芽孢杆菌(Bacillus thuringiensis TbL-22)等,其发酵液中均含有抑菌活性物质。其中,苏云金芽孢杆菌TbL-22处理后可使叶片发病率降低64.05%[38-39]。此外,多项研究表明,Bacillus subtilis CQBS03、GN222和J1等菌株对柑橘溃疡病均具有显著的防治效果[41-42, 44, 46]。
-
假单胞菌属在植物体内和土壤环境中普遍存在,具有生长繁殖快、代谢类型丰富、可产生多种生物活性物质等特点,在植物病害生物防治中具有重要作用。Michavila等[53]从柠檬叶片中分离筛选得到的Pseudomonas protegens CS1,不仅能够显著抑制病原菌生长,还可在叶片表面和组织内稳定定殖。Villamizar等[55]研究发现,Pseudomonas entomophila JS2对柑橘溃疡病菌具有显著拮抗活性。Yang等[82]报道,来源于水稻土壤的Pseudomonas mosselii 923对柑橘黄单胞菌表现出明显的抑制作用,显示出良好的应用前景。
-
除芽孢杆菌属和假单胞菌属外,伯克霍尔德菌属(Burkholderia)和链霉菌属(Streptomyces)等细菌也被证实可有效防治柑橘溃疡病。Riera等[57]和谭小艳等[68]研究发现,来源于柑橘叶片的Burkholderia territorii A63、Burkholderia metallica A53和Burkholderia cepacia在平板对峙试验中均能显著抑制病原菌生长。链霉菌能够产生多种具有生物活性的次生代谢产物,在体外条件下可有效抑制多种植物病原菌,并在多种作物病害防控中表现出良好效果。董玉兰等[56]研究表明,链霉菌CLT3对柑橘溃疡病菌的抑制率较高,其田间防效可达83.85%。此外,从土壤中分离得到的Streptomyces sp. A16、Streptomyces sp. GLL-9、Actinomycetales bacterium CYZ2-6和Streptomyces griseochromogenes YCD1-7-1等菌株,对柑橘溃疡病菌亦表现出良好的拮抗活性[35, 61, 63]。
-
真菌在自然生态系统中分布广泛,种类丰富,但用于柑橘溃疡病防治的研究相对较少。生防真菌主要通过产生具有抑菌活性的次生代谢物来抑制病原菌生长。颜桢灵等[83]对来源于健康柑橘植株的72株内生真菌发酵产物进行筛选,发现其中29株真菌的乙酸乙酯提取物对病原菌具有显著抑制作用。Lin等[84]研究表明,脐橙内生真菌Diaporthe sp. HT-79的粗发酵产物对柑橘溃疡病菌具有明显的抑制效果。Nugroho等[71]发现,来源于南极土壤和海洋沉积物的真菌,如Paraconiothyrium、Cadophora、Toxicocladosporium、Penicillium和Pseudogymnoascus等,对柑橘溃疡病菌亦表现出较强抑制能力。尽管生防真菌资源丰富,但目前可实际应用于柑橘溃疡病防治的种类仍然有限,其潜力尚有待进一步挖掘。
-
噬菌体是一类能够特异性感染并裂解细菌的病毒,具有体积小、宿主特异性强等特点。生防噬菌体可通过裂解病原菌或降低其致病力来实现病害防控。Ali等[78]研究发现,来源于土壤的丝状噬菌体XacF1可通过与柑橘黄单胞菌基因组发生重组,改变宿主菌的生理特性,从而显著降低其致病力。研究还表明,噬菌体Bacteriophages Cp1和Bacteriophages Cp2可识别病原菌不同的表面受体并对其进行裂解,进而降低柑橘溃疡病的发生程度[79]。从污水中分离得到的噬菌体Xac-P9具有较好的稳定性,在处理30 min后对宿主菌的裂解率可达90%,处理150 min后可实现完全杀灭,显示出良好的应用潜力[80]。尽管现有噬菌体对柑橘黄单胞菌具有较好的抑制效果,但其在柑橘溃疡病防控中的实际应用仍较少,相关资源和技术体系仍有待进一步完善。
2.1. 生防细菌
2.1.1. 芽孢杆菌
2.1.2. 假单胞菌
2.1.3. 其他生防细菌
2.2. 生防真菌
2.3. 生防噬菌体
-
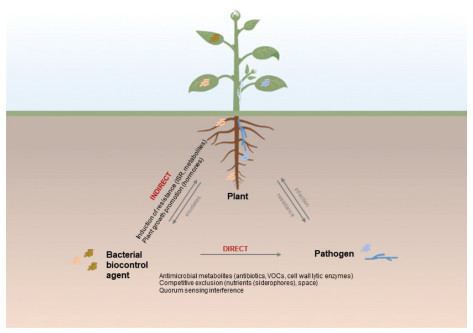
柑橘溃疡病生防微生物的作用机制主要可归纳为以下3类:通过产生抑菌活性物质直接抑制或杀灭病原菌;诱导植物系统抗性,提高寄主整体抗病能力;干扰病原菌群体感应系统或影响其基因组结构,从而削弱致病力。
-
生防微生物可通过分泌多种抗菌化合物直接作用于病原菌,抑制其生长或破坏其细胞结构。Rabbee等[49]利用扫描电镜观察发现,Bacillus velezensis EB-39的乙酸乙酯提取物处理后,病原菌细胞膜出现明显破损或溶解,病原菌数量显著减少。Wang等[48]研究表明,Bacillus amyloliquefaciens F9分泌的脂肽类物质(如Fengycin、Surfactin和Iturin)能够抑制病原菌胞外酶的产生,并诱导细胞壁裂解,从而减轻病害发生。研究还发现,Pseudomonas mosselii 923通过产生pseudoiodinine有效抑制病原菌生长。Pseudomonas aeruginosa LV产生的次生代谢物同样表现出较强的抗菌活性[34]。此外,Michavila等[53]报道,Pseudomonas protegens CS1发酵产物中含有绿脓杆菌螯铁蛋白对映体,可诱导活性氧积累并造成氧化胁迫,从而抑制病原菌生长。Vieira等[73]发现,Penicillium sp. CRM 1540产生的青霉酸在25 μg/mL条件下对病原菌的体外抑制率可达90%。深海真菌Aspergillus terreus SCSIO 41202产生的代谢物对Xcc亦具有显著拮抗作用[75]。
-
生防微生物可通过诱导植物免疫反应,提高寄主对病原菌的防御能力。赖家豪等[42]研究发现,Bacillus sp. GN222、Kosakonia cowanii GN223和Bacillus subtilis GN232可显著提高脐橙防御相关酶活性,从而增强其对柑橘溃疡病的抗性。Riera等[57]发现,在病原菌侵染的叶片中Pseudomonas geniculata 95诱导激活了水杨酸信号途径标记基因水杨酸羧甲基转移酶Ⅰ和SAM-SACM的表达,激活植物免疫系统并显著缓解病害症状。Xie等[74]研究表明,接种丛枝菌根真菌可通过促进防御信号分子积累和病原防御基因表达,提高柑橘对Xcc侵染的抗性。
-
部分生防菌还可通过干扰病原菌的群体感应系统,或通过竞争营养和生态位降低病原菌的定殖能力。Caicedo等[85]发现,Bacillus sp. SJ13、Pseudomonas sp. SJ02和Pseudomonas sp. SJ01均可有效减轻柑橘溃疡病症状。其中,Pseudomonas sp. SJ02可通过降解病原菌扩散性信号分子,阻断其群体感应过程,抑制生物膜形成。Ye等[72]报道的新型信号分子降解菌Acinetobacter lactucae QL-1,可通过群体淬灭效应显著降低病原菌致病力。研究结果表明,破坏柑橘黄单胞菌的群体感应并抑制其生物膜形成是有效防治柑橘溃疡病的重要策略。Ali等[78]研究发现,来自土壤的丝状噬菌体XacF1通过将其自身基因组与柑橘黄单胞菌基因组重组,显著降低了柑橘黄单胞菌的生理活性和毒力,导致其丧失致病性。
3.1. 生防微生物产生抑菌活性物质
3.2. 生防微生物诱导激活植物免疫
3.3. 其他作用
-
目前,柑橘溃疡病的防控仍是以铜制剂为主的化学防治措施为主。本文系统综述了影响柑橘溃疡病发生的主要因素,总结了生防微生物防治柑橘溃疡病的研究进展及其作用机制。柑橘溃疡病的有效防控需要将预测预报、检验检疫、田间管理和病害防治等措施进行综合应用。加强田间管理、有效控制柑橘潜叶蛾发生,可显著降低溃疡病暴发风险。已有研究表明,在夏末秋梢期,柑橘潜叶蛾取食造成的大量伤口是诱发溃疡病流行的重要因素[53-60]。同时,多项研究显示,部分生防微生物的防效可优于传统化学药剂。例如,Diaporthe sp. HT-79产生的亚油酸在7.8 mg/L条件下可破坏病原菌细胞结构[84];噬菌体Xac-P9在与病原菌共培养150 min后可实现完全裂解[80];Streptomyces sp. GLL-9产生的放线菌素X2在田间防效上优于铜制剂[63]。尽管如此,生防微生物在实际推广应用中仍面临诸多挑战。
-
尽管关于柑橘溃疡病生防微生物的研究不断增加,但目前市场上可供应用的微生物制剂种类仍然有限,尚难以成为主流防控手段。其主要原因包括:生防微生物资源尚未充分挖掘;部分生防菌作用机制尚不完全明确,限制了其定向优化和高效利用;微生物制剂防效易受环境条件影响,田间效果稳定性不足;以及微生物制剂在规模化生产、储存和运输过程中仍存在技术瓶颈。这些问题在一定程度上制约了生防微生物在柑橘溃疡病防控中的推广应用。
-
柑橘溃疡病的微生物防治是一个涉及多因素、多层级的复杂过程。未来研究应重点关注以下几个方向:深入解析柑橘黄单胞菌侵染、定殖及致病的分子机制,为生物防治提供更多潜在靶点;创新生防微生物资源挖掘策略,通过多生态位采样,结合16S测序和基因组学技术,高效筛选具有应用潜力的益生菌资源;系统阐明生防菌的作用机制和环境适应性,重点关注其在田间条件下的定殖能力和防效稳定性;根据不同果园生态条件,探索生防微生物的最佳施用方式、剂量和时期,将其科学融入现有果园管理体系中,以提升整体防控效果。
总体而言,有益微生物在柑橘溃疡病防控中具有广阔应用前景。未来,其应用模式有望从单一抑制病原菌向调控植株整体健康和微生态平衡转变,通过优化柑橘微生物群落结构、增强植株长势,从而实现柑橘溃疡病的长期、稳定和绿色防控,为柑橘产业的可持续发展提供有力支撑。



 下载:
下载: