-
羟醛缩合反应又称aldol反应,是含有α-氢原子的醛酮化合物参与的一类重要有机化学反应,该反应也是有机化学实验课教学的重要内容之一[1-2]. 在有机制备实验教材中安排的羟醛缩合反应的内容,如两分子丁醛间的缩合反应[3]、苯甲醛与丙酮的缩合反应[3]以及苯甲醛与苯乙酮的缩合反应[3-4],均是以氢氧化钠作为碱以促进烯醇负离子的形成. 但由于氢氧化钠的碱性过强,生成的β-羟基醛酮化合物将进一步脱水,最终得到共轭的α,β-不饱和醛或α,β-不饱和酮. 这就容易给学生造成两点误解:①认为羟醛缩合反应是两分子羰基化合物加成形成β-羟基羰基化合物后,再脱水形成α,β-不饱和羰基化合物的反应[5-6];②认为β-羟基羰基化合物难以稳定存在,总是会脱水形成α,β-不饱和醛酮. 但事实上,根据反应底物或产物结构的不同,羰基化合物间的反应被冠以了不同的名称,例如芳香醛与含α-H的醛、酮缩合制备α,β-不饱和醛酮的反应被称为克莱森-施密特缩合反应(Claisen-Schmidt反应). 同时,β-羟基羰基化合物也是一类稳定的化合物,已有许多关于其合成的报道. 如2000年,List等人[7]报道了脯氨酸催化的不对称羟醛缩合反应;2008年,张浩等[8]报道了联二萘酚双锂盐催化的羟醛缩合反应;2004年,Wang等[9]报道了在催化量Na2CO3存在下α-甲基酮与芳香醛的羟醛缩合反应.
基础有机化学实验是有机化学教学的重要组成部分,对于学生加深对有机化学基本原理的理解,熟悉有机化合物性质,掌握有机化学实验操作技能,培养动手能力、科研能力和创新能力等方面起着重要作用[10-11]. 同时,本科有机制备实验还需满足操作安全、避免使用高毒和强腐蚀性试剂,可操作性强、成功率高等要求.
结合文献[9]报道,本研究设计了一个交叉羟醛缩合反应合成β-羟基酮的实验,以苯乙酮和对硝基苯甲醛为原料,以水作为溶剂,在碳酸铯存在的条件下制备3-羟基-3-(4-硝基苯基)-1-苯基-1-丙酮. 本研究设计的实验中涉及薄层色谱监测反应和抽滤等基本操作,利于学生进一步掌握和熟练运用这些基本技能.
全文HTML
-
掌握羟醛缩合反应的反应机理,学习β-羟基醛酮的合成方法;学习薄层色谱监测反应进程和抽滤等基本操作.
-
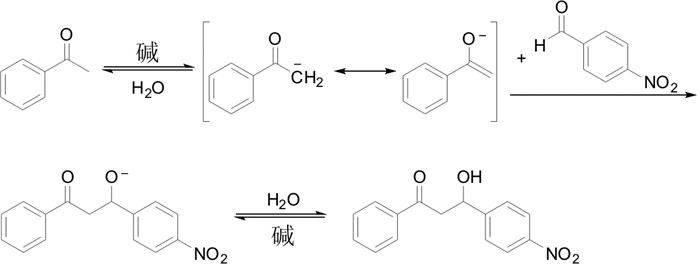
苯乙酮与对硝基苯甲醛的交叉羟醛缩合反应方程式为
其具体的反应机理见图 1.
-
仪器:电子天平,集热式恒温磁力搅拌浴,循环水式多用真空泵,布氏漏斗及抽滤瓶,圆底烧瓶等.
试剂:苯乙酮(重庆川东化工);对硝基苯甲醛(安耐吉化学);碳酸铯(阿达玛斯试剂);碳酸氢钠(重庆川东化工);碳酸钠(重庆川东化工);碳酸钾(重庆川东化工);磷酸钾(阿达玛斯试剂);实验中所用试剂均为分析纯.
-
在100 mL圆底烧瓶中加入苯乙酮(0.62 mL),对硝基苯甲醛(755 mg)和水(30 mL),室温下剧烈搅拌数分钟,以形成足够的浊度和良好的分散度. 然后加入碳酸铯(1.63 g),在50 ℃下继续反应,并通过薄层色谱监测反应,随着反应的进行,将析出大量白色固体,由油水两相体系变为固液两相体系. 反应完成后(约2 h),将反应液冷却至室温,用布氏漏斗抽滤,固体用水洗涤(20 mL×3),干燥后得白色至米黄色粉末,称质量并计算产率(经3次实验,其收率的平均值为97%). 以氘代氯仿作为溶剂,用Bruker-600核磁共振仪进行核磁共振分析:1H NMR (600 MHz,CDCl3) δ 8.23 (d,J=8.6 Hz,2H),7.95 (d,J=7.4 Hz,2H),7.61 (t,J=8.4 Hz,3H),7.48 (t,J=7.8 Hz,2H),5.46 (dt,J=8.7,2.7 Hz,1H),3.86 (d,J=3.0 Hz,1H),3.38 (qd,J=17.8,6.0 Hz,2H);13C NMR (150 MHz,CDCl3) δ 199.47,150.26,147.42,136.26,133.99,128.83,128.16,126.57,123.79,69.25,46.98.
1.1. 实验目的
1.2. 实验原理
1.3. 仪器与试剂
1.4. 实验方法
-
按照1.4的实验方法,首先考察了不同的无机碱对反应的影响(表 1).
由表 1可见,以碳酸钾和碳酸铯作为碱时反应效果较好,能够分别获得96%和97%的产率. 当使用碱性较弱的碳酸氢钠时,反应22 h原料的转化率也只有30%;使用碳酸钠反应时间也较长,需要6 h才能反应完全. 以磷酸钾作碱能够在2 h完成反应,但监测到较多的脱水产物α,β-不饱和酮的产生,且所得产物的颜色较深. 最终,选择以碳酸铯作为碱,进行后续的条件筛选.
-
考察了碳酸铯用量对反应的影响,实验结果见表 2. 随着碳酸铯用量的减少收率略有降低. 最终,决定碳酸铯的用量为5.0 mmol.
-
考察了温度对反应的影响,实验结果见表 3. 根据实验结果,可以看出温度对反应有较大的影响,发现随着反应温度的降低,反应时间需要相应延长;而随着反应温度的升高,脱水副产物的量会逐渐增加. 如当反应温度为30 ℃时,反应时间需要延长到8 h;而当反应温度升高到70 ℃时,原料能够在1.5 h内转化完全,但通过TLC监测发现,主要生成的是脱水产物α,β-不饱和酮. 因此,温度的准确控制是实验成功的关键.
-
探究了溶剂水的用量和反应物比例对反应的影响,实验结果见表 4. 当使用10 mL的水作为溶剂时,产物析出困难且产物颜色较深,同时有脱水副产物的生成导致产率降低明显. 随着溶剂用量的增加,脱水产物随之消失,所得产物成白色. 当溶剂用量为20~30 mL时,获得最高的产率. 当将苯乙酮的用量由5.3 mmol改为5.0 mmol时,产物的收率有所降低,因此决定苯乙酮的用量依然为5.3 mmol.
通过反应条件的系统优化,确定了最佳的反应条件:当对硝基苯甲醛用量为5.0 mmol时,苯乙酮的用量为5.3 mmol,碳酸铯用量为5.0 mmol,溶剂用量为20~30 mL,并在50 ℃下反应2 h.
2.1. 碱对反应结果的影响
2.2. 碳酸铯用量对反应结果的影响
2.3. 温度对反应结果的影响
2.4. 溶剂用量及反应物比例对反应结果的影响
-
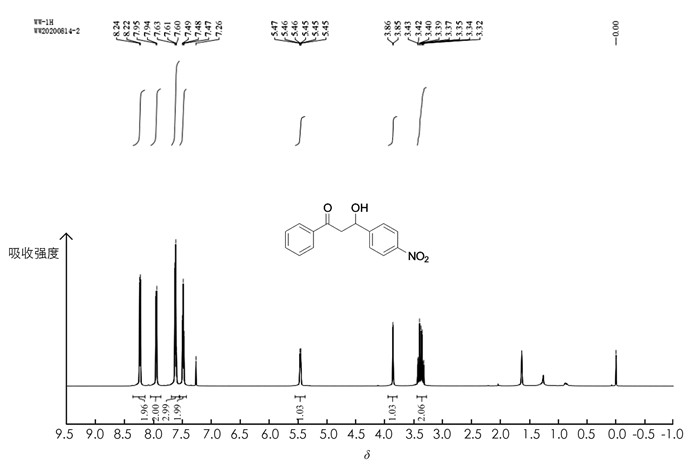
本研究对苯乙酮和对硝基苯甲醛制备β-羟基酮的反应条件进行了系统优化,其产物的1H NMR谱图见图 2. 整个实验过程约需要3 h,实验方案条件温和、绿色环保、可操作性强、实验现象明显、成功率高,适合作为本科有机制备课程的实验教学内容.



 下载:
下载: