-
开放科学(资源服务)标识码(OSID):

-
枇杷是一种传统中药材,富含黄酮类、三萜酸类、多酚类等多种药用活性成分。以枇杷为主要原料的中成药(如川贝枇杷胶囊[1]、半夏枇杷糖浆[2]、强力枇杷露[3]、川贝枇杷膏[4]等)具有改善气道炎症性水肿、扩张支气管、改善呼吸不畅等作用,常被用于缓解肺气肿。枇杷核作为枇杷的种子,富含苦杏仁苷、总黄酮、挥发油、三萜酸、多酚等活性成分,其中,苦杏仁苷是多种蔷薇科类中药材种子部位(杏仁、桃仁等)的重要药效成分,并且在枇杷核中含量远高于其他成分,约为2.11%[5-6]。枇杷核常作为枇杷果肉的加工产物被废弃,因此,开发利用枇杷核中的活性成分有着很高的经济和药用价值。
苦杏仁苷是广泛存在于蔷薇科植物果仁(杏仁、桃仁、枇杷核等)中的一种氰苷类化合物,有着抗癌、抗炎、抗氧化应激、抗器官纤维化[7]、促血管修复[8]、免疫调节等药理作用[9-10]。目前苦杏仁苷入药的多种复方中药材被用于缓解肺气肿,例如麦杏补肺汤[11]、厚朴麻黄汤[12]、清肺化痰汤[13]、杏苏止咳颗粒[14]等,具有降气化痰、清肺止咳等功效,能够改善患者咳嗽、咳痰、喘息、胸闷、乏力等症状,证明含有苦杏仁苷的中药复方对肺气肿有着潜在的疗效,但具体作用机制尚不清晰。本研究采用网络药理学和分子对接手段,针对枇杷核中6种代表性组分治疗肺气肿的可能靶点进行预测,最终聚焦于苦杏仁苷,通过超声辅助提取枇杷核中的苦杏仁苷并完成含量测定,再通过体外实验验证,阐明苦杏仁苷干预肺气肿的作用机制,为枇杷核药用资源的开发利用提供可能的方向。
全文HTML
-
分别对枇杷核中的代表成分苦杏仁苷、槲皮素、山奈酚、熊果酸、绿原酸、阿魏酸进行靶点预测。通过PubChem数据库获取2D结构文件,并采用SwissTargetPrediction、PharmMapper、SuperPred数据库进行预测,将结果以Probability大于0和Norm Fit超过中位数作为条件进行筛选,经整合去重后得到药物靶点;以“Emphysema”为关键词,在CTD、GeneCards数据库中搜集与肺气肿相关的疾病靶点。GeneCards数据库结果去除重复值和无UniProt ID的项目,并以Relevance Score超过中位数作为筛选条件;CTD数据库以Inference Score超过40为筛选条件,将结果整合去重后得到肺气肿的预测靶点。相关网站及数据库如表 1。
-
将预测得到的苦杏仁苷和肺气肿的交集靶点上传至STRING数据库中,将目标生物类别设置为“智人(Homo Sapiens)”,置信度设置为“high confidence(0.700)”,输出结果后导入Cytoscape 3.7.1软件中,通过Cyto NCA插件对结果进行拓扑学分析,计算节点度,构建交集靶点的蛋白互作网络图,并以节点度由大到小进行排序,得到前20个核心靶点。
-
采用DAVID数据库完成GO和KEGG富集分析,并通过微生信在线作图平台绘制GO和KEGG富集分析柱状图和气泡图。
-
使用分子对接模拟苦杏仁苷与核心靶点之间的潜在关系,首先从AlphaFold数据库中获得靶点蛋白的3D结构文件,再从PubChem数据库中获得苦杏仁苷的3D结构文件,通过Open Babel GUI软件对格式进行转换后,导入AutoDockTools 1.5.7中,分别进行去水、加氢、检查扭转键等操作后,通过vina插件进行全分子对接,将对接结果导入PyMOL 2.2.0软件进行可视化分析。
-
电子天平,梅特勒—托利多;超净工作台,苏州净化设备有限公司;电泳及转膜装置、qPCR仪,Bio-rad;荧光倒置显微镜,奥林巴斯;酶标仪,Molecular Devices;高速低温离心机、细胞恒温培养箱、微量分光光度计,Thermo;PVDF膜,Millipore;苦杏仁苷,源叶;SC79(AKT激活剂)、Hoechst 3258、活性氧检测试剂盒、RIPA变性裂解液,碧云天;PMSF,Solarbio;DMSO,MP biomedicals;Tween-20,Biosharp;1.5 M Tris-HCl,Solarbio;SDS,Biofroxx;磷酸化蛋白酶抑制剂,Servicebio;Trizol、Evo M-MLV RT Kit with、gDNA Clean Premix Pro Taq HS qPCR Kit,艾科瑞;胎牛血清,Adamas;Ham's F-12k培养基,Gibco等。
-
选择西南大学华白一号枇杷的新鲜种子作为研究对象,去除表皮杂质,粉碎并过100目筛后置于100 ℃灭活酶3 min;再加入4倍体积的正丁烷,脱脂搅拌3 h,室温挥干溶剂;最后置于55 ℃烘箱中干燥30 min得枇杷核粉末。采用超声辅助提取苦杏仁苷:以60%乙醇为提取溶剂,按1∶20料液比进行投料,50 ℃、40 kHz提取45 min,待反应结束,7 000 r/min离心10 min,取上清液,0.22 μm微孔滤膜过滤即为样品溶液,等待上机检测。
-
精密称取10 mg苦杏仁苷标准品,甲醇溶解并定容至10 mL,即为1 mg/mL苦杏仁苷母液,分别稀释至500、250、125、25、5 μg/mL梯度溶液。色谱柱选用C18柱(150 mm×4.6 mm,5 μm),流动相选择20%甲醇溶液等度洗脱,流速设置为1 mL/min,柱压30 mPa,检测波长为208 nm,以x为杏仁苷标准品的质量浓度(mg/mL),y为峰面积绘制标准曲线。按照上述方法测定样品溶液,将峰面积代入标准曲线,计算得到苦杏仁苷的质量浓度(μg/mL)。
-
为了模拟临床肺气肿,本研究采用香烟烟雾提取物刺激肺癌人类肺泡基底上皮细胞(A549)构建肺气肿细胞模型[27]。取50 mL包氏管,左接蠕动泵,右接云烟牌香烟(每支焦油8 mg、烟碱0.8 mg、一氧化碳7 mg,使用前去除滤嘴),内部为20 mL Ham's F-12k完全培养基。点燃香烟,蠕动泵流速调节至30 mL/min,使烟雾通过导管沉降并逐渐溶于培养基中,总共抽吸5支香烟,过程可见培养基溶液颜色由粉色逐渐变为黄色,伴有不溶性碎屑。抽吸完毕,静置30 min,调整pH值为7.2~7.4,经0.22 μm水系微孔滤膜过滤,高效液相色谱法(HPLC)测得提取液中烟碱质量浓度为1 675.29 μg/mL,记为100% CSE,分装后暂存于-20 ℃冰箱中,于1个月内使用完毕。
-
A549细胞由中国科学院细胞库提供。将A549细胞以每孔3 000个铺至96孔板中,加Ham's F-12k 100 μL培养至贴壁后,加入梯度浓度的苦杏仁苷或CSE,分别培养24、48、72 h;培养结束后,每孔加入20 μL MTT试剂,37 ℃孵育4 h,吸出孔内溶液,每孔加入150 μL二甲基亚砜(DMSO),充分振摇10 min使沉淀充分溶解,于490 nm处检测每孔吸光度值(OD),并计算细胞存活率(R存活)。选取抑制细胞50%活力的CSE浓度作为造模浓度,保留细胞80%以上活力的苦杏仁苷浓度作为安全浓度进行后续实验。
式中:OD实验组代表经苦杏仁苷或CSE处理后的培养孔吸光度值;OD对照组代表未经药物处理的培养孔吸光度值;OD调零组代表调零组(Ham's F-12k 100 μL+MTT 20 μL+DMSO 150 μL)吸光度值。
-
将A549细胞铺至6孔板,培养至一定密度后,加入低、高浓度的苦杏仁苷,培养2 h后加入CSE,继续培养至48 h,每孔加入Hoechst33258染色试剂1 mL,于37 ℃培养箱中孵育20 min,弃去培养基,PBS清洗后于荧光显微镜下观察并拍照。
-
将A549细胞铺至6孔板,培养至一定密度后,加入低、高浓度的苦杏仁苷,培养2 h后加入CSE,继续培养至48 h,每孔加入DCFH-DA试剂1 mL,于37 ℃培养箱中孵育20 min,弃去培养基,PBS清洗后于荧光显微镜下观察并拍照。
-
采用Trizol法提取A549细胞的总RNA,去除基因组DNA,并将其反转录为cDNA,设计并合成引物,按照相应体系和程序进行qRT-PCR反应,结果采用2-ΔΔCt法进行分析并作图。
-
总蛋白的提取全程于冰上进行。采用RIPA裂解液混合体系(RIPA裂解液、PMSF、磷酸化蛋白酶抑制剂比例为98∶1∶1)裂解细胞后,离心取上清液,即为总蛋白溶液。采用BCA法对蛋白进行定量后,加入相应比例的Loading Buffer后进行蛋白煮样。通过SDS-PAGE分离蛋白,采用湿转法将蛋白样品转移至PVDF膜上,浸泡于5%脱脂蛋白摇床2 h以封闭非特异性位点,将膜浸泡于一抗中,4 ℃恒温摇床孵育过夜;将膜取出浸泡于对应二抗中,摇床孵育1~2 h后显影,通过Image J分析蛋白条带灰度值。
-
将A549细胞铺至12孔板,培养至一定密度后,分别加入苦杏仁苷、苦杏仁苷联合SC79溶液(AKT激活剂),培养2 h后加入CSE并继续培养24 h;每孔加入1 mL 4%多聚甲醛,室温固定30 min;每孔加入1 mL Triton X-100,室温通透30 min;每孔加入1%BSA,室温封闭1 h;每孔加入150 μL一抗,4 ℃湿盒孵育过夜,回收一抗,避光条件下每孔加入200 μL荧光二抗,孵育1.5 h;每孔加入1 mL DAPI,避光染色5 min,于荧光显微镜下观察拍摄,通过Image J分析荧光强度。
-
结果均为3次以上独立重复实验所得,数据采用SPSS 21.0进行统计分析,GraphPad Prism 9.5作图,单因素方差分析(one-way ANOVA)比较多组间差异,p<0.05表示差异有统计学意义。
1.1. 肺气肿的靶点筛选
1.2. 靶点整合及蛋白互作网络的构建
1.3. GO和KEGG富集分析
1.4. 分子对接
1.5. 实验仪器与耗材
1.6. 枇杷核中苦杏仁苷的提取及含量测定
1.6.1. 苦杏仁苷的提取
1.6.2. 苦杏仁苷含量的测定
1.7. 体外实验方法
1.7.1. 香烟烟雾提取物(CSE)的制备
1.7.2. MTT法检测苦杏仁苷和CSE对A549细胞活性的影响
1.7.3. Hoechst33258染色检测CSE和苦杏仁苷对A549细胞凋亡的影响
1.7.4. DCFH-DA探针检测CSE和苦杏仁苷对A549细胞总活性氧(ROS)水平的影响
1.7.5. 实时荧光定量聚合酶链反应(qRT-PCR)
1.7.6. 蛋白免疫印迹实验(Western Blot,WB)
1.7.7. 免疫荧光染色实验(IF)
1.8. 数据处理与分析
-
为了探究枇杷核中化学成分与肺气肿发生发展之间的可能关联,采用SwissTargetPrediction、PharmMapper、SuperPred数据库,对枇杷核中的苦杏仁苷、槲皮素、山奈酚、熊果酸、绿原酸和阿魏酸共6种主要成分进行靶点预测,取并集后分别得到了250、316、218、282、316、278个活性成分靶点;随后,采用GeneCards、CTD数据库对肺气肿进行靶点预测,经筛选整合得到3 010个肺气肿靶点。
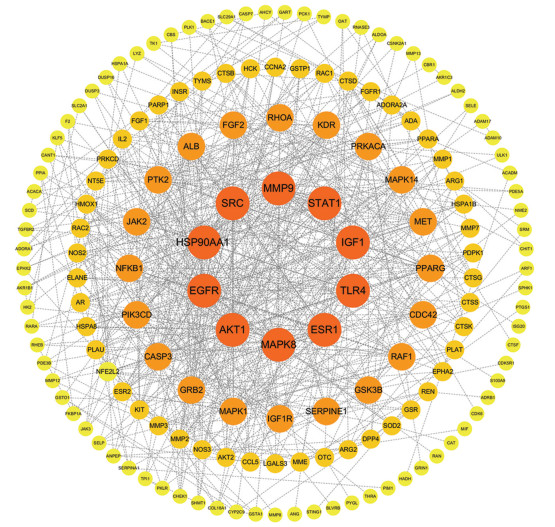
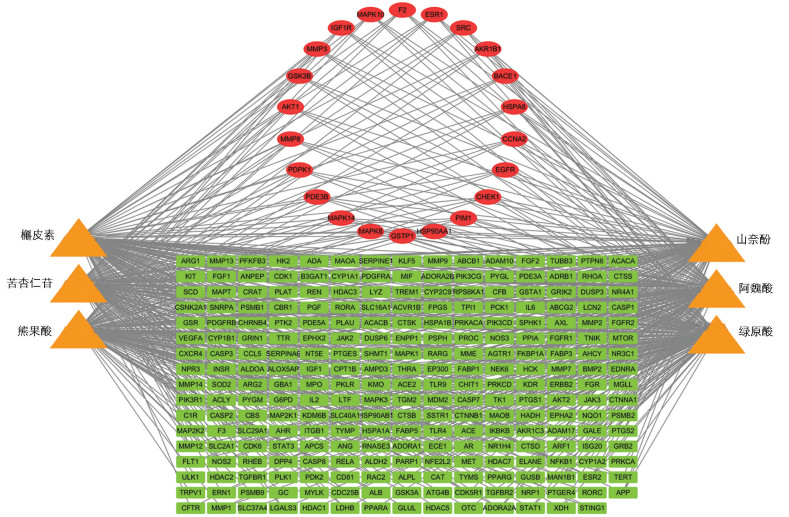
将6种活性成分靶点与肺气肿靶点取交集,共得到181、131、100、119、141、136个交集靶点,并绘制活性成分靶点网络图(图 1),其中,6种活性成分的共同作用靶点有22个,包括GSTP1、HSP90AA1、EGFR、HSPA8、SRC、ESR1、AKT1、MMP8、MAPK14等,涉及EGFR、PI3K/AKT、MAPK等信号通路。考虑到枇杷核中苦杏仁苷的含量远高于其他组分,在开发利用枇杷核过程中价值更高,因此,本研究选择了苦杏仁苷作为后续研究对象。
-
将苦杏仁苷与肺气肿的靶点取交集,共得到181个可能靶点。将结果导入STRING数据库中,选择高置信度(0.700),输出并导入Cytoscape 3.7.1软件,去除独立蛋白,计算靶点节点度并从大到小排序,以红—橙—黄色节点区分优先级,绘制蛋白互作网络图(图 2)。其中,节点度排名前20的蛋白包括AKT1、EGFR、HSP90AA1、SRC、TLR4、ESR1、MAPK8、MAPK1、CASP3、PIK3CD等(表 2),这些蛋白在网络中起枢纽作用,具有成为苦杏仁苷治疗肺气肿核心靶点的潜力。
-
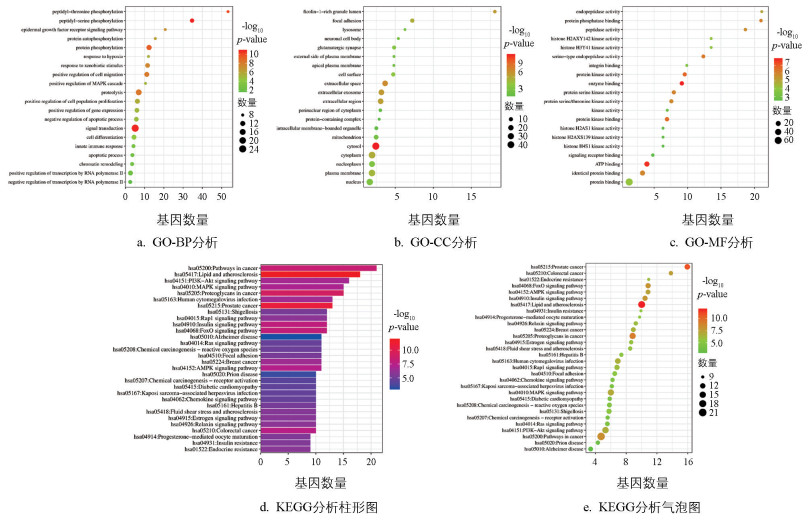
GO和KEGG富集分析结果见图 3。
苦杏仁苷干预肺气肿的生物过程(Biological Process,BP)主要涉及肽基丝氨酸磷酸化(peptidyl-threonine phosphorylation)、蛋白质自磷酸化(protein autophosphorylation)、蛋白水解(proteolysis)、细胞增殖的正向调控(positive regulation of cell population proliferation)、凋亡过程的负调控(negative regulation of apoptotic process)等;细胞组分(Cellular component,CC)包括富含纤维胶凝蛋白-1的颗粒管腔(ficolin-1-rich granule lumen)、黏着斑(focal adhesion)、谷氨酸能突触(glutamatergic synapse)、细胞表面(cell surface)等;分子功能(Molecular function,MF)包括内肽酶活性(endopeptidase activity)、蛋白磷酸酶活性(protein phosphatase binding)、蛋白丝氨酸/苏氨酸激酶活性(protein serine/threonine kinase activity)、信号受体结合(signaling receptor binding)等(图 3a-3c)。KEGG富集分析共富集到了130条信号通路,综合基因数量、显著性和富集程度分析,主要涉及癌症发病途径(Pathways in cancer)、叉头框蛋白O信号通路(FoxO signaling pathway)、脂质与动脉粥样硬化(Lipid and atherosclerosis)、丝裂原活化蛋白激酶信号通路(MAPK signaling pathway)、磷脂酰肌醇3激酶—蛋白激酶B信号通路(PI3K-Akt signaling pathway)、化学致癌—活性氧信号通路(Chemical carcinogenesis-reactive oxygen species)等(图 3d,3e)。以上结果提示,苦杏仁苷可能通过促进蛋白磷酸化、蛋白水解,激活PI3K/AKT信号通路、抑制凋亡信号通路等机制干预肺气肿的发生与发展。
-
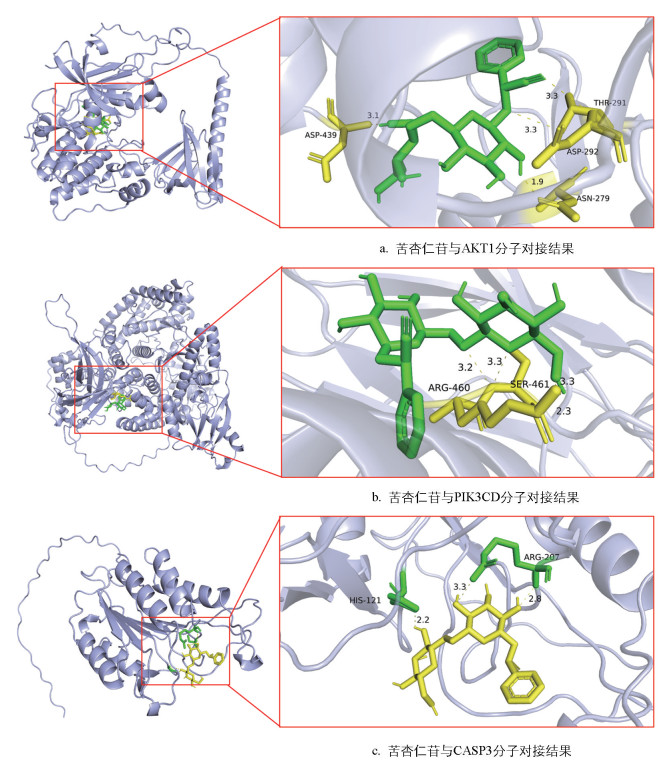
将苦杏仁苷分别与前20个核心靶点进行分子对接,结果如表 3。以对接结合能为判断标准,结合能小于-5 kcal/mol证明结合较稳定,小于-7 kcal/mol证明结合很稳定。GO和KEGG富集分析结果指出,苦杏仁苷对PI3K/AKT和凋亡通路的影响较为突出,并且苦杏仁苷与AKT1、PIK3CD和CASP3的对接结合能均小于-7 kcal/mol(图 4),因此,苦杏仁苷很有可能通过上述靶点及信号通路影响肺气肿的发展。
-
制得苦杏仁苷标准曲线为y=7 433 x+903.2,R2=0.999 1。将样品峰面积代入标准曲线,最终测得枇杷核中苦杏仁苷的提取率为(1.59±0.14)%,如表 4。
-
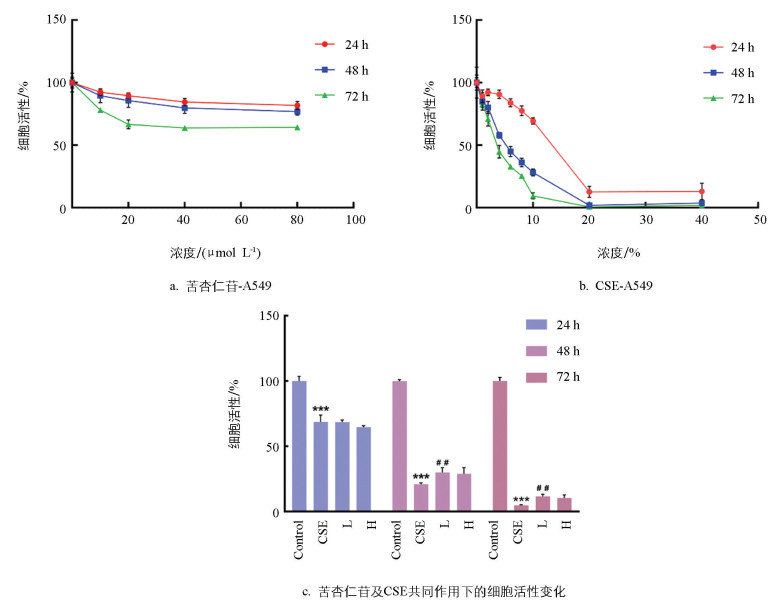
为保证后续实验结果稳定且可控,我们采用市售苦杏仁苷标准品进行活性探究。使用MTT法评估CSE和苦杏仁苷对A549细胞活力的影响。由图 5可知,随着CSE和苦杏仁苷浓度的增大,A549细胞的活性降低;其中,12.09% CSE作用24 h,能够抑制50%的细胞活性,而浓度低于20 μmol/L的苦杏仁苷作用24 h,A549存活率仍大于90%。为兼顾CSE的效用和A549细胞的活性,后续研究采用10% CSE作为刺激浓度;为保证苦杏仁苷的安全性,采用20 μmol/L作为苦杏仁苷的最大给药浓度。
为了进一步观察苦杏仁苷对香烟烟雾提取物引起的细胞活性降低的干预作用,实验分别设置对照组(Control),模型组(10% CSE)、低浓度干预组(10% CSE+10 μmol/L苦杏仁苷,L)和高浓度干预组(10% CSE+20 μmol/L苦杏仁苷,H)。A549细胞经苦杏仁苷预处理2 h,再加入CSE共同作用24、48和72 h,结果如图 5c。相较于对照组,模型组的细胞活性显著降低(p<0.001),苦杏仁苷作用48 h后细胞活性显著上升(p<0.01),提示苦杏仁苷能够减轻CSE对A549细胞的毒性作用。
-
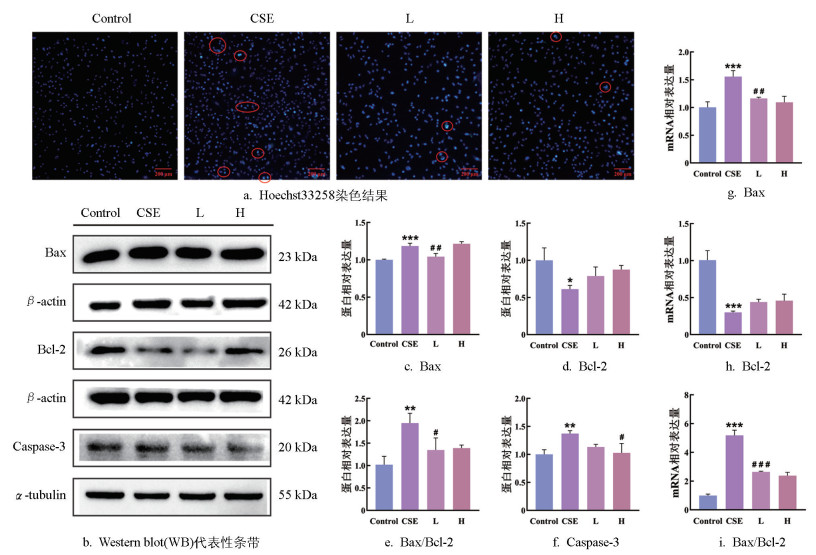
靶点筛选和富集分析结果显示,苦杏仁苷可能通过影响细胞凋亡及相关信号通路干预肺气肿,因此,利用Hoechst33258染色探究苦杏仁苷和CSE对细胞凋亡的影响,结果如图 6。对照组细胞核形态规整,呈现圆形或椭圆形;CSE处理48 h后,A549细胞内出现染色质浓缩、核碎裂等现象,荧光变亮;苦杏仁苷处理48 h后有所减轻,证明苦杏仁苷能够减轻CSE诱导的A549细胞凋亡。
基于Hoechst33258染色结果,进一步采用WB和qRT-PCR实验,探究苦杏仁苷和CSE对凋亡通路的影响。WB结果显示,相较于对照组,模型组的Bcl-2蛋白表达显著降低(p<0.05),Bax(p<0.001)、Caspase-3蛋白(p<0.01)表达和Bax/Bcl-2比值(p<0.01)显著上升;在苦杏仁苷的干预下,Bax蛋白(p<0.01),Caspase-3蛋白(p<0.05)表达和Bax/Bcl-2比值(p<0.05)显著降低(图 6b-6f)。qRT-PCR结果显示,相较于对照组,模型组的Bcl-2转录水平显著降低(p<0.001),而Bax的转录水平和Bax/Bcl-2比值显著上升(p<0.001);苦杏仁苷干预下Bax转录水平(p<0.01)、Bax/Bcl-2比值(p<0.001)显著降低(图 6g-6i)。综合表明,苦杏仁苷能够通过抑制线粒体的凋亡通路,减轻CSE诱导的细胞凋亡。
-
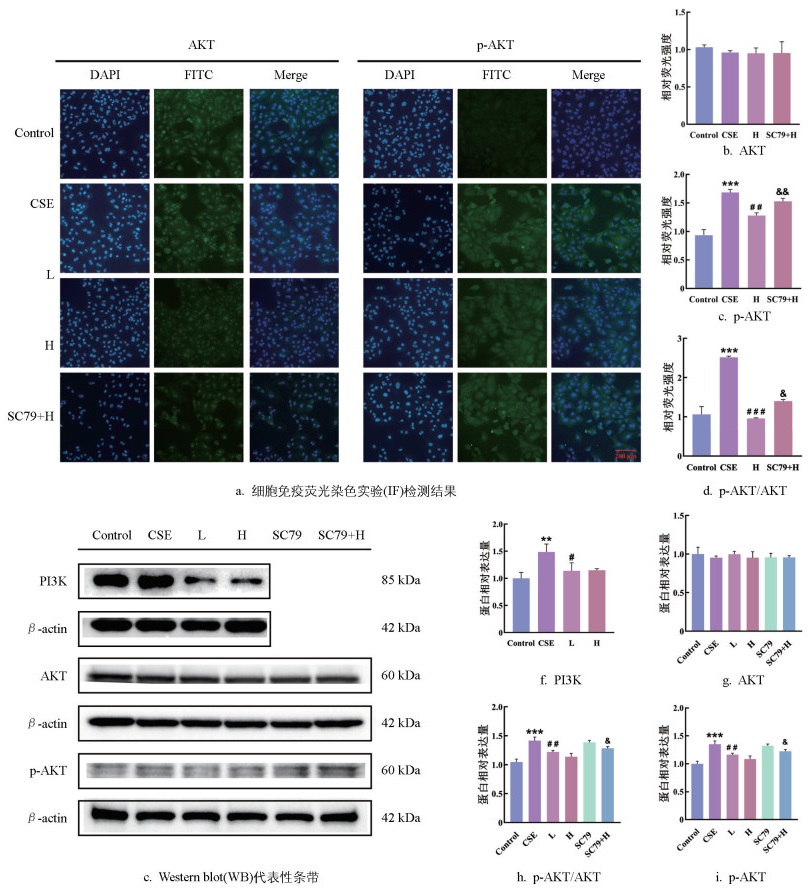
靶点筛选和富集分析结果显示,苦杏仁苷可能通过影响PI3K/AKT信号通路干预肺气肿的发展,因此,可通过WB和IF实验探究苦杏仁苷和CSE对PI3K/AKT信号通路的影响。IF结果显示,相较于对照组,模型组的p-AKT和p-AKT/AKT蛋白表达水平均显著上升(p<0.001),苦杏仁苷干预下显著降低(p<0.01),联用SC79后显著回升(p<0.05)(图 7a-7d)。WB结果显示,相较于对照组,模型组的PI3K(p<0.01)、p-AKT蛋白表达(p<0.001)和p-AKT/AKT比值(p<0.001)均显著升高,而苦杏仁苷干预下显著降低(p<0.05);在此基础上,加入AKT激活剂SC79(SC79+H:10 μmol/L SC79+10% CSE+20 μmol/L苦杏仁苷)则表现出p-AKT蛋白表达和p-AKT/AKT比值显著回升(p<0.05)(图 7e-7i)。综合表明,苦杏仁苷可能通过抑制AKT磷酸化,抑制PI3K/AKT信号通路。
-
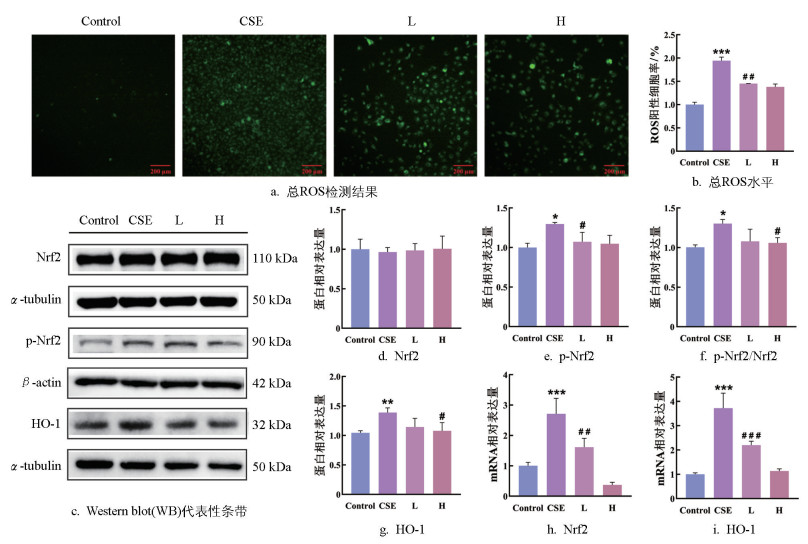
氧化应激是肺气肿的重要发病因素之一,KEGG富集分析结果指出苦杏仁苷可能通过影响ROS水平干预肺气肿,因此,可采用DCFH-DA探针染色检测苦杏仁苷和CSE对细胞总ROS水平的影响,如图 8a和图 8b。相较于对照组,模型组的总ROS水平显著上升(p<0.001),苦杏仁苷治疗下显著降低(p<0.01),证明苦杏仁苷能够降低细胞的总ROS水平,减轻低氧化应激。
Nrf2/HO-1是参与调控氧化应激的关键信号通路,通过WB和qRT-PCR实验探究苦杏仁苷和CSE对Nrf2/HO-1信号通路的影响,如图 8c-8g。相较于对照组,模型组的p-Nrf2(p<0.05)、HO-1蛋白表达(p<0.01)和p-Nrf2/Nrf2比值(p<0.05)显著上升,苦杏仁苷干预下显著降低(p<0.05)。qRT-PCR结果显示,相较于对照组,模型组的Nrf2和HO-1转录水平显著上升(p<0.001),苦杏仁苷干预下表达显著降低(p<0.01)(图 8h、8i)。综合表明,苦杏仁苷可能通过抑制Nrf2/HO-1信号通路的过度激活,减轻CSE诱导的氧化应激。
2.1. 枇杷核活性成分靶点及肺气肿靶点预测
2.2. 蛋白质互作网络(PPI)的构建及核心靶点的筛选
2.3. 交集靶点的GO和KEGG富集分析结果
2.4. 核心靶点分子对接结果
2.5. 枇杷核中苦杏仁苷的提取及含量测定
2.6. MTT法检测香烟烟雾提取物(CSE)和苦杏仁苷对A549细胞增殖活性的影响
2.7. 苦杏仁苷对CSE刺激下A549细胞凋亡的影响
2.8. 苦杏仁苷抑制CSE激活的PI3K/AKT信号通路
2.9. 苦杏仁苷降低CSE刺激下A549细胞的总ROS水平
-
本研究通过网络药理学和分子对接技术对枇杷核中的有效成分进行了初步分析,聚焦苦杏仁苷并探究其干预肺气肿的可能靶点和分子机制。网络药理学结果显示,苦杏仁苷潜在作用靶点包括AKT1、HSP90AA1、CASP3、PIK3CD等,通过分子对接验证苦杏仁苷与核心靶点之间的结合能力,并最终聚焦于AKT1、PIK3CD和CASP3,涉及PI3K/AKT信号通路和线粒体凋亡通路。通过WB、qRT-PCR和免疫荧光等实验,证明CSE刺激下的A549细胞表现出肺气肿中典型的凋亡和氧化应激现象,而苦杏仁苷能够减轻CSE诱导的细胞凋亡和氧化应激,其分子机制可能与抑制AKT磷酸化,影响PI3K/AKT信号通路有关。
网络药理学与分子对接技术是现代药物研发中的重要工具,本研究通过网络药理学,筛选得到苦杏仁苷治疗肺气肿的可能靶点共181个;分子对接结果显示,苦杏仁苷能够与AKT1、CASP3和PIK3CD等核心靶点通过疏水、氢键等方式相互作用,这证明苦杏仁苷可能作为潜在的多靶点药物对肺气肿的发生发展产生了干预作用。本研究通过超声辅助提取枇杷核中苦杏仁苷并完成含量测定,结果显示苦杏仁苷提取率为(1.59±0.14)%。枇杷核来源苦杏仁苷的结构及功效与其他中药来源一致,并且在枇杷核中含量远高于其他成分,具有一定的开发价值。体外研究部分,采用香烟烟雾提取物(CSE)刺激肺癌人类肺泡基底上皮细胞(A549)构建肺气肿细胞模型,该模型表现出显著的氧化应激和凋亡效应,与肺气肿临床发展中的氧化应激和肺组织损伤表现相对应。吸烟是肺气肿最重要的发病因素,香烟烟雾中含有大量的活性氧、活性氮、自由基成分,进入肺部后会直接刺激肺组织产生氧化应激和炎症反应,并削弱肺泡壁弹性纤维功能,加重肺部组织的损伤[28]。PI3K/AKT信号通路与细胞转录、翻译、增殖、存活紧密相关,并参与了肺气肿的发生及发展[29]。AKT是该信号通路的核心枢纽因子,通过自身磷酸化发挥作用,一方面可直接调控下游凋亡通路,加重肺部气道上皮细胞的凋亡和肺组织的实质性损伤,削弱肺部屏障功能[30];另一方面会诱使Nrf2过度激活,抗氧化因子过度表达,加重肺部氧化应激,同时促进炎症因子的表达,加剧肺部炎症反应[31]。炎症与氧化应激、凋亡等机制互相影响,互相促进,加重蛋白酶/抗蛋白酶失衡,进而促进肺泡弹性纤维降解,肺泡弹性降低,呼气困难,促进肺气肿的发展。本研究采用苦杏仁苷干预后,细胞氧化应激和凋亡水平显著减轻,同时PI3K/AKT信号通路被显著抑制,证明苦杏仁苷能够通过抑制AKT磷酸化,干预PI3K/AKT信号通路,同时抑制凋亡和Nrf2/HO-1信号通路,减轻细胞凋亡和氧化应激。
本研究为枇杷核活性成分苦杏仁苷治疗肺气肿提供了一定理论依据,但仅采用了网络药理学单一工具筛选苦杏仁苷的可能作用靶点,得到的结论局限于细胞层面,未来将采用差异表达分析、组学分析等生信手段,全方面佐证苦杏仁苷的作用机制和靶点通路,并进一步探究苦杏仁苷在体内环境中对肺气肿的治疗作用,不断挖掘更多枇杷核活性成分的药用价值。



 下载:
下载: