-
开放科学(资源服务)标识码(OSID):

-
云南黄馨(Jasminum mesnyi Hance)又名云南黄素馨、野迎春、迎春柳、南迎春,属于木犀科(Oleaceae)素馨属(Jasminum)常绿灌木,与迎春花(Jasminum nudiflorum Lindl.)相似。云南黄馨叶片(3~5 cm×1~2 cm)较大,花冠较长;但迎春花多生长在北方,为落叶灌木,先开花后生叶,盛花期无叶片[1-2]。云南黄馨原产于我国,现主要分布于四川西南部、贵州、云南等长江流域以南地带,因其四季常绿、花期较长,观赏价值高,且具备环境适应强、抗逆性高,易于繁殖等诸多优点,广泛应用于园林绿化和景观营造,在城市绿化特别是垂直绿化方面占据重要地位[3-4]。城市绿化种植云南黄馨,还具有良好的生态价值。吕东蓬[5]发现云南黄馨叶片对大气颗粒物污染胁迫具有抗性,有一定的滞尘能力。孙淑萍等[6-7]通过探讨大气污染和SO2对植物细胞内部抗坏血酸、游离氨基酸、叶绿素、可溶性蛋白和脯氨酸含量的影响发现,云南黄馨对大气污染有较强的抗性,能够净化空气中的SO2。另有报道称云南黄馨对甲苯有灵敏的代谢响应和形态表现,可作为一种有效检测土壤甲苯污染的指示植物[8]。另外,也有研究发现云南黄馨提取物主要成分包括β-谷甾醇、α-香树脂醇、β-葡萄糖苷黄酮类,以及芦丁和裂环环烯醚萜苷类物质[9],这些物质具多种活性,其药用潜力巨大。Borar等[10]发现云南黄馨叶片富含抗氧化和抗高血糖活性的物质,在口服葡萄糖耐量试验中表现优异,效果与标准药物二甲双胍相当,可有效控制糖尿病的发生。Dullu[11]利用云南黄馨叶片的乙醇提取物对蚯蚓进行测试,发现其具有驱虫活性。Verma等[12]发现云南黄馨叶片乙醇提取物及其溶剂分馏组分具有广谱抗菌活性,活性提取物主要富含黄酮类和酚类化合物。
目前,关于素馨属(Jasminum)植物病害的报道主要集中在迎春花病害,比如尾孢(Phlebiopsis crassa)[13-14]、多主棒孢(Corynespora cassiicola)[15]、果生刺盘孢(Colletotrichum fructicola)[16]均可引起迎春花叶斑病。而国内外关于云南黄馨病害研究相对较少,目前已知有刺盘孢属(Colletotrichum)的C. siamense、C. nanjingense和C. gloeosporioides造成的叶部病害[17-18]。2018年,Zhang等[19]在合肥市首次从云南黄馨叶斑上分离出多主棒孢(C. cassiicola),此后其他地区也未有多主棒孢(C. cassiicola)为害云南黄馨的报道。本研究通过对武汉地区绿化带中云南黄馨叶斑病病原菌的分离鉴定和生物学特性探究分析,旨在为园林绿化植物病害防控提供理论依据和参考。
全文HTML
-
供试材料:云南黄馨的叶斑病害叶片采自于武汉市洪山区。
PDA培养基:马铃薯200 g,葡萄糖20 g,琼脂16 g,蒸馏水定容至1 000 mL。
-
将采集的云南黄馨的叶斑病害叶片置于自来水下冲洗1~2 min后晾干。在超净工作台内,用经过消毒处理的剪刀从病健交界处剪取组织块(2 mm×2 mm),在0.5%有效氯的NaClO溶液中消毒3~5 min,取出后用无菌水清洗1~2次,每次1 min,洗去消毒液[20]。将消毒、清洗后的组织块用滤纸控干表面多余水分后,转移至含有链霉素(50 mg/L) 的PDA平板上,密封后倒置于28 ℃恒温培养箱黑暗培养,3 d后用灭菌过的接种针从菌落边缘挑取单孢或菌丝于新的PDA平板上进行纯化培养。将获得的纯培养物保存于PDA斜面(4 ℃)及15%甘油中(-80 ℃)备用。
-
将分离所得的病原菌接种到新的PDA培养基上,倒置于28 ℃恒温培养箱中黑暗培养5 d后,用直径为4 mm的无菌打孔器取菌落边缘的菌丝块备用。从花坛中取健康的云南黄馨枝条,在室内进行病原菌离体接种,确定病原菌。首先,用无菌水对云南黄馨健康叶片进行清洗,晾干后采用针刺法在叶片表面制造伤口;然后,用挑针将提前准备好的菌丝块接种至枝条右侧叶片伤口处,枝条左侧叶片仅接种PDA培养基块作为对照;将接种后的叶片放置于铺有浸水脱脂棉的保鲜盒中,保鲜膜密封后,置于28 ℃恒温培养箱中黑暗培养。7 d后从接种的发病叶片上再次采用组织分离法进行病菌分离纯化,观察比较该病原菌与原始接种病原菌是否一致,最终确定云南黄馨叶斑病病原物。
-
菌落形态:取纯化后的菌株,在PDA平板上培养5 d后,用直径为4 mm的无菌打孔器取菌落边缘的菌丝块,转接于新的PDA平板中央,倒置于28 ℃恒温培养箱中24 h黑暗培养,观察记录菌落形态和颜色。
孢子形态:取纯化后的菌株,在PDA平板上培养,待分生孢子形成后,在体视镜下用挑针挑取少许霉层制作玻片,并在显微镜下观察病原菌的形态结构,包括产孢结构的特征,以及分生孢子的形态、颜色、大小,并根据形态学特征初步确定病原菌的种类。
-
将纯化的菌株转接于PDA平板上,置于28 ℃黑暗培养,待菌丝长满平板后刮取收集菌丝体。将收集的菌丝体装入1.5 mL离心管中,加入液氮后快速研磨成白色粉末,采用改良CTAB法[21]提取菌株的基因组DNA,-20 ℃保存备用。使用真菌通用引物引ITS5(5′-GGAAGTAAAAGTCGTAAGG-3′)和ITS4(5′-TCCTCCGCTTATTGATATGC-3′)进行PCR扩增。采用20 μL PCR反应体系:2×Taq PCR StarMix Loading Dye 9.5 μL、正反向引物各1 μL、模板DNA 1 μL、ddH2O 7.5 μL。扩增条件:94 ℃预变性3 min;94 ℃变性40 s,56 ℃退火40 s,72 ℃延伸1 min,共35个循环;72 ℃再延伸10 min。扩增产物经过1%琼脂糖凝胶电泳检测后,送往华大基因有限公司进行核酸测序。根据测序结果在NCBI上进行序列比对,并下载相近序列,利用MEGA 6.0极大似然法构建系统发育树。
-
不同光照条件对菌丝生长的影响:取纯化后的菌株,在PDA平板上培养5 d后,用直径为4 mm的无菌打孔器取菌落边缘的菌丝块,转接于新的PDA平板中央,密封后将菌丝块置于28 ℃恒温培养箱中接受不同光照条件处理;试验共设置24 h连续光照、12 h/12 h光暗交替照射、24 h连续黑暗3个处理,每个处理重复3次,7 d后采用十字交叉法测量菌落直径。
不同温度对菌丝生长的影响:方法参照不同光照条件对菌丝生长的影响,密封后将接种菌丝块的PDA平板分别置于不同温度条件的恒温黑暗培养箱中培养。温度设置4 ℃、8 ℃、12 ℃、16 ℃、20 ℃、24 ℃、28 ℃、32 ℃、36 ℃和40 ℃共10个处理。
不同pH值对菌丝生长的影响:方法参照不同光照条件对菌丝生长的影响,密封后将接种菌丝块的PDA平板置于28 ℃恒温培养箱中黑暗培养,PDA培养基的pH值通过使用1 mol/L的氢氧化钠溶液和盐酸溶液进行调节,pH值设置分别为4、5、6、7、8、9、10共7个处理。
不同碳源对菌丝生长的影响:方法参照不同光照条件对菌丝生长的影响,以不含碳源的Czapek培养基为基础培养基,将其中的碳源等量设置为葡萄糖、乳糖、蔗糖、麦芽糖、果糖、D-甘露醇及可溶性淀粉。
不同氮源对菌丝生长的影响:方法参照不同光照条件对菌丝生长的影响,以不含氮源的Czapek培养基为基础培养基,将其中的氮源等量设置为硝酸钾、硝酸钠、蛋白胨、甘氨酸、硫酸铵及尿素。
-
用SPSS 27.0软件的ANOVA程序进行方差分析,LSD法分析试验中不同处理之间的差异,t测验比较2种处理之间的差异显著性。
1.1. 材料
1.2. 方法
1.2.1. 病原菌的分离纯化
1.2.2. 病原菌的致病性检测
1.2.3. 病原菌的形态学鉴定
1.2.4. 病原菌的分子生物学鉴定
1.2.5. 病原菌的生物学特性
1.3. 数据统计与分析
-
观察发现,云南黄馨健康植株茂盛浓绿、叶片舒展(图 1a),但发病后症状集中在叶片部位,发病早期病斑较小,仅有黑褐色的不规则斑块或浅褐色斑点,多集中在叶片边缘及叶尖部位,少量病斑出现在叶片中部。随着病害蔓延扩大后,病健交接处颜色仍保持黑褐色,但病斑中心颜色逐渐变浅至黄褐色,病斑呈现轮纹状,叶缘部位似火烧状干枯,部分发病严重的植株叶片卷缩,甚至脱落(图 1b)。
-
通过对病健交界处的组织分离纯化培养后,共得到4株不同类型的真菌,并分别命名为X-1、X-2、X-3、X-4。将纯化后的4株真菌分别采用针刺法接种在云南黄馨叶片7 d后,发现X-2、X-3、X-4 3株真菌未能造成叶片发病,仅有X-1菌株可以导致接种叶片发病,病健交界处病斑为黑褐色,与田间症状表现相似;而仅接种PDA培养基块的枝条左侧叶片,未出现发病症状(图 1c)。对接种发病叶片再次进行分离纯化,通过观察菌落形态和显微结构,确定与X-1菌株为同一病原菌,实现柯赫氏法则的验证。
-
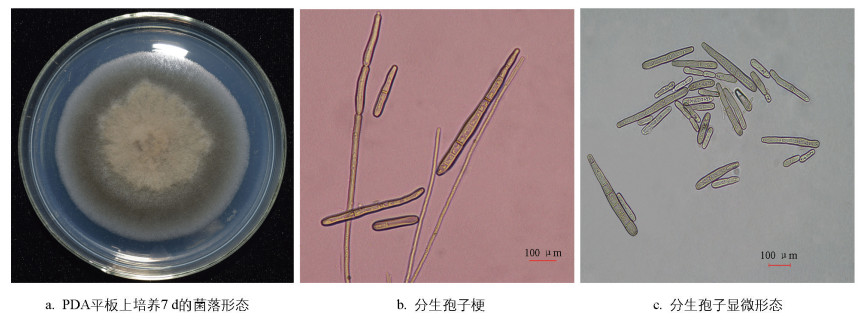
观察菌落形态发现,菌株X-1在PDA平板上的菌落特征明显,形状为近圆形,菌落边缘菌丝呈白色绒毛状,菌落中央部分隆起,呈灰褐色,菌落背面中央区域呈橄榄绿至浅褐色(图 2a)。挑取菌落中央部位菌丝在显微镜下可观察到褐色的分生孢子梗和分生孢子,分生孢子梗长、直立或稍弯,单独或成簇生长。分生孢子单生或串生,倒棍棒形或圆柱形,假隔膜2~12个,大小为15~163 μm×5~15 μm(图 2b、2c)。综合上述形态学特征,初步将菌株X-1鉴定为棒孢属(Corynespora sp.)真菌。
-
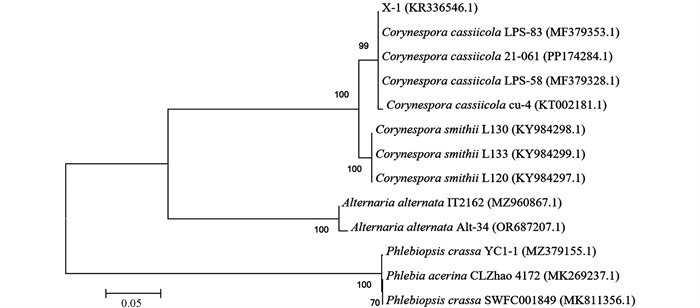
菌株X-1基因组DNA通过PCR扩增及测序后获得长度为574 bp的ITS序列,并将其rDNA-ITS基因序列上传至NCBI的GenBank数据库获得登录号KR336546.1。同时,在NCBI中对该序列同源相似性进行Blast分析,发现X-1的rDNA-ITS序列与多主棒孢Corynespora cassiicola相似性均在99%以上,其中与菌株LPS-83、21-061、LPS-58和cu-4(GenBank登录号分别为MF379353.1、PP174284.1、MF379328.1、KT002181.1)的相似性分别为100%、100%、99.48%、100%。从NCBI中下载棒孢属及其近源属其他种的rDNA-ITS序列,采用MEGA 6.0软件构建系统发育树,结果显示菌株X-1与Corynespora cassiicola聚在一起,bootstrap支持率为99%,而与近源属及棒孢属其他种的关系较远(图 3)。综合形态学和分子生物学鉴定结果,最终将菌株X-1鉴定为多主棒孢Corynespora cassiicola,这是湖北地区关于多主棒孢C. cassiicolae引起云南黄馨叶斑病的首次报道。
-
光照试验发现,不同光照条件对菌丝生长影响存在差异。该菌株X-1在12 h/12 h光暗交替的条件下,7 d后其菌落直径可达到70.33 mm,显著高于24 h连续黑暗条件下的菌落直径,但与24 h连续光照条件下的菌落直径无显著差异,且24 h连续光照和24 h连续黑暗条件下的菌落直径也不存在显著性差异(表 1)。试验表明,光照是该菌株X-1的影响因子之一,适当光照有利于该菌株的菌丝生长,12 h/12 h光暗交替条件为最佳光照条件。
-
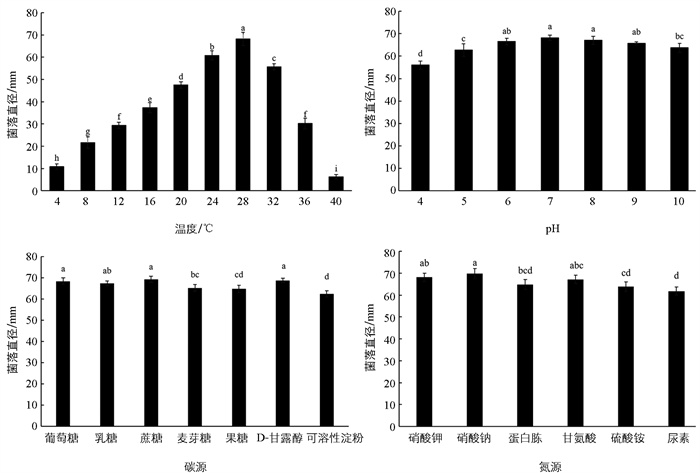
试验发现,菌株X-1在4~40 ℃条件下均可生长,但当温度低于4 ℃或高于40 ℃时,菌落生长极为缓慢。从变化趋势看,随着温度升高,菌丝生长速度逐渐加快,28 ℃时菌丝生长最快,其菌落直径显著高于其他温度的菌落直径,之后温度越高,生长越慢,且菌丝生长速度下降幅度明显(p<0.05,图 4)。
-
培养7 d后发现,菌株X-1在pH值为4~10的平板中均能生长,对pH值适应范围较为广泛。当pH值为4、5和10时,菌落生长较为缓慢,菌落直径显著低于pH值为7和8时的菌落直径,表明菌株X-1对酸性和强碱性环境较为敏感。虽然pH值为7和8时菌落直径最大,而当pH值在6~9时,各处理的菌落直径之间没有显著性关系,证明菌株X-1的最适宜生长pH值范围为6~9(p<0.05,图 4)。
-
在7种碳源培养基上,菌株X-1均能生长,菌落直径从大到小依次为蔗糖、D-甘露醇、葡萄糖、乳糖、麦芽糖、果糖和可溶性淀粉,其中以蔗糖为碳源的菌落直径与以D-甘露醇、葡萄糖、乳糖为碳源的菌落直径不存在显著性差异,但是显著高于以麦芽糖、果糖和可溶性淀粉为碳源的菌落直径(p<0.05,图 4)。
-
在6种氮源培养基上,菌株X-1均能生长,菌落直径从大到小依次为硝酸钠、硝酸钾、甘氨酸、蛋白胨、硫酸铵和尿素,其中以硝酸钠、硝酸钾、甘氨酸为氮源的菌落直径最大,这3种氮源间的菌落直径不存在显著性关系,但以硝酸钠、硝酸钾为氮源的菌落直径显著高于以硫酸铵和尿素的为氮源的菌落直径(p<0.05,图 4)。
2.1. 云南黄馨叶斑病田间症状
2.2. 病原菌的分离纯化和致病性检测
2.3. 病原菌的形态学鉴定
2.4. 病原菌的分子生物学鉴定
2.5. 病原菌的生物学特性
2.5.1. 不同光照条件对菌丝生长的影响
2.5.2. 不同温度对菌丝生长的影响
2.5.3. 不同pH值对菌丝生长的影响
2.5.4. 不同碳源对菌丝生长的影响
2.5.5. 不同氮源对菌丝生长的影响
-
多主棒孢是棒孢属内发现最早的种,寄生范围广,可侵染70多个国家的53科380属530多种植物,包括单子叶、双子叶、苏铁类和蕨类植物[22-23]。在农业生产中,能够给黄瓜、大豆、茄子、甜瓜等农作物带来严重的经济损失[24-25]。多主棒孢主要通过分生孢子进行大量繁殖,借助风、雨或农事操作进行传播,分生孢子侵染植物后会刺激寄主植物分泌纤维素酶、果胶酶等多种化学物质,分解破坏植物细胞结构,导致植物细胞的死亡[26]。多主棒孢因喜好高温高湿环境、极易发生变异、侵染破坏力强,已逐渐由次要病害上升为世界公认的主要病害,并有向新寄主发展蔓延的趋势[27]。武汉地区高温高湿的气候,符合多主棒孢的流行和蔓延的条件。
本研究通过对云南黄馨发病叶片的致病菌进行分离纯化,并对纯化出的菌株进行柯赫氏法则验证发现,菌株X-1在针刺条件下7 d后能够致使云南黄馨叶片发病,发病部位边缘呈现黑色,与田间病斑边缘黑色症状相似,将菌株X-1确定为病原真菌。为进一步确定病原菌X-1的种类,试验综合了形态学观察和rDNA-ITS分子生物学鉴定,结果显示菌株X-1菌落形态和产孢结构符合棒孢属真菌形态特征,且BLST比对和系统发育树构建也证明了菌株X-1的分类学地位,最终将云南黄馨叶斑病分离菌株X-1鉴定为多主棒孢(C.cassiicolae)。这与Zhang等[19]在合肥地区分离到的云南黄馨多主棒孢叶斑病一致,表明由多主棒孢(C.cassiicolae)引起的叶斑病可能已经作为云南黄馨的一种常见病害需要引起重视,另外,合肥、武汉地区均发现该种病害,进一步说明病害流行范围较广。从现有报道来看,多主棒孢除了可为害云南黄馨和迎春花叶片外,还可造成茉莉花(Jasminum sambac)叶斑病[28],表明多主棒孢有向素馨属植物流行蔓延趋势。素馨属植物多具有园林绿化和药用价值,实际生产中应加强对该病害的监测和防治。目前,由多主棒孢造成的叶斑病主要依靠化学防治,如施用百菌清、多菌灵、代森锰锌、甲基硫菌灵、嘧菌环胺等实现病害控制[26, 29]。
本研究中菌株X-1的最适生长温度为28 ℃,适宜pH值范围为6~9,最适光照条件为12 h/12 h光暗交替,这与所报道的多主棒孢的生物学特性基本一致[30-31],但也有报道称多主棒孢在24 h连续光照条件的菌落生长显著快于光暗交替(12 h/12 h) 和24 h连续黑暗条件下的菌落生长[32]。生物学特性试验也发现不同碳源和氮源对多主棒孢菌丝生长的影响存在差异,本研究中最适菌株X-1菌丝生长的碳源和氮源分别为蔗糖和硝酸钠,但碳源为D-甘露醇、葡萄糖和乳糖时菌株X-1的菌落直径与蔗糖无显著性差异,氮源为硝酸钾和甘氨酸时,与硝酸钠也不存在显著性差异(p<0.05)。这与分离自其他寄主植物的多主棒孢菌株存在一定差异,如薛彩英等[30]报道的分离自河南草莓叶部的多主棒孢最适碳源为葡萄糖,最适氮源为硝酸钾和硝酸钠;陈慧杰等[31]报道的分离自江苏绣球叶片上的多主棒孢最适碳源和氮源分别为乳糖和蛋白胨;李雪梦等[33]报道的分离自河南金银花叶片上的多主棒孢最适碳源和氮源分别为D-甘露醇和胰蛋白胨。这些生物学特性的差异,可能是由于来源不同地区、不同寄主植物的多主棒孢对不同生存环境和寄主的适应性不同导致的。




 下载:
下载: