-
开放科学(资源服务)标识码(OSID):

-
十字花科黑腐病是由野油菜黄单胞菌(Xanthomonas campestris pv. campestris,Xcc)引起的一种系统性维管束病害,其典型症状为叶片萎蔫、维管束组织褐变坏死,进而在叶中脉上产生“V”形黄色病斑,严重影响甘蓝(Brassica oleracea var. capitata)、花椰菜(B. oleracea var. botrytis)和西兰花(B. oleracea var. italica)等具有重要经济价值的蔬菜作物的产量和品质[1-2]。目前在农业生产中,主要依赖含铜杀菌剂(如波尔多液)和抗生素类药剂(如链霉素)进行黑腐病的化学防控[3]。然而,长期使用这些化学药剂不仅会导致Xcc菌株产生显著的抗药性,而且会引发化学残留、土壤污染与食品安全等问题。因此,开发环境友好的新型生物抑菌剂成为十字花科黑腐病防治的重要研究方向之一。
Xcc是一种典型的革兰氏阴性需氧杆菌,其菌体形态学特征表现为两端钝圆、中间隆起的杆状结构(1.2~3.5 μm),表面平滑且呈现淡黄色。该菌株具有单极性鞭毛,无芽孢形成能力,可单生或链生,生长最适温度为25~30 ℃,适宜pH值范围为6.1~6.8[4]。Xcc的致病机制涉及胞外多糖(EPS)、胞外酶、生物膜、运动性、III型分泌系统(Type III secretion system,T3SS)等多种毒力因子的协调作用[5]。例如,Xcc会通过分泌多种胞外酶,来降解植物细胞壁的果胶层,促进病原菌在宿主组织中的感染。研究显示,Xcc胞外酶活性与病害严重度呈显著正相关,表明了其在致病过程中的重要性[6]。EPS在Xcc的生物膜形成和环境抗性中发挥关键作用,EPS产量降低,致病力显著减弱,进一步证实了其在Xcc致病性中的核心地位[7]。T3SS是Xcc侵染植物的另一个重要机制,其效应蛋白基因如XopAY和XopL通过抑制植物的模式触发免疫(Pattern-Triggered Immunity,PTI)反应,促进病原菌的侵染,揭示了T3SS效应蛋白在调控植物免疫中的复杂机制[8]。
Chito-Oligosaccharide(COS)是壳聚糖降解产生的低聚物(聚合度2-20),具有水溶性高、生物相容性好、广谱抑菌等特点[9]。研究表明,COS主要通过3种途径抑制植物病原菌:首先,其分子表面携带的正电荷分子与细菌细胞膜中带负电的磷脂结合,破坏膜结构导致K+和三磷酸腺苷(ATP)等关键物质的外流;其次,COS通过抑制病原菌呼吸链酶的活性,干扰电子传递过程,降低能量代谢效率,削弱微生物的生理功能;此外,COS还能作为植物免疫诱导剂,促进植物体内防御相关蛋白的合成,从而系统性提升植物对病原体的免疫响应。这3个层面的协同作用共同构成了COS的广谱抗菌特性[10-12]。基于Xcc的毒力因子和COS的作用机制,壳寡糖作为一种天然抑菌剂,可能通过同时靶向多个致病因子发挥协同抑菌作用。研究表明,COS可通过外源处理减弱烟草的TMV病毒的增殖,从而促进抗病[13];COS可能干扰EPS的生物合成,破坏生物膜的形成,还可能通过调控T3SS效应蛋白的表达或功能,抑制Xcc对植物免疫反应的干扰,但COS对Xcc的抑菌作用并不清楚。
本研究聚焦COS对Xcc的体外抑菌作用分析,明确了COS对Xcc的生长及其多个毒力因子(运动性、胞外酶活性及EPS合成)及效应蛋白基因表达的抑制作用。同时,在甘蓝和萝卜等十字花科植物中比较分析COS对黑腐病的防治效果,研究结果将丰富COS的抗菌谱,为进一步阐明COS的抑菌机制和开发新型高效黑腐病抑菌剂提供一定的理论依据。
全文HTML
-
试验菌株:野油菜黄单胞菌野油菜致病变种Xcc8004,由海南大学陶均教授课题组馈赠。
-
取10 μL菌液接种到5~10 mL的NYG液体培养基(蛋白胨5.0 g/L,酵母提取物3.0 g/L,甘油20 mL/L)中,置于28 ℃、200 rpm培养36 h。
-
供试植物:萝卜(Raphanus sativus L.)、甘蓝(Brassica oleracea var. capitata Linnaeus),均栽培于西南大学园艺园林学院歇马基地。
-
接种Xcc于NYG液体培养基中,28 ℃震荡培养至OD600=0.4,取10 μL菌液接种至新鲜的NYG液体培养基中,加入不同质量浓度的COS溶液,对照组加入等体积无菌水,于28 ℃避光震荡培养36 h,测定各处理组菌液OD600值,每组包含3个独立制备的菌液样本及3次同批次平行测定。
-
将Xcc菌株在NYG培养基中培养(28 ℃,200 rpm)培养36 h,用NYG培养基把菌液的浓度调为OD600=0.4,作为接种液,在接种液中分别加入COS溶液使其终浓度为0.3 mg/mL和0.4 mg/mL,对照组加入等体积无菌水,继续培养2 h,检测方法参考邢芸等的研究[14]进行,每组设置3次技术重复。
1) EPS合成检测:取2 μL上述不同处理的菌液点种于含0.5%琼脂的NYG胞外多糖检测平板中心,静置10 min使菌液吸附,28 ℃培养48 h,分析比较菌落形态及直径变化。
2) 胞外蛋白酶活性检测:取2 μL上述不同处理的菌液点种于含1%脱脂奶粉的NYG胞外蛋白酶检测平板中心,于28 ℃培养2 d,分析菌落周围透明圈直径变化。
3) 胞外淀粉酶活性检测:取2 μL上述不同处理的菌液点在含有0.1%可溶性淀粉的NYG胞外淀粉酶检测平板中心,于28 ℃培养48 h,用1∶100的I2/KI(0.08 mol/L I2,3.2 mol/L KI)溶液染色15 min,用清水将染色液洗净后观察,分析菌落周围透明圈直径变化。
4) 胞外纤维素酶活性检测:取2 μL上述不同处理的菌液点在含有0.5%(W/V)的羧甲基纤维素(CMC)的NYG胞外纤维素酶检测平板中心,28 ℃培养24 h,在平板上加入约20 mL 0.1%的刚果红(Congo Red)染色30 min,水洗两次,再用20 mL 1 M的NaCl脱色两次后观察,分析菌落周围透明圈直径变化。
5) 运动性检测:取2 μL上述不同处理的菌液点种于含0.5%琼脂的NYG游动性检测平板和含有2%葡萄糖的NYG涌动性检测平板中心,于28 ℃培养48 h后观察试验结果。
-
取不同处理后的菌液,按照细菌总RNA提取试剂盒说明书(Servicebio,武汉)提取RNA,反转录为cDNA,具体操作参照反转录预混型试剂盒说明书(Accurate Biology,长沙)。以Xcc thyA为内参基因[15],设计特异引物(表 1)。按照SYBR Green I (江苏百时美生物科技有限公司,连云港)说明书进行qRT-PCR反应。每个样品含3个生物学重复。利用2-ΔΔCT法计算基因表达水平。
-
COS对十字花科作物甘蓝和萝卜黑腐病的防治试验参照李峰等的方法[16],略作修改,具体如下:将Xcc接种于NYG液体培养基中,28 ℃震荡培养至平台期备用。取新鲜白萝卜和甘蓝用自来水清洗干净、晾干后,用75%的酒精消毒;萝卜切成厚约5 mm薄片,甘蓝叶片用1.5 cm的打孔器取样,置于铺有滤纸的9 cm无菌培养皿中(每皿10个甘蓝叶片)。试验设4组验(每组3个重复):3组分别接种Xcc菌液(萝卜100 μL/片,甘蓝20 μL/片),待菌液稍干后,处理组分别施加0 mg/mL、0.3 mg/mL和0.4 mg/mL COS溶液,对照组不接菌,施加等量无菌水。28 ℃培养2~5 d后观察记录结果。
-
本研究所用的t-test和相关性分析均采用SPSS 26.0软件进行处理。
1.1. 试验材料
1.1.1. 菌株来源
1.1.2. 菌株培养
1.1.3. 植物材料
1.2. 试验方法
1.2.1. 最小抑菌浓度(Minimum Inhibitory Concentration,MIC)和最低杀菌质量浓度(Minimum Bactericidal Concentration,MBC)的测定
1.2.2. Xcc致病因子检测
1.2.3. 实时荧光定量qRT-PCR
1.2.4. COS对萝卜和甘蓝黑腐病的防治试验
1.2.5. 数据处理方法
-
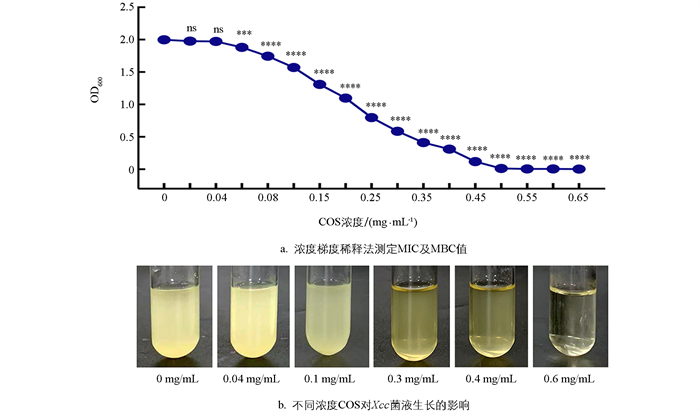
采用浓度梯度稀释法测定COS对Xcc的最低抑菌质量浓度(MIC)和最低杀菌质量浓度(MBC),如图 1所示。在不同浓度的COS处理Xcc菌液36 h后,在0~0.65 mg/mL浓度范围内,OD600值随COS的浓度升高而显著下降,COS质量浓度在0.06 mg/mL时能够显著抑制Xcc的生长,表明COS对Xcc的最低抑菌质量浓度(MIC) 为0.06 mg/mL;当COS质量浓度达到0.5 mg/mL时,Xcc的活性被完全抑制,即最低杀菌质量浓度(MBC)为0.5 mg/mL。本研究选取了0.3 mg/mL和0.4 mg/mL作为后续试验中COS对Xcc致病因子的试验浓度。
-
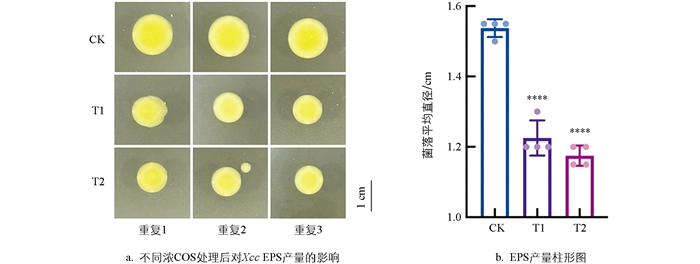
如图 2所示,随着COS浓度的逐步增大,平板中Xcc菌落的直径呈现出逐渐下降的趋势。在COS的浓度为0.3 mg/mL时,菌落直径由1.55 cm减小至1.25 cm;在浓度为0.4 mg/mL时,菌落直径由1.55 cm减小至0.95 cm,较对照组减小至61.3%。这表明COS对Xcc的EPS合成产生了明显的抑制作用。
-
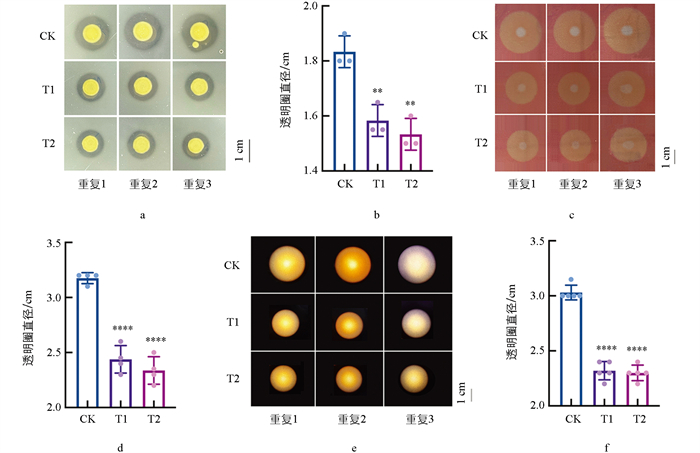
如图 3所示,在0.3 mg/mL和0.4 mg/mL COS处理时,能显著抑制Xcc胞外酶的分泌。在添加0.3 mg/mL COS时,胞外蛋白酶菌落直径由1.85 cm减小至1.55 cm,纤维素酶菌落直径由3.2 cm减小至2.4 cm,淀粉酶菌落直径由3.1 cm减小至2.4 cm;而在COS浓度为0.4 mg/mL时,Xcc的胞外酶的菌落直径分别下降至78.9%、71.9%、73.3%。研究结果说明COS对Xcc胞外酶的分泌均具有显著抑制效果。
-
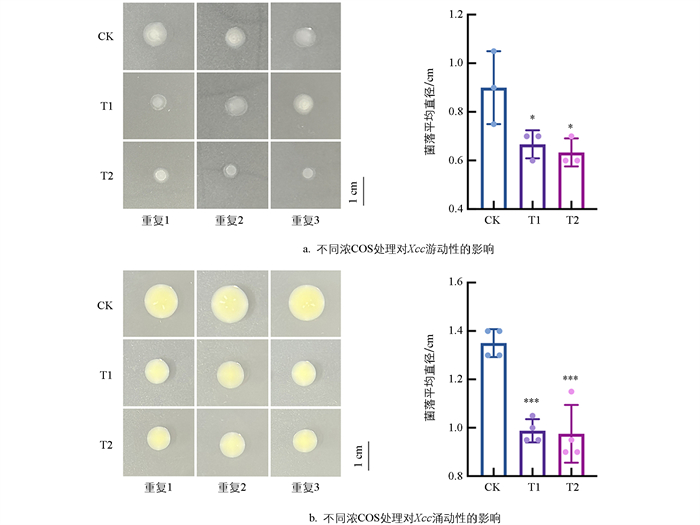
Xcc的致病因子还包括其运动性,细菌运动的方式主要是涌动(Swarming motility)、游动(Swimming motility) 和颤动(Twitching motility) 3种[17],本研究主要聚焦于COS对Xcc涌动性和游动性的抑制作用。如图 4所示,在COS浓度为0.3 mg/mL时,与对照组相比,Xcc游动能力和涌动能力均减弱;而在0.4 mg/mL的COS作用下,Xcc的游动直径由0.9 cm降至0.6 cm,仅为对照组的66.7%(图 4a、4b),涌动直径由1.35 cm降为0.95 cm,仅为对照组的70.4%(图 4c、4d)。试验结果表明COS对Xcc的运动性具有显著的抑制作用。
-
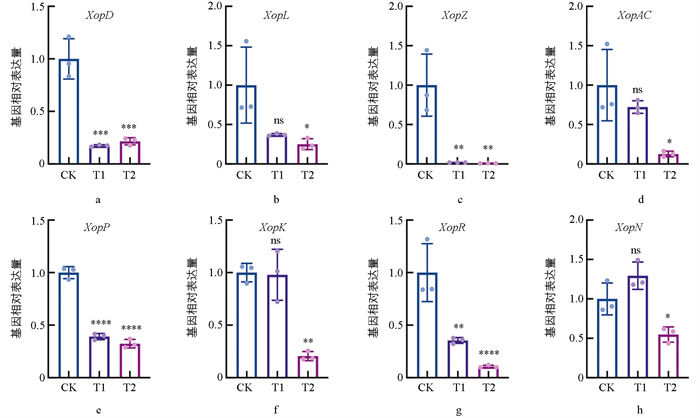
效应蛋白也是Xcc致病性的重要因素之一,本研究检测了COS处理后,Xcc关键毒力基因的表达变化。如图 5所示,在添加0.3 mg/mL COS处理时,效应蛋白基因XopL、XopAC、XopK和XopN的相对表达量无明显差异(图 5b、5d、5f、5h),XopZ、XopR的相对表达量具有显著差异(图 5c、5g),XopD、XopP的相对表达量具有极显著差异(图 5a、5e);而在添加0.4 mg/mL COS处理时,效应蛋白基因XopL、XopAC和XopN的相对表达量均显著降低(图 5b、5d、5h),XopD、XopZ、XopP、XopR、XopK的相对表达量具有极显著差异(图 5a、5c、5e、5g)。其中,COS对XopZ基因的表达抑制最为显著,其表达量仅为对照组的1.78%(图 5c)。
-
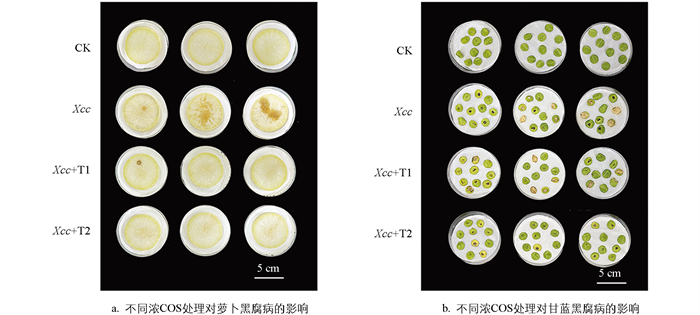
本研究发现COS对Xcc的致病因子有显著抑制效果,接下来探讨了外源COS处理对十字花科作物萝卜和甘蓝黑腐病的防治效果。由图 6所示,在接种黑腐病病菌Xcc8004后,与对照组仅接菌而不添加COS相比,当接种液中分别添加0.3 mg/mL和0.4 mg/mL浓度的COS时,萝卜黑腐病的发病症状显著减轻(图 6a);然而,相同浓度的COS对甘蓝黑腐病的抑制效果并不显著(图 6b)。这一现象表明,COS对十字花科不同作物中黑腐病的防治效果存在显著差异,可能与不同寄主植物对COS的吸收代谢特性不同或病原菌侵染宿主时的特异性机制相关。
2.1. COS对Xcc的抑菌活性分析
2.2. COS对Xcc分泌EPS能力的影响
2.3. COS对Xcc分泌胞外酶的影响
2.4. COS对Xcc运动性的影响
2.5. COS对Xcc效应蛋白基因表达的影响
2.6. COS对十字花科作物甘蓝、萝卜黑腐病的离体防治效果
-
目前国内外对Xcc的致病机制已有系统性研究,已明确多个关键毒力因子[18-22],其治病过程依赖多种途径。例如,EPS通过聚集堵塞植物木质部导管,阻碍水分运输并改变细胞渗透压,最终引发叶片萎蔫及组织坏死;T3SS介导效应蛋白转运以促进病原体定殖[23];多种胞外酶(胞外蛋白酶、纤维素酶和淀粉酶)协同降解植物细胞壁组分,为病原菌的入侵与定殖创造条件[17]。然而现有防治手段仍面临双重挑战:一方面,化学农药因环境风险和抗药性发展问题难以持续;另一方面,生防菌受限于田间稳定性不足和作用迟缓。因此,靶向Xcc毒力因子的新型抑菌剂研发成为突破方向。近期研究发现,植物天然产物如儿茶素可通过破坏Xcc细胞膜或抑制胞外蛋白酶发挥抑菌作用,但其分子机制尚未阐明[16],本研究发现,COS可多靶点Xcc活性,兼具环境友好性和速效性(在一定浓度下,短时间内即可完全抑制Xcc菌株的生长),展现出一定的应用潜力。
革兰氏阴性菌利用T3SS将其效应因子注入植物细胞内,最终导致植物感病。目前对于Xcc8004的效应因子的研究已经取得了系列进展[24-26]。例如,当Xcc效应蛋白XopD[27]和XopL[28]发生突变时,其对宿主的定殖能力显著下降,但其作用机制尚不明确。近期的研究表明,XopAM效应蛋白基因具有脂酶活性,进而影响植物细胞内的脂质稳态,在植物细胞过敏性坏死过程发挥重要作用[29]。本研究初步揭示了COS对T3SS效应蛋白的抑制作用:不同浓度的COS处理均使Xcc效应蛋白基因XopL、XopD的表达量显著下调,在0.3 mg/mL时分别下调了83.6%、63.4%,而在0.4 mg/mL时的浓度分别下调了80.5%、76.1%。同时也检测了其他6个Xcc关键效应蛋白的表达量,在0.4 mg/mL时均下调了50%以上,暗示其对T3SS效应蛋白功能的广谱性抑制。然而,该调控是否通过全局调控因子(如Clp或RsmA)实现仍需验证。此外,当前研究尚未阐明COS与宿主免疫响应的关联性——例如其是否通过诱导植物防卫基因表达来增强抗病性,这一方向值得进一步探索。
COS作为壳聚糖的低聚物,具有广谱的抑菌特性,其抗菌机制具有多靶点特性:对革兰氏阳性菌(如金黄色葡萄球菌)可通过重塑能量代谢途径实现增殖抑制[30];对革兰氏阴性菌(如大肠杆菌)则能特异性阻断DNA转录过程[31];对铜绿假单胞菌,可通过干扰群体感应系统显著抑制生物膜形成[32]。本研究中,COS对Xcc的抑制作用涉及抑制III型分泌系统效应蛋白分泌、降低细菌运动性等多重协同机制。此外,COS在抗病毒领域同样表现出色。研究表明,COS能够有效预防番茄晚疫病、黄瓜白粉病和辣椒病毒病等果蔬病害的发生,其作用机制涉及诱导植物产生系统抗性、干扰病毒复制周期等多个方面。这些特性使得COS在绿色农业和可持续植保领域具有广阔的应用前景[33]。
COS作为植物免疫激活剂,可通过激活水杨酸(SA)和茉莉酸(JA)信号通路增强宿主抗性[12, 34]。有趣的是,而T3SS效应蛋白(如XopL)可通过干扰植物SA信号通路,从而抑制宿主免疫反应[8]。基于此,本研究推测COS可能通过“双效抑制”模式发挥作用:一方面通过显著下调T3SS效应蛋白基因(如XopL、XopD),直接削弱病原菌入侵与定殖能力;另一方面可能通过激活SA/JA信号通路,提升植物自身防御机制。在后续研究中,进一步明确COS对SA/JA通路的具体调控节点及其与Xcc效应蛋白(如XopD)的互作靶点对于解析COS抑制十字花科黑腐病的发生是十分必要的;同时,还需验证COS对不同十字花科作物黑腐病抑制效果差异的分子机制,并评估长期施用对作物生理(如光合作用、根系发育)的影响,以确保符合绿色农业对环境友好型杀菌剂的要求。此外,鉴于COS的安全性和环境相容性,可探索其与植物诱抗剂(如茉莉酸甲酯)或生防菌(如枯草芽孢杆菌)的协同应用,通过多靶点联合调控提升防控效率,同时延缓病原菌抗药性发展,兼顾生态安全与田间实用价值。
-
本研究明确了COS对Xcc具有显著抑制作用,可显著抑制其胞外多糖和运动性、胞外酶等毒力因子。离体控病试验表明COS对白萝卜的黑腐病有显著防控效果,但对甘蓝黑腐病的抑制效果并不显著,为病害绿色防治和COS功能拓展提供了一定的参考依据。



 下载:
下载: