-
开放科学(资源服务)标识码(OSID):

-
环境有机污染物治理是世界范围内亟待解决的重大难题[1-2],这些污染物常包括有机染料(如罗丹明B、亚甲基蓝、甲基橙等)、有机农药(如吡啶环类物质等)、石油类(如多环芳烃等)、阻燃剂(如磷酸酯类物质等)、增塑剂(如邻苯二甲酸酯类物质等)等[3-4]. 诸如罗丹明B(Rh B)在内的一些有机污染物因其自身物理及化学性质相对稳定,能够在自然环境中存在数十年,很难有效自我降解消除,这不仅构成了巨大的环境风险,而且还会随摄食过程进入生物体内,对生物体健康造成严重威胁[5].
基于硫酸根自由基的高级氧化技术因其具有优良的选择性和氧化性,常被用于环境有机污染物的降解,其核心机制是羟基自由基(·OH)和硫酸根自由基(SO4-·)的作用[6]. 如Ikechukwu等[7]使用过硫酸盐降解腐植酸获得80%以上整体降解率,但碱性条件下的降解率(98%)优于酸性条件下的降解率(50%). 进一步研究发现,许多金属元素对过硫酸盐有活化作用,可提高其对有机污染物的降解效率,如Fe,Co,Cu,Ag,Mn等[8]. 在可活化过硫酸盐的金属元素中,Fe因活化效率高、无污染残留和价格低等优点被广泛应用[9]. 苏冰琴等[10]利用高温改性钢渣与碱协同活化过硫酸盐降解甲基橙和苯酚,在25 ℃、pH值为7时降解率可分别高达90.5%和100%. 除上述均相降解体系外,使用固相负载材料构建的非均相体系,可在进一步提高降解效率的基础上有效降低二次污染[11]. 研究发现,碳基材料一方面因较强的吸附性能可以稳定自由基并强化其降解作用[12],另一方面其巨大的比表面积可为降解反应提供大量活性反应位点[13]. 再者,碳基材料与金属元素复合可提升后者的分散性并降低其可萃取性,这不仅能提高其活化效率,还可以减少其浸出污染,如Ouyang等[14]成功地合成了活化过硫酸盐降解处理有机污染物的纳米磁铁矿生物炭复合材料. 但总体来看,可用于活化过硫酸盐降解有机污染物的金属氧化物-生物炭复合材料的研究相对较少. 基于此,本研究采用溶胶-凝胶法制备生物炭负载铁锰双金属氧化物复合材料(MFC),以Rh B为目标污染物,研究其制备条件、使用条件对活化过硫酸氢钾(PMS)的降解反应的影响,并探究其工作机制和稳定性.
HTML
-
秸秆生物炭、竹生物炭、椰壳生物炭购自河南平顶山市绿之源有限公司;六水合氯化铁(FeCl3·6H2O)、四水合氯化锰(MnCl2·4H2O)、氯化钠(NaCl)、氨水(NH3·H2O)、叔丁醇[(CH3)3COH]、碳酸氢钠(NaHCO3)、无水乙醇购自国药集团化学试剂有限公司;柠檬酸、PMS购自中国阿拉丁工业有限公司;Rh B购自天津化学试剂研究所有限公司;腐植酸(HA)购自上海麦克林生化科技股份有限公司;去离子水为实验室纯水机自制;上述试剂均为分析纯.
-
MFC复合材料的制备使用溶胶-凝胶法[9]. 取0.01 mol FeCl3·6H2O和0.005 mol MnCl2·4H2O置于烧杯中,用去离子水在室温下溶解后,加入0.015 mol柠檬酸和0.015 mol NaCl,室温下搅拌1 h后用氨水调节pH值到7.0. 取1.67 g生物炭在去离子水中超声分散30 min后加入上述溶液,并在100 ℃条件下加热搅拌至形成黏性凝胶. 将形成的凝胶置于马弗炉中在300 ℃煅烧1 h,产物冷却后研磨并用去离子水洗涤,在60 ℃烘箱中干燥8 h得到成品MFC. 分别将生物炭、负载铁生物炭、负载锰生物炭、同时负载铁和锰生物炭以及锰铁混合物煅烧后的产品用BC,FC,MC,MFC和MF表示. 通过改变制备条件制备不同铁锰比、不同生物炭种类、不同煅烧温度及不同生物炭含量的MFC.
-
利用扫描电子显微镜(SEM)和X射线衍射仪(XRD)对上述制备获得的MFC进行表征. SEM测试利用ZEISS Sigma 300电子显微镜进行. 取少量待测粉末样品于离心管中,加入无水乙醇,室温超声5~10 min后取少量液体滴在硅片上干燥,安置好样品后抽真空,加速电压3 kV,放大倍数5 000倍. XRD利用Bruker D8 ADVANCE X射线衍射仪进行. 将粉末样品加入到玻璃样品架凹槽中,使松散样品粉末略高于样品架平面,取载玻片轻压样品表面,保持样品表面均匀平整且与框架平面一致并刮去多余样品. 测试参数如下:单色Cu靶Kα辐射(λ=1.541 8 Å),电压和电流分别为40 kV和300 mA. 在10°~80°范围内以10 °/min的速度进行2θ扫描.
-
配制100 mL质量浓度为0.1 g/L的Rh B溶液,加入0.03 g的MFC,恒温水浴加热搅拌,分散均匀后加入0.3 g的PMS置于室温下反应,在2 min反应时间间隔下取3.0 mL样品立即用孔径0.45 μm的膜过滤,测定在554 nm处的吸光度,并根据标准曲线确定Rh B含量. 吸光度采用紫外可见分光光度计测试,型号UV-2401PC,购自日本Shimadzu公司. 机制探讨实验时,取100 mL 0.1 g/L的Rh B溶液(pH值为7.0),分别按3.0 g/L和0.3 g/L剂量加入PMS和MFC后,立即加入过量乙醇或异丙醇(自由基猝灭剂)10 mL后置于室温下反应. Rh B降解程度用Ct/C0表示,C0为Rh B的初始质量浓度(g/L);Ct为降解t时刻后Rh B的残留质量浓度(g/L). 采用伪一级反应动力学模型来拟合MFC对Rh B的降解过程,模型方程为lnCt/C0=-kobst,kobs为伪一级动力学反应速率常数.
-
取100 mL 0.1g/L Rh B溶液(pH值为7.0),加入0.3 g和0.03 g的PMS和MFC后,置于室温(25 ℃)下反应至吸光值恒定不变,测定Rh B降解程度. 测定后回收样品,将其离心10 min,沉淀并用去离子水反复洗涤后在100 ℃条件下热风干燥获得回收MFC. 向回收的MFC中加入100 mL 0.1 g/L Rh B溶液(pH值为7.0)和0.3 g PMS后置于室温下反应至吸光值恒定不变,再次测定Rh B降解程度,连续重复4次.
-
所有实验均进行3次重复,实验结果用Excel 2016软件进行处理,采用平均值±标准偏差表示,图表采用Origin 2022及Photoshop 2024进行制作,用Origin 2022进行方差分析和曲线拟合,采用LSD进行多重比较,显著水平为p<0.05.
1.1. 实验材料
1.2. 实验方法
1.2.1. MFC制备
1.2.2. MFC表征
1.2.3. Rh B降解效率评价
1.2.4. MFC重复利用性评价
1.2.5. 数据处理方法
-
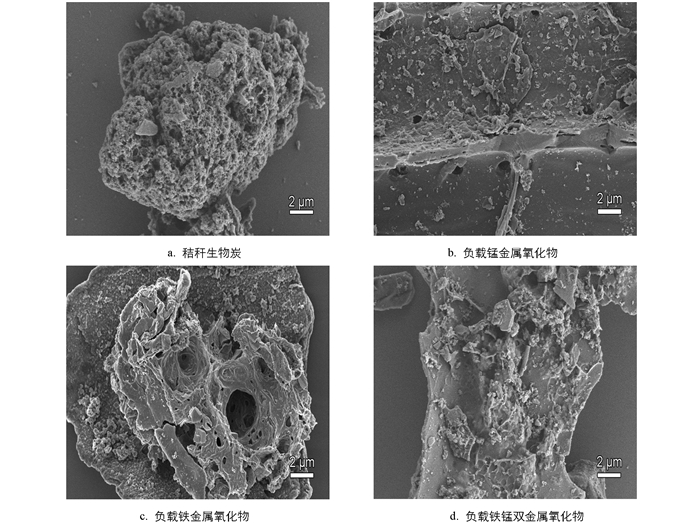
利用秸秆生物炭为原料制备获得的BC,MC,FC,MFC样品的SEM图如图 1所示. 未负载金属氧化物的秸秆生物炭(图 1a)为疏松多孔状结构. 当生物炭负载锰金属氧化物(图 1b)、铁金属氧化物(图 1c)、铁锰双金属氧化物(图 1d)后呈现表面带有细小颗粒的结构. 颗粒的尺寸大约为50~200 nm,应为金属氧化物颗粒. 这些金属氧化物颗粒在复合材料中分散分布,生物炭作为载体有效抑制了其在煅烧过程中的团聚现象,这能为降解反应提供更多的活性位点,有利于提高降解效率.
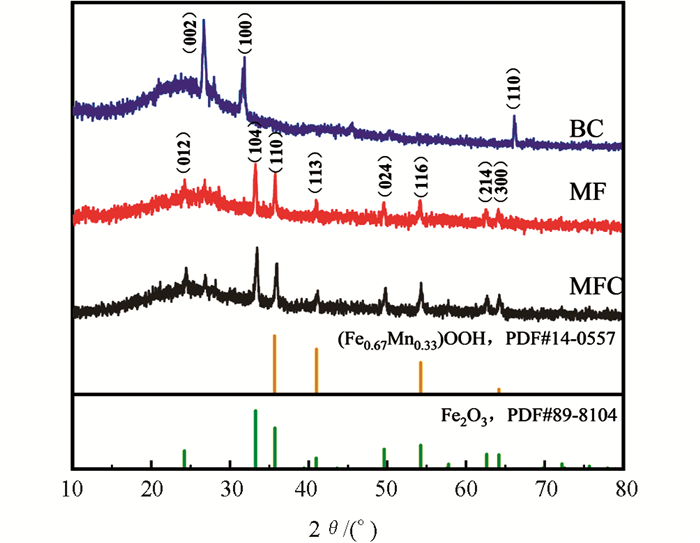
利用秸秆生物炭为原料制备获得的BC,MF,MFC的XRD图如图 2所示. BC有3个衍射峰,其位置与MF和MFC衍射峰的位置不同. 对于MF和MFC,它们都在33.3°,35.7°和54.2°的2θ处出现明显的主要衍射峰. 将其与Fe2O3(pdf#14-0557)和(Fe0.67Mn0.33)OOH(pdf#89-8104)标准卡片比对,可以发现MF和MFC所显示的衍射峰与标准卡片的特征衍射峰一致,3个主要衍射峰分别对应(104),(110),(116)晶面[15],这充分说明通过溶胶-凝胶法可成功制备负载铁锰双金属氧化物的生物炭复合材料.
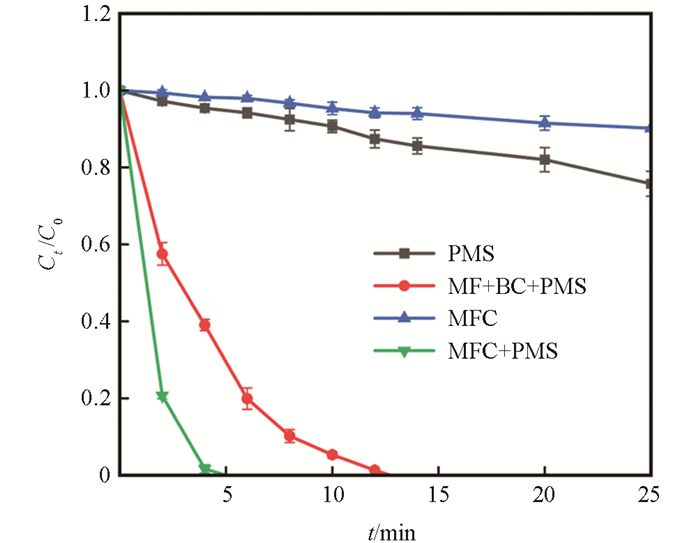
图 3对比了单独使用PMS或单独使用MFC、联合使用MF/BC混合物与PMS以及联合使用MFC与PMS对Rh B的降解效果. 结果显示,单独使用PMS和MFC,在25 min内的降解率仅分别为23.4%和9.8%;联合使用MF/BC混合物与PMS的降解效率明显高于单独使用PMS和MFC,可在12 min内将Rh B全部降解,反应速率常数kobs=0.341 min-1. 这证明铁锰氧化物MF能够活化PMS,促进Rh B降解. 相比之下,联合使用MFC与PMS的降解效率最高,可使降解率在5 min内达到100%,反应速率常数kobs=1.024 min-1,远高于联合使用MF/BC混合物与PMS的结果(0.341 min-1). 这表明将铁锰双金属氧化物负载于生物炭上可大幅度提升其对过硫酸盐的活化作用并促进Rh B降解. 生物炭作为载体能够抑制MF团聚、提供大量反应活性位点、吸附自由基促进反应,从而提高降解速率.
-
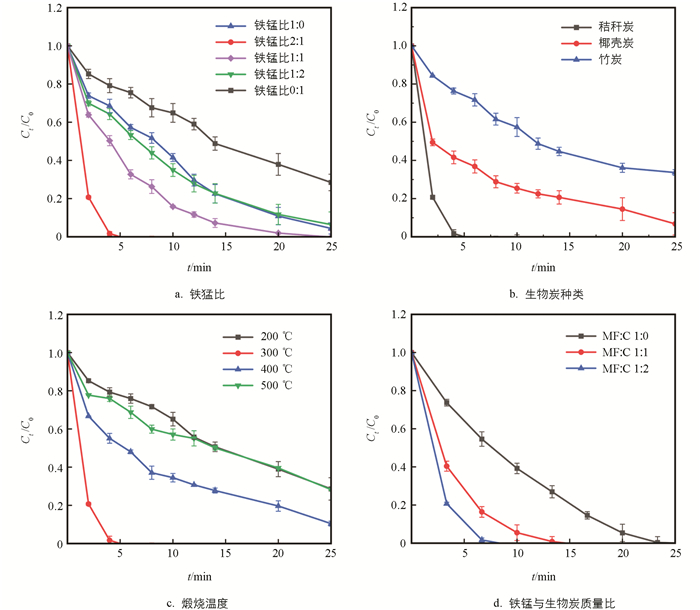
不同制备条件(铁锰比、生物炭种类、煅烧温度、铁锰与生物炭质量比)对MFC性能的影响结果如图 4所示. 当利用秸秆生物炭,在煅烧温度300 ℃、铁锰与生物炭质量比为1∶2时,不同铁锰比下制备的MFC的性能差异巨大(图 4a)(p<0.05). 铁锰比越高,MFC性能越好,且铁锰比为2∶1的MFC可在5 min使Rh B完成降解,降解速率常数kobs=1.024 min-1. 不同铁锰比对MFC效果的影响可能与材料表面官能团和缺陷结构有关,铁锰比改变影响了材料表面酸碱官能团和缺陷结构的种类及数量,进而对反应过程中MFC对活性自由基和有机污染物的吸附效果及活性反应位点造成影响[16]. 生物炭种类对MFC的性能也有明显影响(图 4b). 在煅烧温度300 ℃、铁锰与生物炭质量比为1∶2以及铁锰比2∶1的条件下,选用秸秆生物炭时,MFC的性能最优,明显优于选用椰壳生物炭和竹生物炭的样品(p<0.05). 这可能是不同种类生物炭的结构及表面官能团种类数量不同,影响活化反应中活性位点导致[16]. 就煅烧温度来看(图 4c),300 ℃的效果最佳,高于或低于此煅烧温度对MFC的性能呈现都不利,这是因为煅烧温度改变材料中各组分的含量,影响其最终降解效果. 当在不同铁锰与生物炭质量比的条件下制备MFC,发现铁锰与生物炭质量比为1∶2时,其产物性能明显优于1∶1和2∶1. 这可能是因为体系中过多的铁锰会导致它们在溶胶-凝胶过程中无法得到良好分散效果,易发生团聚而在生物炭中不能均匀负载,减少了活性位点,降低了MFC的性能[17]. 这些结果显示,在溶胶-凝胶法制备MFC时,选用秸秆生物炭、铁锰比2∶1、煅烧温度300 ℃及铁锰与生物炭质量比1∶2时,可制备出性能最好的MFC,其可在5 min使Rh B降解率达到100%,反应速率常数kobs=1.024 min-1.
-
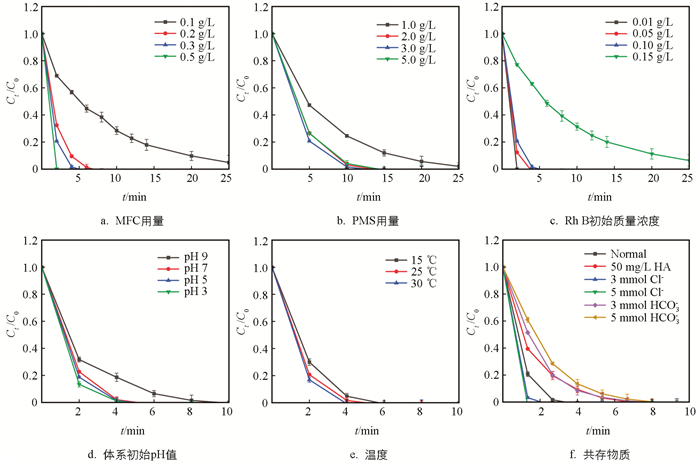
图 5a是MFC用量对其性能的影响结果. 由图 5a可知,Rh B的降解速率随MFC用量的增加而提高. 当MFC用量从0.1 g/L增加到0.2 g/L时,反应速率常数kobs由0.116 min-1大幅度提升到0.713 min-1,但将MFC用量继续从0.2 g/L增加到0.5 g/L时,反应速率常数kobs仅从0.713 min-1提升到1.491 min-1,即随MFC用量的增加,反应速率的增速在不断降低. 这是因为MFC用量较低的情况下,体系中产生的活性氧物质数量有限,单位质量底物Rh B可用活性氧数量有限,为活性氧效率提升提供了巨大空间. 而随MFC用量增加,这个空间逐渐被压缩,反应速率增速逐渐降低.
图 5b是PMS用量对MFC性能的影响结果. 由图 5b可知,当PMS用量从1.0 g/L增加到3.0 g/L时,随PMS用量增加,Rh B的降解速率显著提升(p<0.05),降解效率由1.0 g/L时10 min降解98%提升到2.0 g/L时6 min降解100%,再到3.0 g/L时5 min降解100%. 在这3个PMS用量下的反应速率常数kobs分别为0.381,0.832,1.024 min-1. 这是因为PMS用量越高,MFC能更高效地与PMS接触而产生更多的活性氧物质[18]. 但PMS用量从3.0 g/L增加到5.0 g/L时,降解速率不增反降,几乎与PMS含量为2.0 g/L时持平,kobs下降为0.794 min-1. 这是因为过量的PMS会生成大量的SO4-·,引发了硫酸根自由基的自湮灭现象[19],具体反应为:SO4-·+SO4-·→S2O82-和SO4-·+S2O82-→SO42-+S2O8·-.
图 5c是Rh B初始质量浓度对MFC性能的影响结果. 由图 5c可见,MFC性能随Rh B初始质量浓度的升高而降低. 当RhB初始质量浓度由0.01 g/L升高到0.10 g/L时,虽然降解速率有一定程度下降,但仍可在5 min实现完全降解. Rh B初始质量浓度为0.01,0.05,0.10 g/L时,反应速率常数kobs分别为1.819,1.242,1.024 min-1. 而当Rh B初始质量浓度升高到0.15 g/L时,经25 min处理Rh B降解率虽达不到100%,但也能达到90%以上. 这说明MFC可在较宽Rh B初始质量浓度范围内保持良好性能.
图 5d是降解体系初始pH值对MFC性能的影响结果. 由图 5d可见,在初始pH值为3~9的体系中Rh B均可在10min内被全部降解,但不同初始pH值条件下的降解速率有明显差异(p<0.05). 总体来看,体系初始pH值越高,降解速率越低. 体系初始pH值分为3,5,7,9时,反应速率常数kobs分别为1.149,1.091,1.024,0.679 min-1. 一方面,体系pH值升高降解效率降低可能原因是在酸性环境更有利于SO4-·生成,而随pH值升高,体系中SO4-·相对含量下降,而·OH相对含量上升,但由于·OH的氧化能力不及SO4-·,导致降解速率降低. 另一方面,体系pH值升高可能导致形成Fe(OH)3等沉淀而附着于MFC表面,阻碍了其表面活性位点与PMS的活化反应[20].
图 5e是反应温度对MFC性能的影响结果. 由图 5e可知,当反应温度从15 ℃升至35 ℃时,Rh B完全降解的时间由6 min缩短至4 min,反应速率常数kobs从0.898 min-1提高到1.159 min-1. 这是因为MFC对PMS的活化过程为吸热反应[17],反应温度上升有利于PMS分解,加速自由基产生,并提高了PMS,Rh B与MFC之间的碰撞频率,从而提升了降解速率.
无机阴离子(Cl-和HCO3-)和腐植酸(HA)广泛存在于水体中,它们可能会对Rh B的降解产生影响. 由图 5f可知,与正常降解组相比,引入Cl-可显著提高Rh B的降解速率. 当Cl-为3 mmol和5 mmol时,反应速率常数kobs分别为1.414 min-1和1.782 min-1,显著高于正常降解组的1.024 min-1(p<0.05). 这是因为Cl-会与自由基发生反应生成氧化活性更高Cl2-·,并进一步转化生成HClO,从而促进了Rh B的降解[21];而与Cl-的作用相反,HCO3-的引入会抑制Rh B的降解,3 mmol和5 mmol HCO3-的反应速率常数kobs分别为0.464 min-1和0.489 min-1,显著低于正常降解组的1.024 min-1(p<0.05). 这是因为HCO3-对自由基具有猝灭作用,生成氧化还原电位更低的CO3-·和HCO3-·,导致Rh B的降解率降低[22]. 和HCO3-一样,腐植酸也会抑制Rh B的降解,50 mg/L时的反应速率常数kobs为0.553 min-1,这是因为腐植酸作为天然有机物的一种,反应过程中与Rh B相互竞争,消耗生成活性自由基[23],从而抑制了Rh B的降解.
-
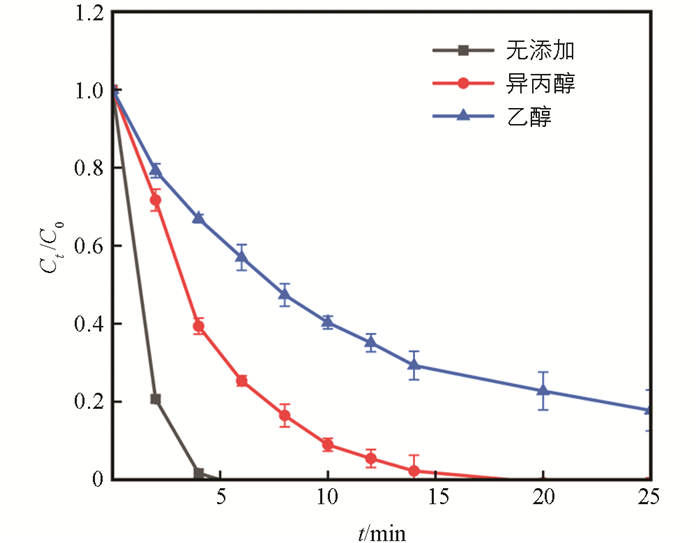
为进一步探讨SO4-·和·OH在MFC活化PMS降解Rh B中的贡献,研究了两种自由基捕获剂对降解效率的影响,其中异丙醇可专一性捕获·OH,而乙醇可同时捕获两种自由基[24]. 由图 6可知,异丙醇可使Rh B的完全降解时间由5 min延长至18 min,反应速率常数kobs由1.024 min-1降低到0.464 min-1(p<0.05);而乙醇导致Rh B的降解速率呈现更大幅度下降,在25 min时也只有80%,反应速率常数kobs由1.024 min-1降低到0.069 min-1(p<0.05). 从两种自由基捕获剂导致的kobs下降幅度可初步判断在不考虑两种自由基相互影响的情况下,MFC活化PMS降解Rh B的过程中·OH的作用大于SO4-·.
-
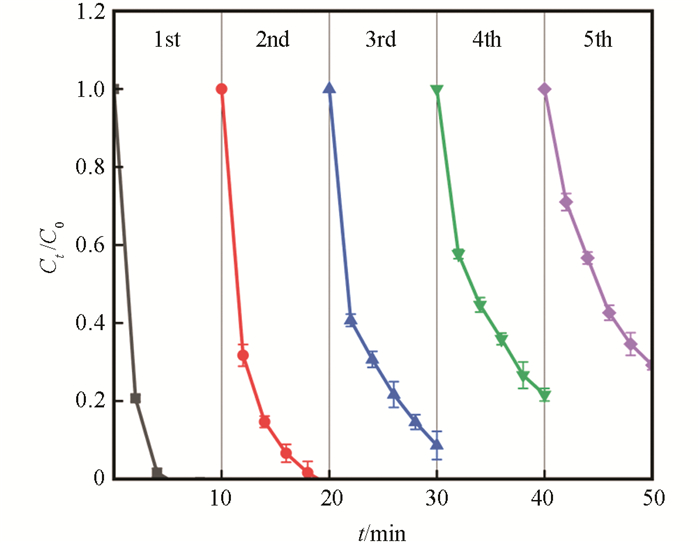
固相催化剂或活化剂的重复利用性对其极为重要,本质上由其稳定性决定. 对MFC连续5次回收循环利用结果显示(图 7),Rh B降解效率随MFC循环利用次数的增加而逐渐降低,5次的反应速率常数kobs分别为1.024,0.591,0.239,0.138,0.124 min-1,呈逐渐下降趋势(p<0.05). 第2次循环时可在9 min内实现完全降解,所用时间相较于初次降解的5 min明显增加(p<0.05). 当第3,4,5次循环利用时,虽无法在10 min内实现完全降解,但降解率仍可分别达到93.25%,79.77%和70.8%,这表明MFC的稳定性和可重复利用性较好.
2.1. MFC表征及活化性能
2.2. 制备条件对MFC性能的影响
2.3. 使用条件对MFC性能的影响
2.4. 自由基降解机制初探
2.5. MFC的重复利用性
-
本研究采用溶胶-凝胶法制备生物炭负载铁锰双金属氧化物复合材料MFC,SEM结果显示,金属氧化物以细小颗粒负载于复合材料中,XRD结果显示,复合材料中存在铁锰双金属氧化物. 制备条件对MFC的性能有显著影响,本研究发现,利用秸秆生物炭,在铁锰配比2∶1、铁锰与生物炭质量比1∶2及在300 ℃下煅烧制备获得的MFC性能最佳,可在5 min使Rh B的降解率达到100%,反应速率常数kobs高达1.024 min-1. 此外,MFC的性能随其用量、PMS用量和反应温度的增加而提升,但在初始pH值为3~9时,随pH值的升高而降低. Cl-可显著改善MFC的性能,而HCO3-和腐植酸的存在对MFC效能的发挥不利. 初步研究表明,在MFC活化PMS降解Rh B的过程中·OH的作用大于SO4-·. 本研究制备的MFC具有良好的稳定性及可重复利用性,回收循环利用5次后对Rh B降解率仍可保持在70%以上. 本研究结果提出了一种新型的、可用于活化PMS降解Rh B的生物炭负载铁锰双金属氧化物复合材料,对高效降解环境有机污染物提供了有益参考.





 DownLoad:
DownLoad: