-
开放科学(资源服务)标识码(OSID):

-
苍术属于菊科(Asteraceae)草本植物苍术属(Atractylodes)多年生植物,国内分茅苍术(Atractylodes lancea (Thunb.) DC.)和北苍术(Atractylodes chinensis (DC.) Koidz)。在西汉时期就曾有记载,苍术味辛、苦,可以入药,具有燥湿健脾、祛风散寒、明目等功效[1]。国内报道苍术的药用价值主要是抗炎、抗肿瘤、调节胃肠功能和代谢等,为多种疾病的治疗提供了新的思路和方法[2],是急支糖浆的主要药用成分。近年来随着野生型苍术的资源枯竭,人工种植重茬的面积逐年增加,目前在我国湖北、江苏、安徽、四川、重庆等地都有人工种植基地,仅重庆地区的栽培总量就已达到200 hm2[3-4]。苍术对环境要求严苛,近年来病害问题也越来越严重[5],如内蒙古赤峰地区就曾发现有苍术黑斑病、苍术斑点病、苍术枯萎病、苍术菌核病等[6]。苍术黑斑病目前已成为遏制苍术产业发展的重要病害之一,发病植株叶片从叶缘向内扩散,发病部位呈圆形或不规则,病斑显黑色或黑褐色,发病后期导致整面叶片变黑色焦枯状脱落[7-10],严重影响了苍术的生产质量,因此对于苍术黑斑病的治理研究已刻不容缓。
在湖北地区对苍术黑斑病病原的鉴定曾有过报道,但缺少致病性测定;对于川渝地区苍术黑斑病研究少有报道,大部分的研究仅表明真菌会引发植株上黑斑病的发生。苏会荣等[11]在红树林的白骨壤(Avicennia marina)中发现有零星的黑斑病,鉴定为番茄匍柄霉(Stemphylium lycopersici)。董宁等[12]报道新疆地区链格孢(A.alternate)会引发香梨果萼黑斑病。赵金梅等[13]曾在猕猴桃的黑斑病样品中鉴定出致病菌为链格孢(A.alternate)。黄大野等[14]在重庆地区的水葫芦上也鉴定出了能形成黑斑的病原菌链格孢(Alternaria sp.);崔海洋等[15]在河北秦皇岛地区人工种植的北苍术上也发现了黑斑病,鉴定其病原菌为茄链格孢(Alternaria. solani)。目前对于苍术黑斑病的防治研究也较少,徐晓斌等[16]在对鄂西北地区苍术黑斑病上推荐使用新型苯醚甲环唑水分散粒剂,但具体毒力测定数据尚未有报道。
本研究对川渝地区苍术人工种植区进行了苍术黑斑病的调查,鉴定了黑斑病病原,并筛选了6种常见药剂对苍术黑斑病病原进行毒力测定,旨在为苍术黑斑病的防治提供科学依据。
HTML
-
越冬苍术样品:从重庆涪陵、城口、巫溪、石柱采集田间越冬的苍术枯萎植株10株,带回实验室于室温下通风处保存。
苍术发病样品:从四川盐源、冕宁、甘洛采集一年生的苍术发病植株共14株,实验室分离鉴定。
试验所用的健康苍术:四川盐源种植基地提供种子在温室内种植备用。
PDA培养基:马铃薯200 g,葡糖糖20 g,琼脂20 g,去离子水1 L;链霉素、氨苄青霉素,赛默飞生物有限公司。
供试药剂:98%多菌灵、96%腈菌唑、98%吡唑醚菌酯、95%苯醚甲环唑、98%啶酰菌胺、97%戊唑醇,湖北康宝泰精细化工有限公司。6种药剂配制为1×104 μg/mL的母液,用于药剂毒力测定。
生化试剂:CATB试剂、DNA纯化回收试剂盒,天根生化科技(北京)有限公司;2×Taq PCR Master Mix、DNA连接试剂盒,大连宝生物工程公司;T-载体试剂盒,北京全式金生物技术有限公司;ITS1/ITS4引物,华大基因生物有限公司。
仪器:倒置显微镜成像平台(Axio Observer),蔡司集团。
-
苍术种植后,次年4-5月在重庆涪陵、城口、巫溪、石柱和四川甘洛、盐源、冕宁的苍术种植区对苍术黑斑病的发生进行调查,在种植区域内采用五点调查法,每个点随机选取10株苍术,观察记录苍术黑斑病的发生并拍照保存。
-
采用常规组织分离法和孢子分离法[17]从越冬苍术及一年生苍术上得到纯化的菌株FL1、FL2、FL3、FL4、FL5、FL6及YY1、YY2、YY3、YY4、YY5、YY6、YY7、YY8、YY9、YY10,重新接种于PDA培养基上,28 ℃恒温培养箱内培养7~9 d后观察和描述菌落的形状、颜色及基质颜色。在倒置显微镜下观察分生孢子的形态、大小并拍照记录,查阅《中国真菌志·链格孢属》[18]根据真菌形态检索真菌种类。
-
按照柯赫氏法则,选用种植在温室内的健康苍术叶片,在实验室进行离体叶片接种试验。叶片用75%酒精进行表面消毒,再用无菌水冲洗3遍后晾干备用。将叶片放置在垫有滤纸的培养皿内培养并用消毒的接种针在叶片表面造成微伤口,取长满培养皿的菌株用直径6 mm的打孔器打好菌饼接种在苍术叶片表面,对照组接种同样大小无菌的PDA,加入适量的无菌水在滤纸上保持湿润;接种后每2 d观察记录1次,将发病的叶片再次分离纯化,得到的菌株与初始病原菌进行比较。
-
病原菌DNA提取,对在PDA培养基上纯化8 d的菌株YY4及FL2采用CTAB法提取基因组DNA,将得到的DNA样品放于-20 ℃冰箱中保存备用。
根据真菌的保守基因通用引物ITS(转录间区)序列、TEF1-α(翻译延伸因子)进行rDNA-PCR扩增,引物参考ITS(登录号:KY014551)、EF(登录号:AB513841)分别为:ITS1:5′-TCCGTAGGTGAACCTGCGG-3′,ITS4:5′-TCCTCCGCTTATTGATATGC-3′;EF-1F:5′-CATCGAGAAGTTCGAGAAGG-3′,EF-1R:5′-TACTTGAAGGAACCCTTACC-3′。PCR反应体系为25 μL:12.5 μL 2×Taq PCR Master Mix(0.05 U/μL、Taq DNA Polymerase、4 mmol/L MgCl2、0.4 mmol/L dNTPs、2×PCR反应缓冲液)、0.5 μL引物F、0.5 μL引物R、1.5 μL样品DNA、10 μL无菌水。PCR扩增程序设置为:94 ℃预变性5 min,94 ℃变性30 s,55 ℃退火30 s,72 ℃延伸60 s,共36个循环,最后72 ℃延伸10 min,12 ℃保温。
PCR扩增的产物经1%的琼脂糖凝胶电泳检测,目的片段经DNA纯化回收试剂盒回收,回收产物由北京六合华大基因科技股份有限公司进行测序。测序结果与GenBank数据库进行序列比对,对比GenBank登录的链格孢属及近似属的序列,经同源性分析,利用MEGA5构建系统发育树,分析亲缘关系,以确定分类地位。
-
根据查阅的相关文献[19-22],利用菌丝生长速率法[21]测定病原菌对药剂的敏感性:将6种配制好的药剂母液根据不同浓度梯度配制成测定浓度,分别取1 mL母液加入到不同浓度的药剂稀释液(49 mL)中,灭菌冷却后倒入50 ℃左右的PDA培养基中,混匀后分别倒入直径9 cm培养皿内,每50 mL倒4个培养皿。苯醚甲环唑、啶酰菌胺、戊唑醇的系列浓度为0.1、0.4、1.6、6.4、25.6、102.4 μg/mL;腈菌酯和吡唑醚菌酯的系列浓度为0.1、0.3、0.9、2.7、8.1、24.3 μg/mL;多菌灵的系列浓度为0.1、0.2、0.4、0.8、1.6、3.2 μg/mL,6种药剂的溶剂均为丙酮。用加入等量无菌水的PDA培养基平板作为空白对照,加入等量丙酮的PDA培养基平板作为溶剂对照。将纯化好的菌株用灭菌打孔器打6 mm的菌饼,接种于培养基中,密封后倒置在28 ℃培养箱中培养7 d,采用十字交叉法测定菌落直径,计算菌落直径平均值和菌丝生长抑制率。利用SPSS 22.0软件对数据进行统计分析,求毒力回归方程(浓度对数值为x;菌落抑制率几率值为y)及抑制率为50%的有效抑制中浓度(EC50)、抑制率为90%的有效抑制浓度(EC90)、相关系数R。
1.1. 试验材料
1.2. 试验方法
1.2.1. 田间苍术病害发生调查及症状观察
1.2.2. 病原菌的形态观察
1.2.3. 病原菌的致病力测定
1.2.4. 病原菌的分子生物学鉴定
1.2.5. 药剂敏感性测定
-
在重庆涪陵、城口、巫溪、石柱和四川甘洛、盐源、冕宁的苍术种植区中调查苍术病害的发生情况,4月下旬至5月初开始出现零星病斑,后期发病加重,发病率约在23.2%,严重时达到86.8%。田间发病的苍术(图 1a、1b)从基部开始向顶部蔓延,叶片出现黑褐色不规则病斑,逐渐向整片叶面扩展,直至整片叶片枯黄,可导致早期落叶,个别枝条枯死。一些叶片从边缘开始出现黑褐色病斑,然后向叶片内部扩展(图 1c),叶片褪绿开始变黄。
-
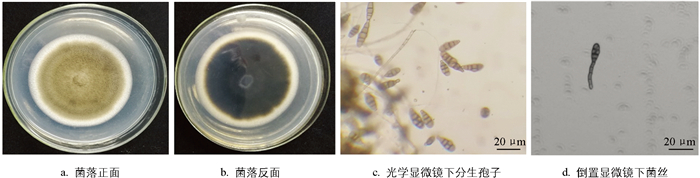
从重庆涪陵采集的越冬植株表面及四川盐源地区的发病苍术叶片上分离纯化得到4种疑似致病菌(FL2、FL4及YY4、YY7),将其接种在PDA培养基中28 ℃培养,发现两地得到的菌株,菌落形态特征基本一致,确认为同一种致病菌,培养1~2 d,外围菌丝均为白色绒毛菌落,并有气生菌丝产生,菌落的平均生长速率达11.8 mm/d,菌丝由白色逐渐变为青褐色,并形成同心圆;9 d后菌丝长满整个培养皿(图 2a、2b)。在光学显微镜下,分生孢子呈青褐色,倒棒状,倒梨状,多横隔,偶有纵隔;菌丝有横隔,长短不一,呈青褐色(图 2c、2d)。根据《中国真菌志·链格孢属》[18]记载的分类标准,将分离得到的菌株初步判定为细极链格孢(Alternaria tenuissima)、链格孢(A.alternata)、长柄链格孢(Alternaria longips)。
-
将纯化得到的YY4菌落针刺接种在健康的苍术叶片上,28 ℃皿内保湿培养,3 d后,接种的叶片开始出点褐色小斑点,逐渐向周围扩展;7 d后接种部位出现明显褐色坏死斑,发病症状与田间自然发病的苍术植株基本相同(图 3)。切取发病叶片病健交界处进行组织分离培养,获得与接种的病原菌形态特征一致的菌落,可以确定分离得到的病原菌即为苍术黑斑病的病原菌。
-
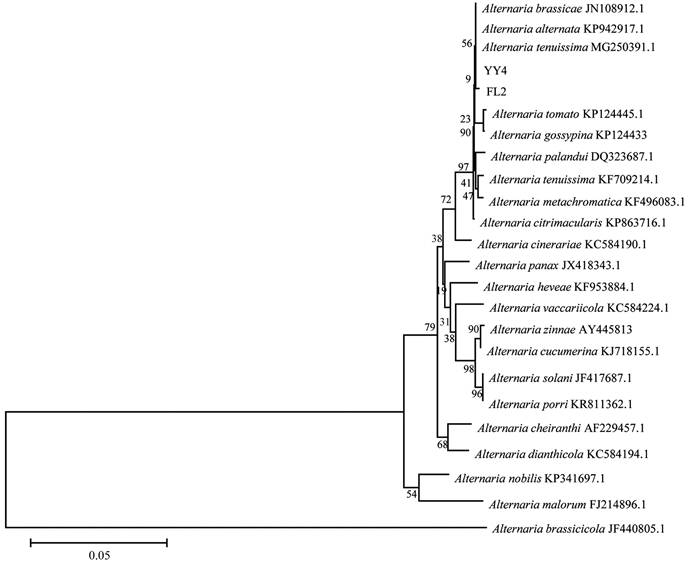
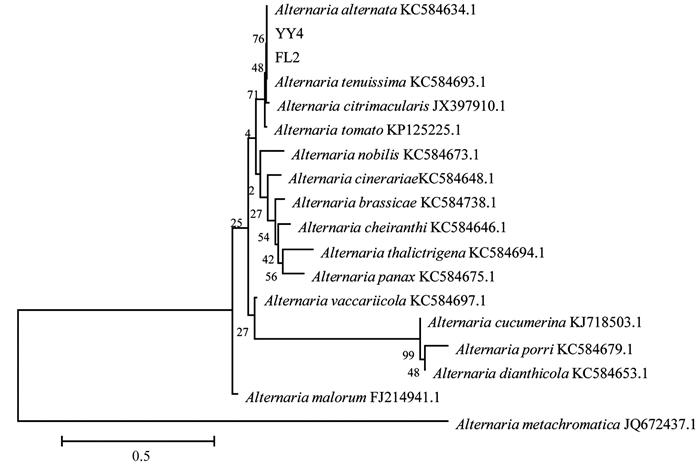
选取FL2及YY4菌株基因组DNA作为模板进行保守基因序列扩增,根据真菌通用引物ITS1和ITS4、EF-1R和EF-1F扩增出570 bp、280 bp的片段,将扩增片段测序后得到的结果提交至GenBank。利用BLAST进行同源性比较,将菌株样品的ITS序列与链格孢属(Alternaria)22种真菌的ITS序列构建系统发育树(图 4),结果显示样品菌株FL2、YY4与A. tenuissima、A. alternata、A. brassicae聚在同一分支上,且该病原菌的ITS序列与这3种菌的同源性最高可达100%。菌株样品的TEF1-α基因序列与Alternaria中16种真菌的TEF1-α序列构建系统发育树(图 5),结果表明菌株样品的TEF1-α基因序列同A. tenuissima、A. alternata、A. citrimacularis聚在同一分支上,并与A. tenuissima、A. alternata的同源性为100%。综合比对结果显示,菌株样品的ITS、TEF1-α基因序列与A. tenuissima、A. alternata的同源性更高。形态学鉴定中观察到该致病菌的分生孢子分隔处轻微缢缩,且分生孢子属于明显的长分生孢子,再结合分子生物学鉴定,判定川渝地区引起苍术黑斑病的病原菌为细极链格孢(A. tenuissima)。
-
6种化学药剂的毒力回归方程、EC50、EC90及相关系数(R)见表 1,供试药剂的相关系数R>0.9,即认为毒力回归方程成立。由表 1可知,每种药剂的毒力回归方程的斜率与药剂毒力成正比,其中多菌灵的斜率值最大,说明病原菌对98%多菌灵更为敏感,EC50仅为0.50 μg/mL;浓度为1.30 μg/mL时即可达到EC90。97%戊唑醇、95%苯醚甲环唑、96%腈菌唑对病原菌的抑制效果比较好,EC50均小于2 μg/mL,分别是1.06、1.52、1.76 μg/mL,其次是98%吡唑醚菌酯和98%啶酰菌胺。
2.1. 田间发病统计及病状观察
2.2. 病原菌的分离纯化及形态特征
2.3. 病原菌致病性测定
2.4. 菌株保守基因序列扩增及分析
2.5. 药剂的敏感性测定
-
链格孢属(Alternaria)真菌中有90%的种可以引起作物病害,给农业生产带来较大的损失[23]。本研究首次在重庆涪陵及四川盐源发现了苍术黑斑病,分离得到的病原在PDA培养基上所表现的菌丝初期为白色,后期从基部开始变为青褐色,最后变为黑色,分生孢子单生,长椭圆形,一端尖,多横隔,偶有纵隔,与王义勋等[24]在湖北调查发现的黑斑病病原形态类似。分子生物学鉴定是现代生物学鉴定中最常见的手段,其中ITS、TEF1-α、TUB等基因均是适用于物种鉴定的诊断工具[25]。本研究对苍术黑斑病病原的2种保守基因ITS、TEF1-α序列扩增后,比对到的结果均与A. tenuissima、A. alternata有很高的同源性。Fan等[26]在苎麻上鉴定出引发苎麻黑斑病的病原菌为A. alternata,据其形态学鉴定的结果发现A. alternata的分生孢子无缢缩。本研究两个地点所分离的链格孢分生孢子更接近椭圆,综合分析,重庆涪陵及四川盐源的苍术黑斑病病原为细极链格孢(A. tenuissima)。
细极链格孢是一种普遍存在的叶部病害斑病原体,可侵染多种作物,例如花椒褐斑病、苹果斑点落叶病、猕猴桃黑斑病、甜瓜黑斑病、芹菜叶斑病、草莓黑斑病、樱桃黑斑病等作物[13, 27-31];同时细极链格孢也是刺五加黑斑病、地黄叶斑病、太子参叶斑病等药用作物病害的病原体[32-34]。本研究表明,细极链格孢(A. tenuissima)也可引起苍术发生黑斑病。
本研究中各种药剂的毒力测定方程反映了6种药剂对病原菌的抑制效果:干扰细胞分裂的药剂多菌灵对病原菌的抑制效果最好;而戊唑醇、苯醚甲环唑及腈菌唑等药剂次之;啶酰菌胺和吡唑醚菌酯对于病原菌的抑制效果不及前两类药剂明显。以上6种药剂均属于内吸性药剂,其中啶酰菌胺和吡唑醚菌酯通过阻止线粒体中的呼吸作用,抑制能量传递来呈现杀菌活性;戊唑醇、苯醚甲环唑和腈菌唑通过阻碍真菌麦角甾醇的生物合成,起到影响生物膜的形成和渗透作用[35-37];多菌灵通过干扰病原菌有丝分裂中纺锤体的形成影响细胞分裂,但病原菌的特定位点如发生突变会导致对此类杀菌剂产生抗性,因此在长期使用杀菌剂的情况下,容易产生具有抗性的病原菌,使得药剂对病害的抑制效果下降[38-39]。戊唑醇、苯醚甲环唑对猕猴桃褐斑病的病原链格孢(A. alternata)抑制效果最强[13],在本研究中这两种药剂抑菌效果也较好。敖显禧等[40]针对贵州核桃叶斑病药剂筛选中用17种药剂对病原进行毒力测定,发现苯醚甲环唑对病原木贼镰刀菌(Fusarium equiseti)的防治效果较好。文克俭等[41]在测定6种杀菌剂对3种禾草病害的防治研究中也表明多菌灵对禾草云斑病的防治效果最好。多菌灵作为一种广谱性杀菌剂,对其他作物的病害也有一定的抑制作用,对链格孢叶斑病(Alternaria alternata)、葡萄孢灰霉病(Botrytis cinerea)、葡萄孢斑点病(Botrytis polygoni)、离蠕孢叶枯病(Bipolaris zeae)、轮斑病菌(Didymella rhei) 和匍柄霉褐斑病(Stemphylium vesicarium)病原菌菌丝生长抑制作用较好(EC50=0.049 μg/mL),但对平头炭疽菌(Colletotrichum truncatum)抑制效果一般(EC50=0.197 μg/mL)[42-44],本研究显示多菌灵对苍术黑斑病的抑制效果最好。
-
侵染重庆涪陵及四川盐源的苍术,引发苍术黑斑病的病原为细极链格孢(A. tenuissima),药剂的室内毒力测定中,多菌灵对病原的抑制效果最佳,对于苍术黑斑病的防治具有一定的作用及潜力。







 DownLoad:
DownLoad: