-
开放科学(资源服务)标识码(OSID):

-
河流生态系统在维持地球表面的水文循环、能量平衡以及气候变化中发挥着重要作用。然而,随着经济的快速发展,城镇人口的增长,人们生产和生活所产生的污水量大幅增加,污水成分也日趋复杂。但污水收集和处理设施的处理效率滞后于当前的需求,从而导致河流水体中污染物浓度超出其承载能力,河流生态系统遭到破坏,难以维持平衡[1-3]。因此,构建有效的城镇河流生态健康评价体系,将有助于监测城镇河流生态系统状况,从而有针对性地开展河流生态修复与治理工作。
Karr[4]在1981年以鱼类为研究对象,基于生物完整性的相关概念,首次系统构建了生物完整性指数(Index of Biotic Integrity,IBI)评价方法体系,并将其应用于河流健康评价中。该方法体系提升了河流健康评价的精度和效率,其综合性和预警功能也为河流的持续管理提供了有效工具。IBI自提出以来,经过几十年的研究与发展,其研究对象已从鱼类扩展到了大型底栖无脊椎动物[5]、浮游动物[6]和浮游植物[7]等,并广泛应用于河流、湖泊、水库、湿地、地下水等多种水生生态系统的健康状况评价中[8-12]。目前,以鱼类和大型底栖无脊椎动物[13-16]为研究对象的完整性指数评价体系的构建最为成熟,以浮游动物和浮游植物[17-19]为研究对象的相关研究也较为丰富。然而,近年来,各地水体普遍遭受了不同程度的污染,水生生态系统退化现象频发,鱼类、大型底栖无脊椎动物、浮游动物和浮游植物的多样性显著减少,导致难以全面准确地评估此类水体的健康状况[20]。
相较于传统生物指标,在河流生态系统健康评价研究中,微生物群落凭借其独特的生物学特性,正逐步成为备受关注的研究对象。微生物在物种多样性方面具有显著优势,且能更敏锐地响应所处生境的变化[21]。研究表明,微生物群落多样性和丰度与水生生态系统的健康程度高度相关,其结构和功能会对水质变化做出动态响应[22-23]。在受到强烈干扰的情况下,微生物群落虽发生改变,但并未出现明显的多样性损失[24],这些特性为其作为生态健康评价指标奠定了坚实的理论基础。
微生物群落理论背景与技术的发展,使得微生物生物完整性指数(Microbial Index of Biotic Integrity,M-IBI)的提出与应用在实际应用中展现出多方面的潜力:首先,微生物群落对环境变化的响应速度远超传统生物指标(如鱼类、大型底栖无脊椎动物等),能够精准且迅速地捕捉到短期污染波动情况[21],这使M-IBI具有更高的准确性与灵敏性;其次,微生物凭借其广泛的环境适应性和高丰度特征,即便在受到严重干扰的水体环境中,依然能够保持稳定的群落结构,这一特性有效弥补了传统生物指标在低多样性环境中的失效问题[25],为M-IBI在不同环境下的广泛应用奠定了基础;再者,随着测序技术的不断革新与广泛应用,Illumina高通量测序技术的应用使微生物数据的获取变得更加高效和全面,为M-IBI的动态监测与精准评估提供了强有力的技术支撑[26-27]。Wang等[26]的研究表明,在受人类活动强烈干扰的城市湖泊进行健康状况评价时,底栖生物完整性指数(Benthic Index of Biotic Integrity,B-IBI)与水质无显著相关关系,而M-IBI与水质呈显著正相关关系,这表明M-IBI在反映实际水质情况时具有更高的敏感性。苏瑶等[28]通过高通量测序技术成功构建了M-IBI评价体系,并将其应用于河流水生态系统的健康评价中,其结果与水质状况基本吻合。孙瑶等[29]也通过构建M-IBI评价体系对上海松江区4条河道生态系统的健康状况进行评估,有效反映了生态修复后河流水质的变化情况。以上研究均证明了M-IBI的广泛适用性,然而,现有研究多集中于湖泊或大型河流[22, 30],针对城镇河流的研究仍较为缺乏。城镇河流具有水文波动剧烈、污染物来源复杂的特点[3, 31],传统IBI方法因生物群落多样性受干扰显著减少而难以适用。因此,本研究以乐山市茫溪河为例,旨在构建适用于城镇河流的M-IBI评价体系,为高干扰环境下的河流健康监测提供新方法。
HTML
-
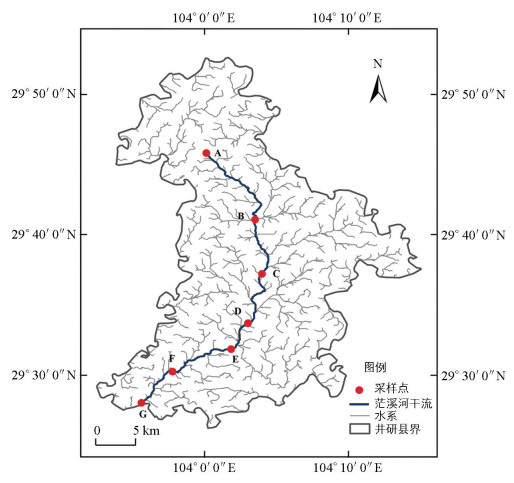
选取四川省乐山市井研县境内的茫溪河干流(29°27′~29°44′N,103°55′-104°05′E) 为研究对象。茫溪河是岷江下游左岸的一级支流,在井研县境内的流域面积为663 km2,河长75.0 km,河宽30~50 m,多年平均径流量3.53 m3/s。水资源主要依靠降水补给,径流量季节变化显著,是井研县的主要河流。该县的重要城镇、工业以及农业发展区主要沿其干流两岸分布。根据茫溪河的自然环境特征及城镇分布情况,在水源地(A)、沿线主要城镇交汇处(B~F)以及出境断面(G)共设置了7个采样点,具体分布位置如图 1所示。
-
于2022年9月(丰水期)和2023年1月(枯水期)对水样进行采集,每个点位采集3份水样混合后取6 L水样作为最终样品,置于灭菌密封聚乙烯塑料瓶中。丰水期水样标记为AF~GF,枯水期水样标记为AD~GD。将水样运回实验室后,取其中1 L水样,参照《地表水环境质量标准》(GB 3838—2002)对以下水质指标进行分析测定:高锰酸盐指数(CODMn)、化学需氧量(CODCr)、氨氮(NH3-N)、总氮(TN)、总磷(TP)。另外5 L水样,每1 L使用0.22 μm的微孔滤膜抽滤形成一个样品(包括3个平行样和2个备份),抽滤后的滤膜置于10 mL灭菌离心管中,保存在-80 ℃冰箱中,用于后续高通量测序。此外,使用手持式多参数高精度水质测定仪(TE-1800)现场测定pH、水温(T)、溶解氧(DO)、电导率(EC)、浊度(FTU)等水质参数。
-
采用TIANamp Soil DNA Kit试剂提取盒对各采样点位水样中的微生物DNA进行提取。按照说明书操作,使用1%琼脂糖凝胶电泳检测提取的DNA片段,并通过分光光度计测定DNA的质量和纯度(OD260/OD280)。本次高通量测序的目标区域为515FmodF_806RmodR,引物为515FmodF(GTGYCAGCMGCCGCGGTAA),806RmodR(GGACTACNVGGGTWTCTAAT)。
DNA提取、高通量测序均由上海美吉生物医药科技有限公司完成,微生物数据分析在美吉生物云平台(www.majorbio.com)进行,折线图和箱线图使用Origin 2022绘制。
-
参考点应选择不受人为干扰的原始状态的点位,但茫溪河作为井研县的主要河流,该县的生产生活主要位于茫溪河周边,很难找到处于理想状态的参考点,于是选择受人为干扰较小的点位作为参考点。参考文献[25, 32],依据《地表水环境质量标准》(GB 3838—2002)对CODMn、CODCr、NH3-N、TN和TP共5项指标进行赋分。各水质参数达到Ⅰ、Ⅱ、Ⅲ、Ⅳ和Ⅴ类标准时,分别计5、4、3、2和1分;未达到Ⅴ类标准的计0分,各水质因子之和即为该采样点的水质总分。参考点设置参考文献[27],将水质总分大于75%分位数的点位设为参考点,其余采样点设为受损点。
-
冗余分析(Redundancy Analysis,RDA)和典范对应分析(Canonical Correspondence Analysis,CCA)均可用于微生物群落组成与环境因子之间的关联分析[33-35]。先用species-sample数据进行去趋势对应分析(Detrended Correspondence Analysis,DCA),如分析结果中梯度长度的第一轴小于3.5则选择RDA,反之则选择CCA。在绘制RDA/CCA结果图后,通过图中箭头的方向和长短来判断每个环境因子对微生物群落组成的影响程度。计算得到envfit分析表,选出具有显著影响的环境因子。
-
参考文献[27, 36-38],选取以下指标作为候选指标:多样性指标、群落组成指标和耐受性/敏感性指标。其中,多样性指标包括Ace、Chao、Shannon、PD、Sobs等α多样性指数;群落组成指标为优势物种的相对丰度,以及部分具有代表性的细菌群落的相对丰度;耐受性/敏感性指标主要为与相关环境因子呈正/负相关菌群的相对丰度。
确定候选指标后,采用箱线图和相关性分析对相关指标进行筛选。筛选过程参考文献[21],首先,通过箱线图比较各候选指标在区分参考点和受损点方面的能力(四分位距(Interquartile Range,IQ)≥2,即两箱体无重叠或有重叠但中位线不在对方箱体内),筛选出具有代表性的候选指标;其次,对选出的指标进行Pearson相关性分析,若两候选指标间的相关系数|R|≥0.7且p<0.05,则认为两指标具有显著相关性,并保留其中一个指标。
-
参考文献[28, 30, 39],将筛选得到的核心指标构建为M-IBI评价体系。采用比值法对核心指标进行赋分,指标值的计算公式如下:当指标值随着干扰的增强而增大时,M-IBI得分=(最大值-点位值)/(最大值-5%分位数);当指标值随着干扰的增强而减小时,M-IBI得分=点位值/95%分位数。最终,M-IBI得分为各项指标得分之和。该方法计算得到的M-IBI值范围为0~1,若结果大于1,则记为1。将各采样点的M-IBI得分按从大到小排序,以95%分位数作为健康状态的评价阈值,M-IBI得分高于该阈值的采样点视为健康状态;将低于95%分位数的分布范围五等分,分别划分为健康、亚健康、一般、较差和极差状态。
1.1. 研究区域概况与采样点设置
1.2. 样品采集与分析
1.2.1. 样本采集与水质分析
1.2.2. Illumina高通量测序
1.3. M-IBI体系的构建
1.3.1. 参考点的选择
1.3.2. 环境因子的确定与筛选
1.3.3. 微生物参数的确定与筛选
1.3.4. 评价标准及指标得分
-
根据1.3节所述的评分标准,对各采样点的CODMn、CODCr、NH3-N、TN和TP进行赋分,综合水质得分为各项水质参数得分的总和,结果见表 1。各点位综合水质得分范围为9~23,其中综合水质得分的75%分位数为17,选取综合水质得分≥17分的位点为参考点,即设置AF(丰水期)和AD(枯水期)为参考点,其余位点为受损点。
-
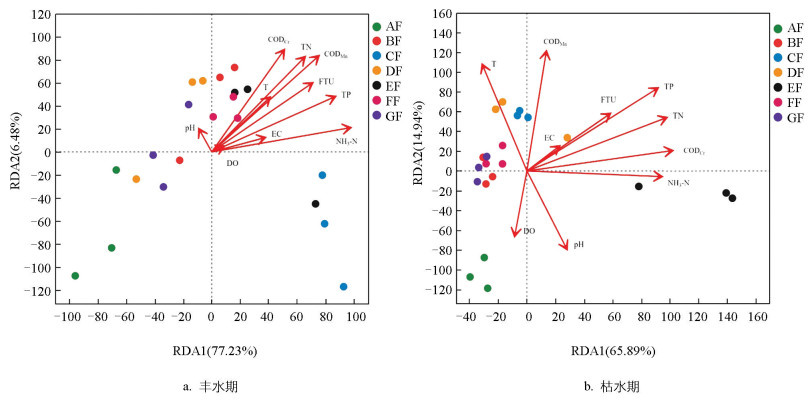
对丰水期和枯水期门层次的微生物群落与水质指标进行RDA分析,结果如图 2所示。丰水期,第一个RDA轴解释了77.23%的优势门的微生物结构变化,第二个RDA轴解释了6.48%的优势门的微生物结构变化,累计解释量为83.71%。Mantel检验表明,CODMn、CODCr、NH3-N、TN和TP与微生物群落分布呈显著相关(0.001<p≤0.01)。枯水期,第一个RDA轴解释了65.89%的优势门的微生物结构变化,第二个RDA轴解释了14.94%的优势门的微生物结构变化,累计解释量为80.83%。Mantel检验表明,pH和FTU与微生物群落呈显著相关关系(0.01<p≤0.05),而T、CODMn、CODCr、NH3-N、TN和TP与微生物群落呈极显著相关关系(p<0.01)。由此推断,影响茫溪河流域微生物群落的关键环境因子为CODMn、CODCr、NH3-N、TN和TP。
-
分析丰水期和枯水期各采样点门分类水平的物种组成情况,结果显示,不同时期茫溪河中的优势菌门均为变形菌门(Proteobacteria),其中,丰水期占比为38.74%,枯水期占比为27.88%。其次,丰水期占比较高的还有厚壁菌门(Firmicutes,34.97%)和拟杆菌门(Bacteroidota,11.47%);枯水期占比较高的门有放线菌门(Actinobacteriota,20.88%)和蓝细菌门(Cyanobacteria,16.25%)。
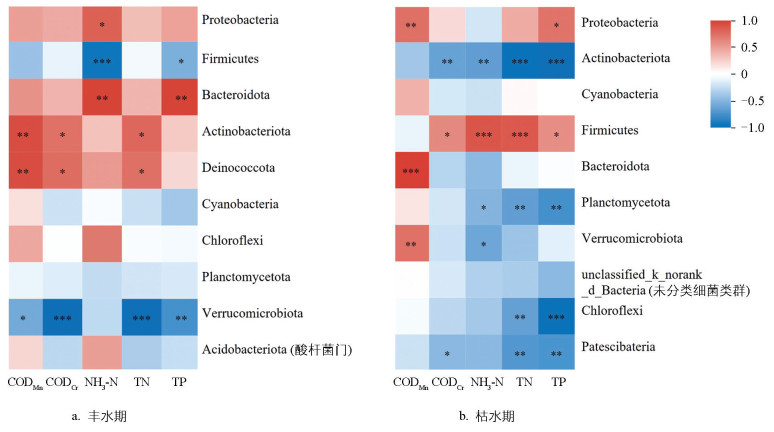
进一步分析关键环境因子与两个时期前10优势门微生物群落之间的相关性(图 3),结果表明:在丰水期,前10优势门中的变形菌门、厚壁菌门、拟杆菌门、放线菌门、奇异球菌门(Deinococcota)和疣微菌门(Verrucomicrobiota)与CODCr、CODMn、NH3-N、TN和TP的相关性较强;在枯水期,前10优势门中的变形菌门、放线菌门、厚壁菌门、拟杆菌门、浮霉菌门(Planctomycetota)、疣微菌门、绿弯菌门(Chloroflexi)和髌骨细菌门(Patescibacteria)与上述环境因子的相关性较强。
综合两个时期环境因子与前10优势门微生物群落之间的相关性,将变形菌门、厚壁菌门、拟杆菌门、放线菌门和疣微菌门的相对丰度指标纳入微生物完整性指数的候选指标。
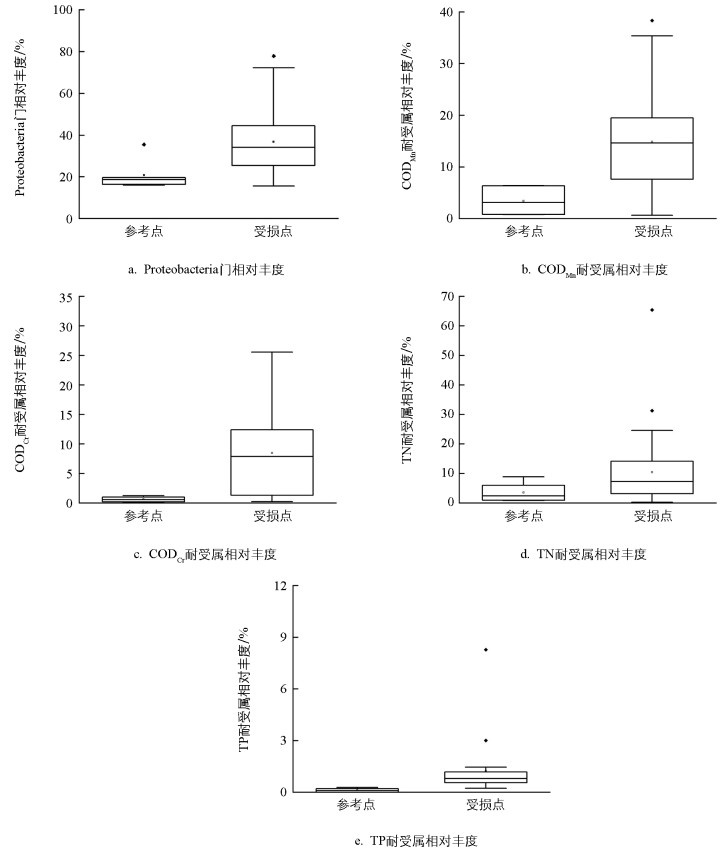
在此之外,进一步选用能够反映河流微生物群落多样性、功能微生物群落的指标作为候选生物参数,共确立了20个备选指标(表 2)。分析所有指标对干扰的判别能力,通过箱线图筛选出符合要求的5项指标(图 4);对这5项指标进行Pearson相关性分析,选取相关性系数绝对值均小于0.7(表 3)的指标,最终获得用于计算M-IBI的4项指标:Proteobacteria门相对丰度、CODMn耐受属相对丰度、CODCr耐受属相对丰度、TP耐受属相对丰度。
-
计算4个筛选出的指标对应的M-IBI分值,相加后获得各采样点的M-IBI总分,以此为基础建立茫溪河M-IBI指标的河流生态系统健康评价标准(表 4),并评估各采样点的健康状况(表 5)。结果显示,丰水期:1个点位健康状况为健康,5个为亚健康,1个为一般;枯水期:4个点位健康状况为健康,1个为亚健康,2个为一般。与丰水期相比,枯水期健康状况为健康的点位比例更高,整体健康状况更好;河流中游(B点~F点)的健康状况略差于上游(A点)和下游(G点)。
2.1. 参考点的选择
2.2. 环境因子的确定与筛选
2.3. 生物参数的确定与筛选
2.4. 评价结果
-
对茫溪河7个采样点的7个水质指标测定数据进行分析(表 1),结果表明pH、T、DO、CODMn、NH3-N、TN、TP浓度在枯水期的波动小于丰水期,说明该河流水体的稳定性在枯水期较高。这与枯水期处于冬季,冬季气温较低,降水量也更小有关,气温和降水量会对河流水体的稳定性产生间接影响[40]。另外,水质指标在空间维度上也存在明显差异,A点CODMn、CODCr、TN、TP的浓度在丰水期和枯水期均远低于其余点位。这一差异可能源于A点为水源地,周边居住人口少,其余点位附近为中小型城镇聚居地,常住人口较多,且分布有少量工业园区,人类活动对河流水质影响较大。因此,人类生产生活是该河流水环境因子在不同河段存在明显差异的主要影响因素。
-
Illumina高通量测序技术能够高效、全面地揭示微生物群落结构,实现对微生物的时空动态监测。因此,相较于传统生物指标(如鱼类、大型底栖无脊椎动物等),利用该技术监测微生物群落所获得的数据不仅能揭示生态系统的动态变化机制,还能提供更丰富的研究数据。基于此构建的M-IBI能够更准确地评价受干扰河道的健康状况。例如,张迪涛等[30]使用Illumina高通量测序技术构建了M-IBI,对武汉市东西湖区5个湖泊的生态系统健康状况进行评价,综合考虑了多种环境因子与水生微生物的相关性,有效区分了不同受损湖泊水生态系统的健康状况。董婧等[41]也采用相同方法评价了北京市城市河道的生态健康,其评价结果能够明显区分以自然水体和再生水厂作为补水的不同城市河道。同时,由于Illumina高通量测序技术产生的数据量极为庞大,基于该技术的M-IBI评价虽已应用于湖泊、河流、湿地、地下水等生态系统的健康评估,但在分析过程中可能因方法和参数选择的不同而导致结果偏差。因此,针对相同类型的生态系统,需要更多参数和应用实例对评价体系进行进一步优化和验证,以更准确地反映水体的健康状况。
本研究通过Illumina高通量测序技术获取了河流水体中的微生物相关数据信息,构建了M-IBI体系对城镇河道健康状况进行评估。评估结果与河流周边实际环境条件基本吻合,具体表现为:受人为干扰因素最小的A点健康状况较好,枯水期河流的健康状况优于丰水期。结果表明,M-IBI能有效区分不同健康状态的水体,为城镇河流健康诊断提供量化依据。
-
微生物对环境的变化往往具有较高的敏感性,环境变化会导致微生物群落组成和分布发生变化[42-43]。不同污染程度的水体中微生物群落组成差异显著,因此可通过监测微生物群落的变化来推断河流生态系统健康状况的变化[26, 44-46]。
优势菌门的变化对于河流水质的变化往往能起到较好的指示作用。在本研究中,变形菌门、放线菌门、厚壁菌门、拟杆菌门和疣微菌门在丰水期与枯水期均具有较高的相对丰度。其中,变形菌门在大多数养殖废水、湿地及沉积物环境中均为优势菌门[47-49],且被广泛认为是天然水体中抗生素抗性基因(Antibiotic Resistance Gene,ARG)的主要宿主之一[50]。该门类下的部分细菌还拥有自养与异养等多种代谢方式,因而生存能力更强[51-52]。变形菌门因其较强的适应性和对水体中污染物变化的高度敏感性,常被用作淡水细菌的指示剂,反映水体的污染程度[53-54]。厚壁菌门具有坚韧的细胞壁,耐受性较高,它可以降解包括药物在内的多种复杂有机化合物,从而更好地适应受药物影响的环境[55-56]。该菌门还能适应厌氧和高营养环境,常见于污水处理系统,在进水阶段为优势菌群,对水体的污染程度也具有一定的指示作用[31, 57]。放线菌门和拟杆菌门大多为异养菌,能够通过产生一系列酶至细胞外的方式分解和利用复杂的大分子有机化合物[58-59]。黄小兰等[60]的研究表明,在赣江下游河湖交错带中,放线菌门的丰度与Cu、Pb的浓度呈正相关,拟杆菌门与Hg含量呈正相关;张健[61]、褚奇奇[62]、朱小杰[63]等的研究也表明,放线菌门和拟杆菌门对重金属污染具有较高的敏感性。疣微菌门在有机物分解和氮循环中发挥重要作用[64],Sha等[65]的研究表明,疣微菌门的丰度与Cd和Pb的浓度呈正相关。由图 3可知,上述4种菌门相对丰度较高,与环境因子相关性显著,且均参与了河流生态系统的循环,因此可作为河流生态系统健康状况的指示菌群。
-
1) 本研究构建了包含Proteobacteria门相对丰度、CODMn耐受属相对丰度、CODCr耐受属相对丰度、TP耐受属相对丰度4个关键评价指标的M-IBI体系,证实其在城镇河流健康监测中具有适用性。结果显示,茫溪河整体处于“健康—亚健康”状态,枯水期健康水平优于丰水期;中游(B点~F点)由于受人类活动影响显著,其健康水平明显低于上游(A点)和下游(G点)。这一结果验证了M-IBI对空间异质性和季节性波动具有高敏感性。
2) 与传统IBI评价体系相比,M-IBI充分利用微生物群落多维响应的特性,解决了城镇河流生物单一性导致的评价盲区问题。该体系不仅为城镇河流健康评价提供了更为全面和精准的视角,同时也为高干扰水体的动态监测开辟了新的思路与方法,为相关领域的研究和实践提供了重要的理论支持和技术支撑。
3) 本研究虽然成功构建了适用于城镇河流的M-IBI评价体系,为其分级分区管理提供了更为准确的动态量化监测工具,但是鉴于环境因子与微生物功能之间关联机制的复杂性,尚未对其开展量化解析。后续研究可结合宏基因组学技术,进一步探究污染胁迫下微生物的代谢机制,从而为M-IBI体系赋予更丰富的生物学内涵。此外,为推动M-IBI体系向标准化和通用化方向发展,后续研究可通过扩大样本范围,在不同区域和不同类型水体中验证其评价效能,进一步增强该体系在城镇河流健康评价中的普适性,为高干扰水体的生态监测提供更坚实的理论与技术支持。





 DownLoad:
DownLoad: