-
开放科学(资源服务)标识码(OSID):

-
Cpx双组份调控系统(以下简称Cpx系统)广泛存在于细菌中,由内膜组氨酸激酶CpxA及胞质反应调节剂CpxR组成[1],当细菌面临复杂环境应激时,位于其内膜上的CpxA因子发生自磷酸化,将磷酸基团转移到CpxR,促使CpxR蛋白磷酸化,磷酸化的CpxR可作为转录激活因子,从而调控下游相关基因的转录,帮助细菌适应不利环境。cpxA/R基因的缺失,对多数细菌的毒力及其在多种环境刺激下的耐受性及存活具有重大影响[2-5],因此,有研究利用Cpx系统(cpxR/lon)缺失导致的菌株毒力下调制成减毒活疫苗,以此抵御野毒株感染[6]。从另一个角度来看,CpxA/R本身也可作为一个可调控的靶标分子,通过外在因子对其激活或失活,从而达到控制细菌生长的目的。
基因组信息分析发现,多杀性巴氏杆菌中也存在Cpx系统,但目前作用并不清楚,需进一步研究。多杀性巴氏杆菌作为一种重要的人畜共患细菌性病原,传染性强,发病率、死亡率较高[7],目前对其防控主要依靠抗生素,但过多抗生素使用会加剧多杀性巴氏杆菌耐药株的产生,因此需要更多行之有效的方法。本课题组前期通过基因编辑手段,发现多杀性巴氏杆菌部分基因缺失能显著降低菌株毒力,并赋予了菌株较好的交叉免疫保护特性[8-9]。基于对Cpx系统在其他细菌中功能的了解,本研究选择了多杀性巴氏杆菌Cpx系统进行研究,旨在通过同源重组方法实现多杀性巴氏杆菌中cpxA基因和cpxA/R双基因的缺失,探讨Cpx系统基因缺失对菌株毒力、交叉保护性及环境应激耐受等方面的影响,为多杀性巴氏杆菌的有效防控提供新的依据。
HTML
-
昆明小鼠(雌性、18~22 g)、C57BL/6小鼠(雌性、18~22 g)购自湖南斯莱克景达实验动物有限公司,动物饲喂及相关实验操作均由西南大学实验动物伦理审查委员会批准(批准号:IACUC-20210715-03)。牛源A型、B型、F型多杀性巴氏杆菌(PmCQ2,PmB,PmF)、猪源A型多杀性巴氏杆菌(PmP)及禽源A型多杀性巴氏杆菌(PmQ),暂存于西南大学动物医学院肉牛疫病防控研究室。小鼠肺泡上皮细胞系存于西南大学动物医学院肉牛疫病防控研究室。用于构建基因缺失株的载体pUC19oriKanR由实验室前期构建并保存。
-
卡那霉素、甲酰胺、DMSO、MTT,上海生工生物工程有限公司;马丁肉汤培养基、脑心浸液肉汤培养基(20211109),青岛海博生物技术有限公司;透明质酸、结晶紫染料,Solarbio公司;琼脂糖、透明质酸酶、脱脂奶粉,BioFroxx公司;BamH Ⅰ、Hind Ⅲ限制性核酸内切酶,宝生物(大连)工程有限公司;2×Taq PCR Mix,Vazyme公司;药敏纸片,杭州微生物试剂有限公司;Stains-All,BBI公司;氯化钠、氯化钾、果糖、葡萄糖、氯化铁、氯化镁、氯化钙、硫酸铜(分析纯),北京科隆生物技术有限公司;FeSO4·7H2O(分析纯),Alladin公司;硫酸鱼精蛋白,上海源叶生物科技有限公司;DMEM、1640培养基、PBS缓冲液、0.25%胰蛋白酶,Gibco公司;TMB显色液,Beyotime公司;HRP标记羊抗鼠IgG、Mouse IL-12、TNF-α、IFN-γ ELISA Kit,Thermo公司;细菌RNA提取试剂盒,北京天漠科技开发有限公司;改良型Bradford蛋白浓度测定试剂盒,Sangon公司。
-
本研究中基因缺失株的构建参照实验室前期hyaD基因缺失株的构建方法[9],即通过设计cpxA及cpxR基因的上下游同源臂引物,PCR扩增分别获得各自基因上下游同源臂,融合上下游同源臂后连接到pUC19oriKanR基因缺失载体上。选择牛源A型多杀性巴氏杆菌CQ2株(PmCQ2),首先对其cpxA基因进行缺失,其后对PmCQ2-ΔcpxA进行cpxR基因缺失,基因的缺失验证采用DNA水平及转录水平检测。缺失株构建及验证所用引物见表 1。
-
吸取1 mL处于对数生长期的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液,13 400 r/min离心15 min,弃上清,PBS洗2次,最后用1 mL无菌PBS重悬菌体,将上述液体置于42 ℃金属浴中处理1 h (处理前后均吸取100 μL进行稀释涂板计数)。剩余菌液13 000 r/min离心20 min,吸取100 μL上清液加入到900 μL荚膜染色液中混匀,测定OD630值。同时配制不同浓度梯度的透明质酸标准溶液(每100 μL含0、1、3、5、10 μg),分别吸取100 μL加入到900 μL荚膜染色液中,测定OD630值绘制标准曲线。根据标准曲线计算各菌株的荚膜多糖含量,每组设置3个重复。
-
使用BHI培养基将计数后的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液稀释至1×108 CFU/mL,吸取400 μL到48孔细胞培养板中,以BHI培养基作阴性对照,置于37 ℃恒温培养箱中培养48 h。将培养基吸净,每孔加入200 μL无水甲醇固定1 h,吸出甲醇固定液,用PBS洗3次,室温晾干1 h;随后每孔加入200 μL 1%结晶紫,于37 ℃处理1 h,吸出结晶紫染液,PBS洗3次,室温晾干1 h;每孔加入200 μL 33%冰乙酸,37 ℃处理30 min,测定OD630值,每组设置3个重复。
-
将处于对数生长期的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液浓度调整为1×109 CFU/mL,吸取1 mL菌液至100 mL马丁肉汤培养基、LB肉汤培养基、脑心浸液肉汤培养基、牛肉膏蛋白胨液体培养基中,置于37 ℃振荡培养箱中培养14 h,每组设置3个重复,每2 h取样测定OD600值,绘制生长曲线。
-
接种约5×104个/孔小鼠肺泡上皮细胞到96孔细胞培养板中,放于37 ℃、5% CO2培养箱中贴壁2 h。以1 MOI PmCQ2、PmCQ2-ΔcpxA、PmCQ2-ΔcpxAΔcpxR以及实验室前期构建的毒力显著降低的PmCQ2-ΔqseCΔluxS感染细胞,于37 ℃、5% CO2的培养箱中处理12 h,吸出上清,PBS洗2次,之后每孔加入100 μL DMEM培养基和20 μL MTT溶液(5 ng/mL),继续放入培养箱中培养4 h,弃上清,每孔加入100 μL DMSO溶液,于水平摇床上避光处理10 min,测定OD570值,进行细胞毒性的比较。
-
将处于对数生长期的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液浓度调整为4×106 CFU/mL,将18只昆明小鼠随机分为3组,每组6只,每只注射100 μL上述菌液,进行肌肉攻毒。12 h后眼球采血,解剖小鼠,分离肺脏、肝脏、脾脏,将组织称量后,加入1 mL无菌生理盐水,匀浆并稀释涂板计数,计算脏器定殖量。
-
接种2×104个/孔小鼠腹腔原代巨噬细胞到48孔细胞培养板中,以“+”晃动,于37 ℃、5% CO2培养箱中贴壁2 h,吸出上清,PBS洗3次,以1 MOI PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液感染细胞,于37 ℃、5% CO2培养箱中处理6 h。感染结束后,收集细胞上清液,按照IL-12、TNF-α、IFN-γ炎性因子ELISA试剂盒说明书测定其分泌量。
-
吸取1 mL PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液,转接至100 mL马丁液体培养基中,于37 ℃振荡培养箱中培养至对数生长期,进行稀释平板计数后,将菌液13 400 r/min离心15 min后,加入适量PBS重悬菌体。在重悬菌液中加入0.15%甲醛溶液,充分混匀后置于37 ℃灭活24 h,每6 h涡旋振荡1次。灭活后的菌液、无菌PBS分别与15 VG矿物油佐剂以4∶1的比例混匀,制成5×109 CFU/mL PmCQ2-ΔcpxA、PmCQ2-ΔcpxAΔcpxR灭活苗和PBS乳化剂。将灭活苗涂布于马丁固体培养基中,37 ℃培养箱培养24 h,检测其是否灭活完全。在进行安全性评价后,保存于4 ℃冰箱。
将90只昆明小鼠随机分为15组,每组6只,免疫接种程序和攻毒情况见表 2。加强免疫7 d后对各组进行肌肉攻毒,根据各菌株的半数致死量(LD50)及课题组前期研究,将菌株浓度调整为PmCQ2:5×108 CFU/mL,PmB:1×108 CFU/mL,PmF:5×109 CFU/mL,PmP:100 CFU/mL,PmQ:100 CFU/mL,每只小鼠注射100 μL菌液,每12 h观察1次,连续观察1周,记录小鼠死亡情况。
-
根据灭活苗交叉免疫保护性的评价结果,仅测定针对牛源A型多杀性巴氏杆菌抗原的抗体消长规律,将12只昆明小鼠随机分为2组,每组6只,按照表 2对小鼠进行免疫。免疫结束后,尾静脉采血,之后每隔30 d,进行1次尾静脉采血,连续观察150 d,测定血清抗体效价,绘制抗体消长曲线。
-
将处于对数生长期的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液浓度调整为1×109 CFU/mL,吸取100 μL菌液至马丁固体培养基中,涂布均匀后,用无菌镊子夹取药敏片贴于培养基上,每组3个重复。将贴好药敏片的培养基,置于37 ℃恒温培养箱中培养12 h(无需倒置),测定抑菌圈直径,判断菌株对抗生素的敏感性。
-
将处于对数生长期的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液浓度调整为1×109 CFU/mL,吸取100 μL菌液到100 mL马丁液体培养基(含200 mmol/L NaCl、200 mmol/L KCl、4%葡萄糖、4%果糖、pH值为8.5)中,于37 ℃或特定温度的振荡培养箱中培养14 h,每组设置3个重复,每隔2 h测定OD600值,绘制生长曲线。以同样的方法将其接种至pH值为5.5的马丁液体培养基中,于37 ℃培养,从第8 h开始,每隔1 h测定OD600值,第14 h结束,每组设置3个重复,绘制生长曲线。
-
将处于对数生长期的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR菌液浓度调整为1×109 CFU/mL,吸取50 μL菌液到5 mL马丁液体培养基(含200 μmol/L C2H5O、200 μmol/L H2O2、15 mmol/L FeCl3、5 mmol/L MgCl2、5 mmol/L CaCl2、200 μmol/L FeSO4、5 μmol/L CuSO4)中,每组设置3个重复,于37 ℃振荡培养箱中培养12 h后测定OD600值。
-
采用Graphpad Prism 9.0软件进行数据统计分析,p<0.05为差异有统计学意义。
1.1. 试验材料
1.2. 主要试剂
1.3. 基因缺失株的构建
1.4. 荚膜多糖含量的测定
1.5. 生物膜含量的测定
1.6. 生长曲线的测定
1.7. 细胞毒性的测定
1.8. 脏器定殖量的测定
1.9. 感染小鼠腹腔巨噬细胞炎性因子分泌能力的比较
1.10. 灭活苗的制备及交叉免疫保护性评价
1.11. 抗体消长规律的测定
1.12. 药敏试验
1.13. 不良环境下生长曲线的测定
1.14. 其他模拟环境中生长状况的观察
1.15. 数据统计分析
-
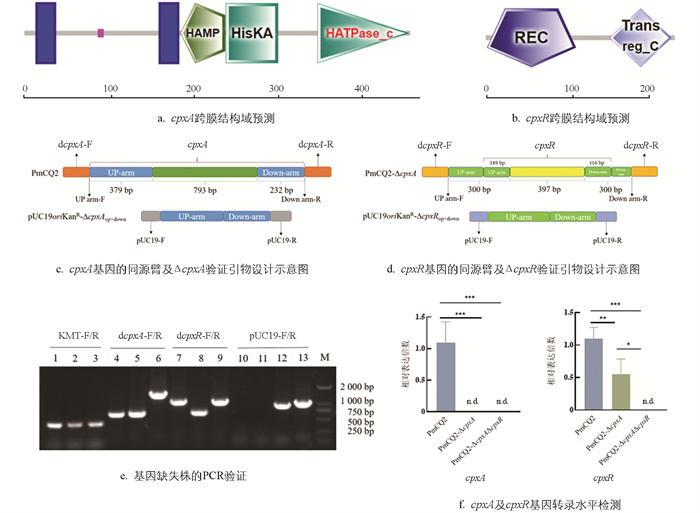
Cpx系统对多数革兰氏阴性菌的毒力、耐药性及环境响应能力等具有显著影响,但其在多杀性巴氏杆菌(Pm)中的作用尚未揭示。本研究选择实验室前期分离到的一株强毒荚膜A型多杀性巴氏杆菌菌株PmCQ2,对其Cpx系统基因进行缺失。根据PmCQ2全基因组测序结果,利用在线分析软件SMART对其CpxA和CpxR蛋白结构域进行分析(图 1)。
由图 1a可知,cpxA基因全长1 404 bp,其中15~37 aa、164~186 aa为跨膜域,89~96 aa为低度复杂区域,189~243 aa为HAMP信号转导域,244~307 aa为HisKA结构域,355~465 aa为HATPase_c结构域。cpxR基因全长702 bp,编码蛋白的2~111 aa为CheY同源接收域,153~229 aa为组氨酸激酶的信号接受域(图 1b)。对CpxA部分结构域(核酸序列区段为379~1 172 bp)进行缺失,筛选获得PmCQ2-ΔcpxA(图 1c);其后对该缺失株中的CpxR部分结构域(核酸序列区段为189~586 bp)进行缺失,筛选获得PmCQ2-ΔcpxAΔcpxR(图 1d),从DNA层面(图 1e)及RNA转录层面(图 1f)检测验证,缺失株构建成功。
-
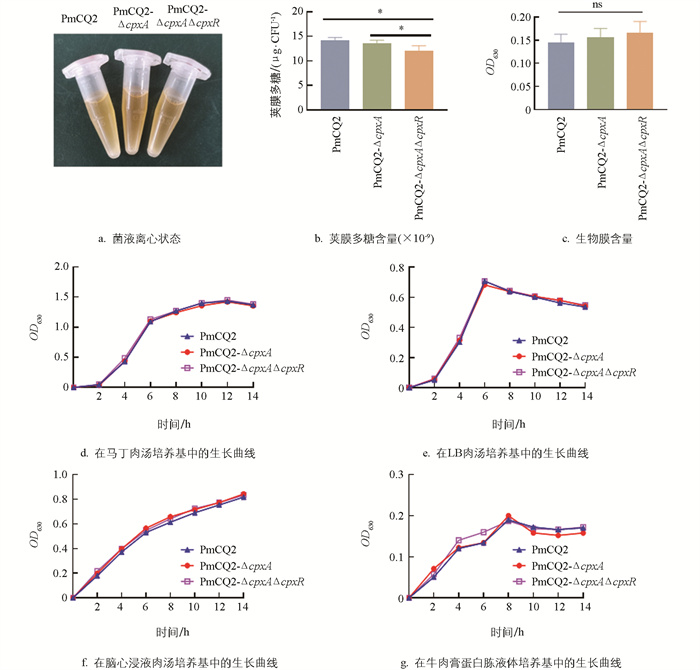
为探究Cpx系统基因缺失对Pm生物学特性的影响,本研究对菌液离心状态进行观察,发现Cpx系统基因缺失并不会对菌体的离心状态产生影响(图 2a),但在荚膜多糖产生方面,cpxA/R双基因的缺失能显著降低菌株的荚膜多糖(图 2b)。有研究发现Pm具有荚膜多糖含量与生物膜含量呈反比的特点[9],测定缺失株与野生株生物膜发现,3株菌株间差异无统计学意义(图 2c),同时该系统基因的缺失也并不会影响菌株在多种培养基中的生长速度(图 2d-2g)。
-
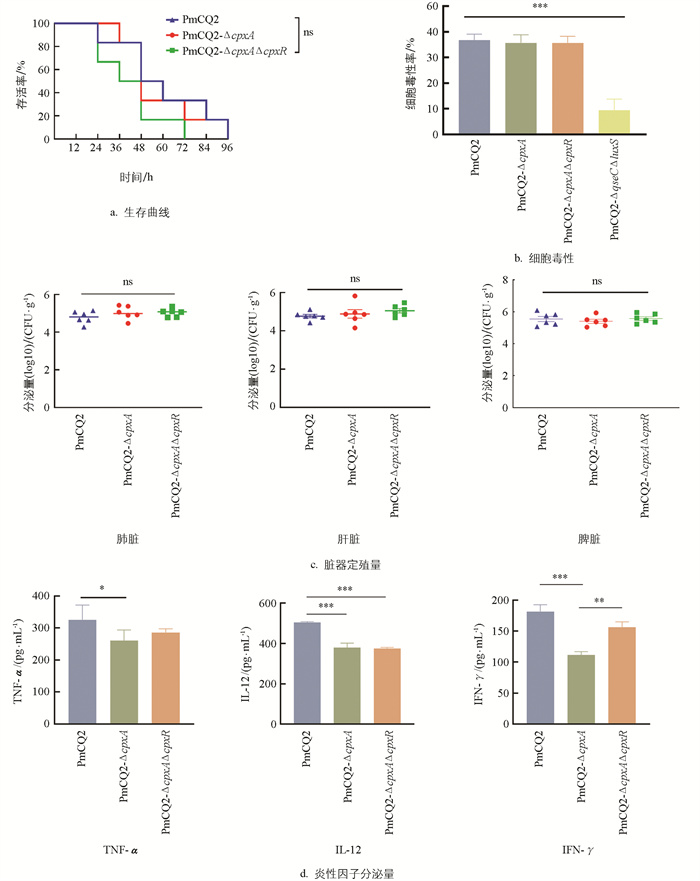
分别以相同剂量的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR通过肌肉途径感染小鼠,3株菌株导致小鼠死亡的速率差异无统计学意义(图 3a)。
采用小鼠肺上皮细胞来测定各菌株的细胞毒性作用,并以另一个双基因缺失株PmCQ2-ΔqseCΔluxS为参照,发现Cpx系统基因缺失株对细胞的毒性和野毒株间差异无统计学意义,但显著高于PmCQ2-ΔqseCΔluxS(图 3b)。
以4×106 CFU/mL的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR肌肉攻毒感染小鼠,发现感染12 h后小鼠肺脏、肝脏、脾脏中的载菌量差异无统计学意义(图 3c)。
以1 MOI的PmCQ2、PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR感染小鼠腹腔巨噬细胞,6 h后收集细胞上清,用ELISA试剂盒检测巨噬细胞分泌炎性因子的情况发现,与野生株相比,PmCQ2-ΔcpxA感染显著降低了细胞TNF-α、IL-12、IFN-γ相关炎性因子的分泌量,而PmCQ2-ΔcpxAΔcpxR感染显著降低了细胞IL-12的分泌量(图 3d)。
-
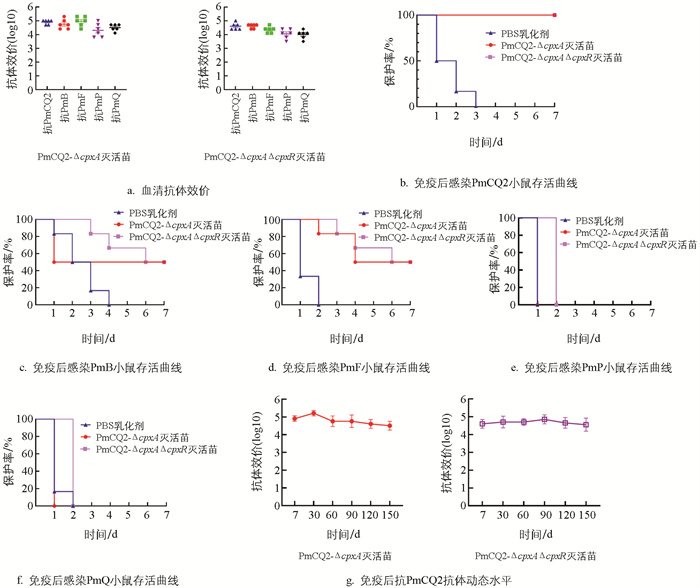
前期发现,部分基因缺失会赋予多杀性巴氏杆菌的交叉免疫保护特性[8-9],为探究cpxA/R基因缺失是否会同样赋予Pm菌株交叉免疫保护能力,我们通过制备野毒株和基因缺失株灭活苗,同时以PBS乳化剂为对照,分别免疫小鼠,首免14 d后加强免疫1次,首免21 d后进行尾静脉采血并分离血清,检测抗体水平的产生情况,随后对小鼠进行攻毒测试。结果发现,cpxA及cpxA/R基因缺失株灭活苗均能诱导小鼠产生较高的抗体水平(图 4a),两个基因缺失株灭活苗对牛源A型Pm的保护率为100%,对牛源B型、F型Pm的保护率为50%,但对猪源、禽源A型Pm无保护性(图 4b-4f)。用这两个基因缺失株灭活苗免疫小鼠后,其抗体水平可达1∶25 600~1∶102 400,并能稳定维持150 d以上(图 4g)。
-
有研究表明,Cpx系统主要通过对下游因子的调节帮助细菌适应自然环境中的各种应激,从而维持其自身的生存能力[2-5]。本研究发现,PmCQ2-ΔcpxA和PmCQ2-ΔcpxAΔcpxR对绝大多数抗生素敏感性差异无统计学意义,但对氨苄西林的敏感性显著增加(表 3)。
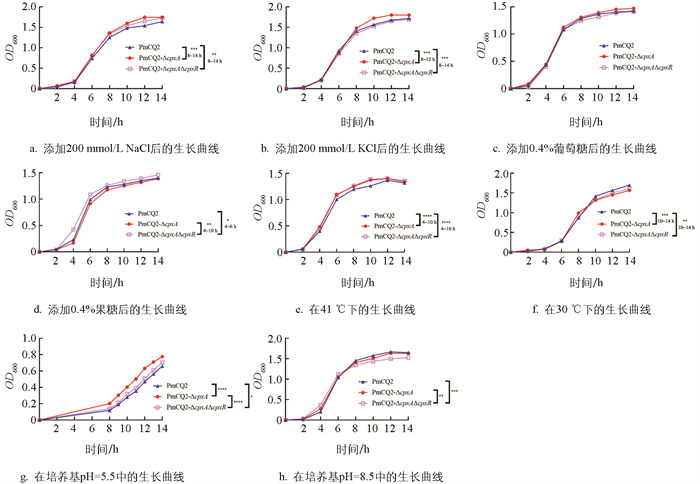
为进一步探究Cpx系统基因对Pm应对环境刺激能力的影响,通过在培养基中添加不同的刺激因子或改变培养条件,模拟各种应激环境测试基因缺失株的生长情况。结果显示:在添加盐离子及糖的环境中,基因缺失株仅对高浓度Na+、K+离子的添加有所响应,Cpx系统基因的缺失能促进菌株的生长(图 5a-5d);在温度反应测试中,发现Cpx系统基因的缺失促进了菌株在高温环境中的生长,减缓了菌株在低温环境中的生长(图 5e-5f);在酸碱耐受性方面,Cpx系统基因的缺失促使了菌株对酸的耐受性,降低了菌株对碱的耐受性(图 5g-5h)。
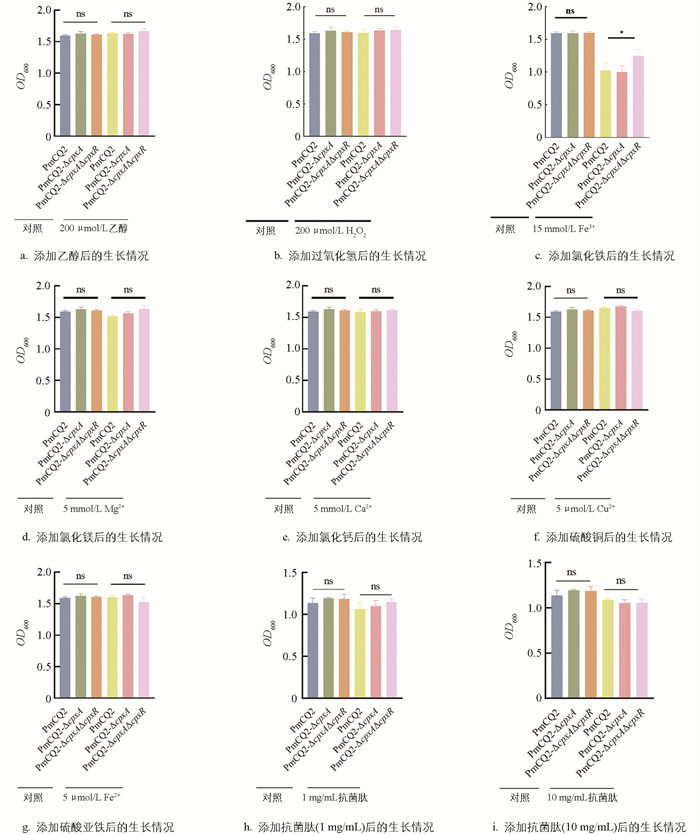
考虑到Cpx通路在其他细菌中能够应对氧化应激、金属离子胁迫及抗菌肽毒性,本研究也在Pm中进行了测试,结果发现,在添加15 mmol/L Fe3+后,3种菌株的生长速度均减缓,PmCQ2-ΔcpxA的生长情况与野生株差异无统计学意义,而PmCQ2-ΔcpxAΔcpxR的生长速度显著高于PmCQ2-ΔcpxA,其余测试差异无统计学意义,说明Cpx系统基因的缺失并未影响到Pm菌株对氧化应激及抗菌肽的敏感性(图 6a-6i)。
2.1. 基因缺失株的构建
2.2. 基因缺失株的生物学特性分析
2.3. 基因缺失对菌株毒力的影响
2.4. 交叉免疫保护性测定
2.5. Cpx系统基因对Pm的环境响应能力的影响
-
鉴于cpxA/R基因对部分细菌毒力、耐药性和应对环境应激等方面的调控,且未有相关报道表明该系统对Pm的影响,因此本研究对cpxA/R基因进行了敲除,但一直未能成功构建PmCQ2-ΔcpxR,课题组也会继续进行构建,以对本研究的相关数据进一步加以论证。另外,在基因敲除的过程中发现,cpxA基因的位点对其功能的发挥至关重要,也有研究发现,cpxA基因某些位点突变或定向缺失,会导致HAMP功能域晶体结构变化,从而对CpxA与CpxP的结合或信号转导产生影响[10-11]。
探究细菌毒力最常用且直观的方法是测定半数致死量(LD50),本研究在前期探索时,测定了PmCQ2和PmCQ2-ΔcpxA的LD50,但二者毒力差异无统计学意义,且PmCQ2的LD50与课题组前期的结果相差100倍左右,我们推测这种差异可能源于攻毒方式的不同。生存曲线结果表明,Cpx系统基因缺失株与PmCQ2毒力差异无统计学意义,仅小鼠死亡时间略微提前。结合这一结果,同时考虑到PmCQ2在感染早期仅发生肺部脏器定殖,因此我们选择测定感染12 h时的脏器定殖量,Pletzer等[12]的研究结果发现,baeR在定殖早期发挥作用,而cpxR在定殖后期发挥作用,这说明时间点的选择有助于揭示Cpx系统在细菌毒力方面的贡献。选择肺上皮细胞进行细胞毒性试验,并将毒力显著降低的PmCQ2-ΔqseCΔluxS作为对照,以证明试验结果的可靠性。结果发现,与野生株相比,PmCQ2-ΔcpxA、PmCQ2-ΔcpxAΔcpxR的毒力差异无统计学意义。在Pm感染过程中,机体通过免疫系统产生高水平的炎性细胞因子,以防御细菌入侵[13];Qiu等[14]研究发现,感染Pm的小鼠肺组织,其炎症因子MCP-1、TNF-α和IL-1β表达均显著上调,高毒力菌株感染所导致的表达水平显著高于低毒力菌株。本研究结果发现,缺失株感染巨噬细胞后,上清中部分炎性因子分泌量降低,我们推测,这可能与细菌荚膜含量不同导致的炎症反应程度变化有关[15]。
敲除沙门氏菌lon和cpxR基因,其菌株毒力显著降低,但却能刺激机体产生更强的免疫反应[6]。本课题组前期研究也发现,多杀性巴氏杆菌某些基因如qseC、hyaD等的缺失,可致使菌株具有较强的交叉免疫保护作用,其中ΔhyaD灭活苗几乎能对本试验所用的攻毒菌株产生完全的保护作用[9],因此,我们探究cpxA/R基因缺失能否发挥与上述菌株相同的作用。由于cpxA/R基因缺失后细菌毒力无显著变化,若制备成活苗,易导致毒力返强,因此将其制备成灭活苗,研究结果表明,灭活苗的交叉保护作用有限,仅对牛源B型、F型多杀性巴氏杆菌具有50%的免疫保护性。我们推测,特定的基因缺失才能赋予菌株良好的交叉免疫保护性。对于这些特定基因缺失后引起的菌株灭活苗保护性发生变化的原因,一方面,基因缺失可能直接影响保护性抗原的表达,从而提升疫苗的保护效果;另一方面,基因缺失后,导致细菌表型改变,使部分抗原裸露在菌体表面更易被识别,进而增强了保护效力。
在发现Cpx系统对牛源A型Pm的生物膜、毒性、抗生素敏感性等方面均无显著贡献时,我们通过在培养基中添加相应因子以模拟外界环境压力,测试cpxA/R基因缺失株的生长情况,从而探讨Cpx系统对这一方面的影响。结果显示,不论是cpxA单基因缺失还是cpxA/R双基因缺失,都显著增加了Pm在模拟酸性环境中的耐受性,这与其他细菌截然不同,如副猪嗜血杆菌cpxR基因缺失后,在酸性、碱性、氧化应激条件下的抗性显著降低[16]。我们从以下3方面对其进行了推测:1) 在课题组构建的多个缺失株中,如ΔqseC、ΔhyaD、ΔqseC、ΔluxS等,大多表现为毒力降低的同时,对环境应激抗性也降低[8-9];在双组份系统相关基因ompR缺失后,毒力与野生株差异不大,但耐酸性显著增加,表现出与本研究的两个缺失株相同的特性。这种共性可能表明双组份系统在Pm中有特殊作用,需进一步研究。2) 不同双组份调控系统在环境应激中的作用机制是复杂的,在本试验中,Cpx系统在酸性和碱性环境中的表现差异很大。有研究表示,大肠杆菌仅在Na+、K+与碱性环境共同存在的情况下,Cpx系统才被激活[17],因此Cpx系统在不同pH下的表现也许与其多样的触发机制有关。3) 测定方法的不同导致的结果差异。冯芬芬[18]发现,副猪嗜血杆菌在0.02 mol/L NaOH处理时,Cpx系统不发挥作用,但在pH为8.5、9.5时,与野生株相比,ΔcpxA差异无统计学意义,但ΔcpxR和ΔcpxA/R耐性显著降低;大肠杆菌的耐酸反应系统,在指数相细胞中,被Fur和PhoP/Q调控因子激活,而在固定相细胞中,被RpoS和OmpR激活[19]。本研究测试的是菌株在改变pH后培养基中的生长情况,并未考虑极性pH胁迫下的细菌存活率。
cpxA/R基因缺失后,铁摄取和转运相关基因表现为上调,但不明显。我们推测,这可能与Cpx系统相关基因缺失对金属离子应激的反应有关,因此在马丁培养基中添加了金属离子进行测试。结果显示,仅在添加15 mmol/L Fe3+时,PmCQ2-ΔcpxAΔcpxR的生长速度显著高于PmCQ2-ΔcpxA,表明cpxR基因对Pm菌株在高浓度铁离子环境下的生长有抑制作用。考虑到宿主对细菌的先天防御限铁策略,我们在马丁培养基中添加了不同浓度的螯合剂2,2'-联吡啶,结果表明,缺失株与野生株间差异无统计学意义。分析其原因,一方面,我们认为细菌通过不同的双组份系统适应应激[20],而在多杀性巴氏杆菌中,Cpx系统可能并非主要的包膜应激反应;另一方面,有研究表明,在限铁条件下,竞争性金属离子的存在,如Cu2+、Zn2+等,会诱导Cpx系统的转录[21],且营养条件的改变也会影响其调控。在大肠杆菌中发现,转铁蛋白的调控依赖于酸性环境诱导的Cpx系统[22]。我们将在后续研究中,通过螯合剂清除培养基中的Fe3+并添加其他金属离子,或组合不同应激条件,以探究Cpx系统是否发挥作用。
Cpx系统在Pm中的表现与其他革兰氏阴性菌不同,cpxA/R基因缺失后的Pm在高温、高渗透压、酸性环境中表现出适应性,在应对氧化应激和抗菌肽处理时无明显反应,仅在对碱应激和低温应激时表现出与其他细菌相似的反应。这种差异性也在霍乱弧菌的研究中被观察到,该研究发现,Cpx系统仅在氯离子添加后被触发[23],证实霍乱弧菌Cpx系统对氯离子的刺激是特异性的。我们推测,在Pm中,该系统的触发机制可能显著异于其他革兰氏阴性菌,且在巴氏杆菌cpxA/R基因缺失株中,可能存在替代的信号转导途径。此外,考虑到牛源A型多杀性巴氏杆菌是重要的呼吸道病原体,在体内主要经受呼吸道气体浓度变化及温度策略的环境压力,因此在试验设计时应注重这方面条件的优化和机制探究。





 DownLoad:
DownLoad: