-
开放科学(资源服务)标识码(OSID):

-
羟基自由基(·OH)是氧化能力最强、反应活性最高的活性氧物种,具有强电负性和高氧化电极电位(2.8 V),可以与绝大部分的生物分子和有机物发生多种不同类型的化学反应[1],在碳和养分循环[2-3]以及污染物降解过程中起着重要作用。针对自然界中·OH的产生,以往的研究多关注于地表光照环境(如大气、地表水和海洋),认为光照/光催化作用是产生·OH的主要机理[4]。近年研究表明,浅层地下黑暗环境也是产生·OH的重要来源[5]。在黑暗环境下羟基自由基的非生物生成途径有两种:第一种是Fe(Ⅱ)诱导的Fenton反应机制,即Fe(Ⅱ)与H2O2反应生成·OH;第二种是有机质中氢醌与半醌引发的·OH的形成[5]。稻田作为典型的湿地,是一个自由基强烈生成的系统,在长期淹水条件下会产生很多还原性物质,在落干遇氧或根泌氧的再氧化条件下,这些还原性物质会被氧化,继而产生·OH[6]。
紫色母岩风化发育的水稻土作为我国西南地区重要的水稻耕作土壤,近年来面临日益严重的酸化问题[7-9]。土壤酸化不仅会导致土壤铝毒害和盐基离子流失等土壤退化现象,还会提高重金属化合物在土壤溶液中的溶解度从而活化有毒重金属[10],对土壤肥力、作物生长发育及农产品质量安全构成严重威胁。研究表明,施加土壤改良剂是改善土壤酸化,提高退化土壤生产力的有效途经[11-14]。施加不同改良剂后,土壤的基本性质(如pH值、有机质质量分数、氧化还原条件)会发生改变[15],进而可能影响·OH的生成速率和产生量,最终调控土壤中养分及污染物的循环。目前,关于不同改良剂对土壤基本性质的改变以及铁元素转化介导的·OH累积量差异的研究仍较为有限,而阐明这一机制对于深入理解酸化紫色水稻土中的养分循环及污染物转化过程具有重要意义。基于此,本研究以不同土壤改良剂处理的酸化紫色水稻土为研究对象,系统探究·OH的表观产量和影响因素,旨在为揭示酸化紫色土环境中·OH在养分循环及污染物转化等过程中的作用机制提供新的角度。
全文HTML
-
酸化紫色水稻土采自重庆市江津区黄庄村,土壤pH值为4.1。样品采集后,过100目筛(去除土壤中大粒径的石块、根系等)备用。本研究选择了5种有机/无机土壤改良剂:水稻秸秆生物炭、猪粪、生物有机肥、海泡石及石灰。盆栽试验在国家紫色土肥力监测基地温室内(30°26′N,106°26′E)完成。其中,水稻秸秆生物炭在600 ℃下烧制而成,pH值为9.3;猪粪经发酵腐熟制成,pH值为7.6;生物有机肥是由芝麻饼和花生饼经好氧发酵复配根际生防放线菌——娄彻链霉菌及枯草芽孢杆菌,并添加腐殖酸生产而成,pH值为8.3;海泡石为含水的镁硅酸盐粘土矿物,具有多孔层状结构和强大的吸附能力,pH值为8.9;石灰主要成分为氧化钙,pH值为12.4。
-
称取土壤5 kg于塑料盆(直径25 cm、高30 cm)中,按照1%的质量比加入上述土壤改良剂,同时设置对照处理(CK,不施加改良剂),每一组处理设置3个重复试验。将土壤与改良剂混匀后,加入自来水,使其处于淹水状态(水层高5 cm左右),平衡2 d后,移栽苗龄一致、长势相近的水稻幼苗。水稻生长期间每日按时浇水,使盆内保持5 cm高的水层。
-
于水稻成熟期采集水土界面的土壤(采样过程中原位测定土壤pH值和Eh值),迅速装入提前充满高纯氮气的采集袋,避免其与空气中的氧气接触,将采集到的样品进行避光处理后立即带回实验室测定相关指标。
-
从采集袋中取7 g鲜土样加入置于厌氧袋中的棕色玻璃瓶中,加入2.8 mL苯甲酸钠(25 mmol/L)溶液,摇匀,随即将样品暴露于空气中,保持避光处理并放置在轨道摇床(220 r/min,25 ℃)上进行氧化培养。取1 mL悬浮液,装进已预加入1 mL甲醇的5 mL棕色玻璃瓶,经0.22 μm膜完成过滤。在预定的时间间隔内(0、1、2、4、6 h)取样并重复上述操作。使用HPLC高效液相色谱仪(岛津LC-20AT)测定生成的对羟基苯甲酸(p-HBA)浓度,并根据公式(1)-(2)计算·OH浓度及·OH生成速率常数。
式中:a·OH为羟基自由基的浓度(μmol/L);bp-HBA为对羟基苯甲酸的浓度(μmol/L)。
式中:kobs,·OH为羟基自由基生成速率常数[μmol/(L·h)];d(Rt2-t1)为t2-t1时间段内羟基自由基生成量的微分。
-
采用光度法测定亚铁质量分数。在厌氧手套袋中称取7 g鲜土样加入棕色玻璃瓶中,之后进行氧化培养。在氧化培养的第0、1、2、4、6 h取样,取1 mL样品于50 mL离心管中,加入8 mL的0.1 mol/L硫酸铝浸提剂,加塞,摇匀。放置5 min后用慢速滤纸过滤,将滤液转移至50 mL容量瓶。加入1 mL盐酸羟胺,摇匀。放置5 min后,加入5 mL邻菲罗啉溶液,再加超纯水稀释至刻度。放置45 min,在分光光度计上,于530 nm进行测定并根据公式(3)-(4)计算Fe(Ⅱ)质量分数及Fe(Ⅱ)消耗速率常数。
式中:wFe(Ⅱ)为亚铁量(mg/kg);m1为在工作曲线上查得铁量(μg);t为分取倍数(待测液体积mL与吸取待测液体积mL比值);m为新鲜土样质量(g);k为新鲜土样换算成烘干土样的水分换算系数。
式中:kobs,Fe(Ⅱ)为二价铁消耗速率常数[mg/(kg·h)];d(Rt1-t2)为t1-t2时间段内二价铁消耗量的微分。
-
土壤有机质(Soil Organic Matter,SOM)用油浴加热—K2Cr2O7法测定。将土壤鲜样自然风干,研磨,过100目筛后,称取0.2 g土壤样品于硬质试管,加K2Cr2O7与H2SO4的混合液5 mL,放入小漏斗,用石蜡锅煮沸腾5 min。冷却后,将样品与洗涤液转移至三角瓶,总体积约40~50 mL。加3滴邻菲啰啉指示剂,用FeSO4溶液滴定至紫红色,记录消耗FeSO4溶液体积并计算土壤有机质质量分数。
-
利用Excel 2019进行数据整理和描述性统计,SPSS 27.0进行数据统计分析,Origin 2021进行绘图。采用线性回归分析、皮尔逊相关性分析进行参数间的相关性检验,采用单因素方差分析(ANOVA)检验各因素的显著性差异。
1.1. 供试材料
1.2. 试验设计
1.3. 样品采集与处理
1.4. 测试方法
1.4.1. ·OH的测定
1.4.2. Fe(Ⅱ)的测定
1.4.3. 土壤有机质的测定
1.5. 数据处理与分析
-
使用便携式pH计对酸化紫色水稻土的pH值进行原位测定。添加不同土壤改良剂的酸化紫色水稻土的pH值存在一定差异(表 1),6种土壤样品的pH值范围为4.28±0.06~6.67±0.04,呈酸性或弱酸性。6种土壤样品的pH值从大到小依次为:石灰、海泡石、水稻秸秆生物炭、猪粪、生物有机肥、CK。所有处理组的pH值均显著高于CK处理组,说明加入改良剂可以提高酸化土壤的pH值。由表 1可知,海泡石和石灰处理组的改良效果较好,由于石灰中富含碱性物质,可以有效中和土壤中的活性酸和潜性酸,提高pH值[16]。值得注意的是,海泡石具有高比表面积和强吸附能力,一方面可吸附土壤中的氢离子,降低土壤的酸度,提高pH值;另一方面还可释放出一些碱性物质(如钙离子),中和酸性物质,起到提高土壤pH值的作用。
对水土交界界面的氧化还原电位进行现场测定,施用不同土壤改良剂后,酸化紫色水稻土的Eh值存在一定差异(表 1)。6种土壤样品的Eh值范围为-178.4±0.4~-262.8±1.5 mV,均呈现出一定的还原性。其中,海泡石和石灰处理组的Eh值显著低于CK处理组,说明添加海泡石和石灰有利于土壤形成良好的还原性环境,可以在再氧化过程中释放更多的电子,促进·OH的产生。
-
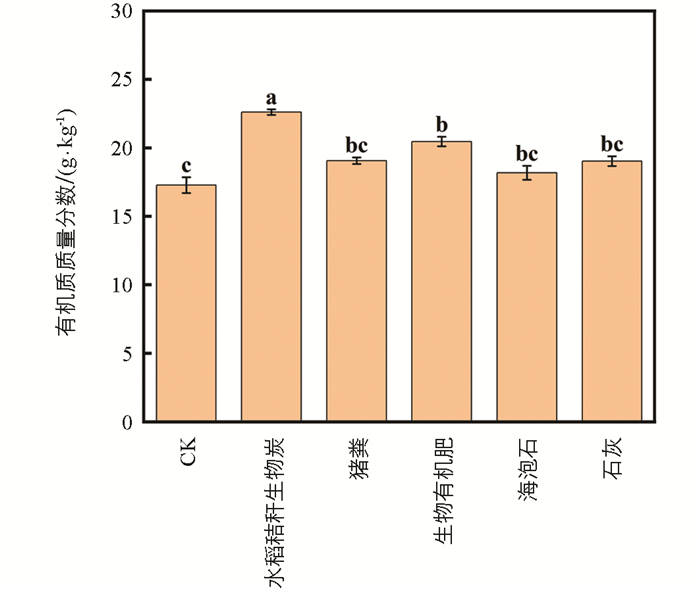
改良剂的加入会影响稻田土壤中有机质的质量分数和性质[4]。本研究中,施用不同土壤改良剂的酸化紫色水稻土的SOM质量分数范围为17.53±1.67~21.86±1.29 g/kg,不同处理之间SOM存在一定差异(图 1)。水稻秸秆生物炭和生物有机肥作为有机物料,施入土壤后,能显著增加SOM质量分数(p<0.05)。而石灰和海泡石属于无机改良剂,对土壤有机质质量分数的影响相对较小。
-
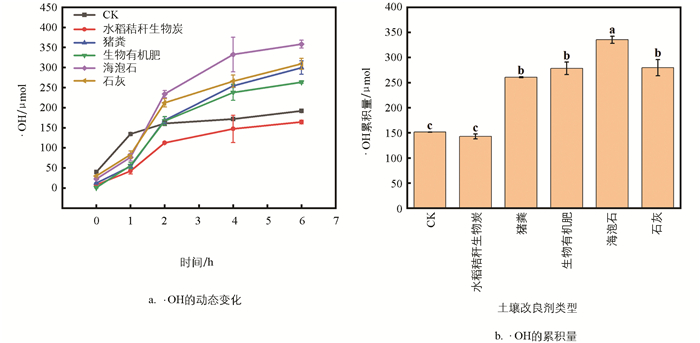
由图 2a可知,施用不同土壤改良剂的酸化紫色水稻土在氧化培养前期(0~2 h)迅速累积,随着氧化培养时间的增加,·OH的累积量总体呈上升趋势。氧化6 h达最大值,可达到142.73±4.78~335.24±7.21 μmol/L,说明氧气是介导·OH生成的重要因素。由图 2b可知,施用不同土壤改良剂的酸化紫色土·OH的表观产量存在一定差异。6种土壤样品·OH累积量从大到小依次为:海泡石、石灰、生物有机肥、猪粪、CK、水稻秸秆生物炭。除水稻秸秆生物炭处理组·OH累积量与CK处理组无显著差异以外,其余土壤改良剂处理组·OH的表观产量均显著高于CK处理组(p<0.05),其中海泡石的促进效果最强。
对0~2 h ·OH的累积量进行生成速率常数拟合(表 2),结果表明,不同土壤改良剂处理组之间·OH生成速率存在明显差异,6种土壤样品kobs,·OH从大到小依次为:海泡石、石灰、猪粪、生物有机肥、CK、水稻秸秆生物炭。其中海泡石处理组的kobs,·OH最大,且与其余改良剂处理组之间差异有统计学意义(p<0.05),而水稻秸秆生物炭处理组的kobs,·OH显著低于其他处理组(p<0.05)。各个处理组kobs,·OH的大小与·OH的最终累积量大小呈正比关系,进一步说明了海泡石、石灰、生物有机肥、猪粪的添加对水稻土中·OH的生成有促进作用。
-
Fenton体系是以H2O2和O2作为自由基前驱体,分别以Fe(Ⅱ)、Fe(Ⅲ)作为电子供体、受体,通过链式反应生成活性氧的体系,用于引发或终止自由基的生成[17]。在地下环境中,含铁(Ⅱ)黏土矿物通常被认为是土壤和沉积物中激活O2生成·OH的主要成分,它通过一系列单电子转移反应还原氧气并依次生成O2·-、H2O2和·OH[4]。Fe(Ⅱ)在·OH的产生过程中占据主导作用,其存在对·OH的生成非常重要[18]。因此我们推测不同改良剂处理组中水稻土Fe(Ⅱ)质量分数可能存在差异,从而导致·OH的生成潜能不同。
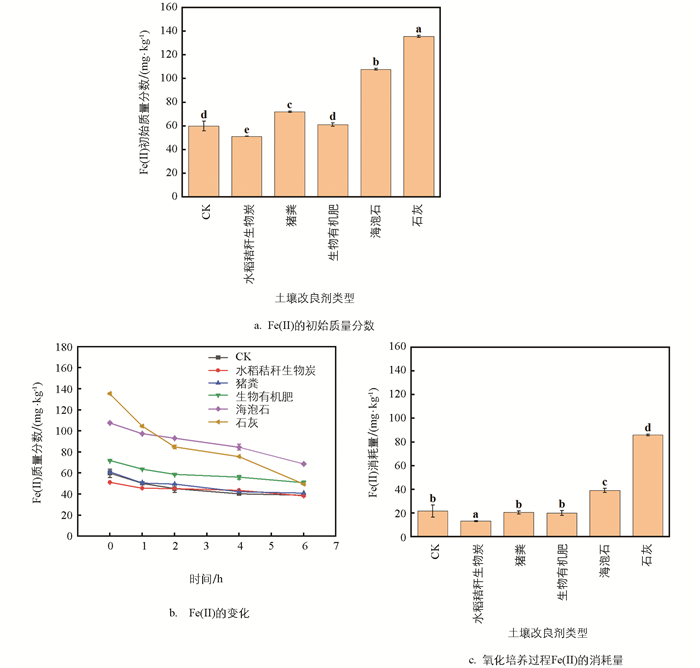
不同改良剂处理酸化紫色水稻土氧化培养过程Fe(Ⅱ)初始质量分数、Fe(Ⅱ)变化及氧化培养过程Fe(Ⅱ)的消耗量如图 3所示。
如图 3a所示,厌氧条件下,不同处理组土壤Fe(Ⅱ)初始质量分数(mg/kg)从大到小依次为:石灰(135.52±0.85)、海泡石(107.82±0.78)、猪粪(71.98±0.49)、生物有机肥(60.98±1.47)、CK(59.91±4.01)、水稻秸秆生物炭(51.20±0.23)。其中,水稻秸秆生物炭处理组0 h时Fe(Ⅱ)总质量分数显著低于CK处理组(p<0.05),生物有机肥处理组的Fe(Ⅱ)质量分数与CK处理组无显著差异,而海泡石与石灰处理组的Fe(Ⅱ)质量分数显著高于其他处理组(p<0.05)。此外,随着氧化时间增加,酸化紫色水稻土中Fe(Ⅱ)质量分数均呈下降趋势(图 3b),并且不同处理组中Fe(Ⅱ)的消耗量也存在一定差异(图 3c),6种土壤样品Fe(Ⅱ)消耗量(mg/kg)从大到小依次为:石灰(85.96±0.74)、海泡石(39.09±1.82)、CK(21.64±5.21)、猪粪(20.52±1.36)、生物有机肥(20.04±2.04)、水稻秸秆生物炭(13.14±0.45)。其中,水稻秸秆生物炭处理组的Fe(Ⅱ)减少量低于其他处理组(p<0.05),猪粪和生物有机肥处理组Fe(Ⅱ)消耗量与CK处理组无显著差异,而海泡石和石灰处理组Fe(Ⅱ)消耗量均显著高于CK处理组(p<0.05)。
在氧化培养初期(0~2 h),不同改良剂处理紫色水稻土中Fe(Ⅱ)质量分数呈现出急剧下降的趋势,对该阶段Fe(Ⅱ)的质量分数进行伪零阶生成速率常数拟合,得到氧化培养过程中提取Fe(Ⅱ)的伪零阶转化速率常数kobs,Fe(Ⅱ)。如表 3所示,6种土壤样品kobs,Fe(Ⅱ)从大到小依次为:石灰、海泡石、CK、猪粪、水稻秸秆生物炭、生物有机肥,其中石灰处理组显著高于其他处理组(p<0.05),说明石灰对水稻土中Fe(Ⅱ)的转化有显著促进作用。
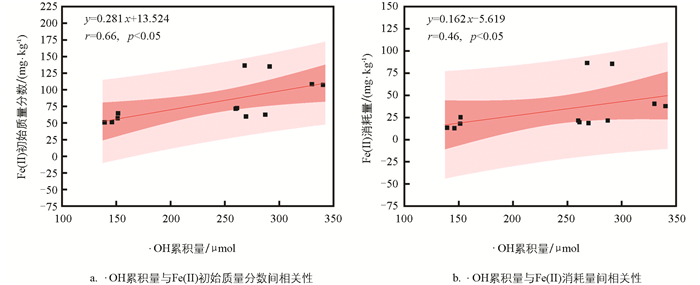
进一步对不同土壤改良剂处理组Fe(Ⅱ)的初始质量分数、氧化消耗量与·OH累积量进行线性回归分析(图 4),结果表明,Fe(Ⅱ)初始质量分数与·OH累积量呈正相关,说明体系中Fe (Ⅱ)初始质量分数对·OH的生成具有显著影响。氧化培养过程中,Fe(Ⅱ)消耗量与·OH累积量呈显著正相关(p<0.05),说明随着Fe(Ⅱ)的消耗,土壤体系中·OH在不断生成。并从图 2和图 4中发现,·OH的生成趋势与Fe(Ⅱ)的消耗趋势基本保持一致,均为0~2 h反应速率最快,2~6 h反应速率逐渐减缓。在氧化过程中,·OH的产生在2 h后减慢,可能是由于活性较高的Fe(Ⅱ)快速消耗,随后活性较低的Fe(Ⅱ)向O2转移电子的效率降低[19]。
-
与CK处理组进行比较,除水稻秸秆生物炭处理组以外,其余处理组均显著促进体系中·OH的生成(p<0.05)。不同土壤改良剂处理的酸化紫色水稻土中·OH的表观产量存在差异,这可能与土壤改良剂本身的性质有关。不同土壤改良剂通过直接或间接影响酸化紫色水稻土基本性质及Fe(Ⅱ)质量分数,进而影响·OH的表观产量。
经石灰和海泡石处理的·OH表观产量显著提高。添加石灰后,酸化紫色水稻土Eh值显著降低(p<0.05),土壤还原性增强,有利于Fe(Ⅱ)的稳定存在。因此,石灰处理组氧化培养前Fe(Ⅱ)初始质量分数显著高于其他处理组(p<0.05),其·OH的产生量也得到显著提高(p<0.05)。也有研究表明,加入少量石灰后土壤溶液pH值轻微提高,更有利于体系中H+电离,并且土壤中带负电的有机官能团成为更具反应活性的电子供体[20],从而更容易生成·OH。海泡石可作为载体,因此可通过协同载体与催化剂的作用提高催化剂的芬顿性能[21]。已有研究表明,在酸性环境中,部分海泡石表面被溶蚀,孔隙率增加,可能增加催化剂的活性位点[22],从而促进海泡石与土壤中的有机质和铁结合,导致反应中电子传递加快,促进·OH的生成。
生物有机肥处理组和猪粪处理组的·OH的生成量显著高于CK处理组(p<0.05)。生物有机肥会提高溶解性有机物质量分数,相关研究表明,SOM会参与·OH的产生[23],还原后的SOM与Fe(Ⅱ)具有相似的·OH生成潜力[18]。SOM中的还原部分向O2提供电子,产生H2O2,进一步分解产生·OH[5, 24-25]。而猪粪处理组·OH表观产量显著高于CK处理组,其氧化培养前的Fe(Ⅱ)总质量分数显著高于CK处理组(p<0.05)。有研究表明,添加猪粪后,土壤中有效铁的质量分数会显著提高,添加10 g/kg猪粪可使土壤有效Fe质量分数增加128.6 mg/kg[26]。这是由于在集约化养殖畜禽的饲料中,铁等微量元素添加剂应用广泛,但畜禽对这些微量元素的利用率不高,导致铁等微量元素在畜禽粪中残留量较高[26]。
有研究提出,生物炭通过增加碳储量释放养分和加速电子转移过程来影响土壤性质[15],并且有助于形成大的土壤团聚体,进而对·OH的累积产生积极作用。但与以往研究不同,经水稻秸秆生物炭处理的紫色土·OH表观产量并未显著提高。这也许是由于SOC与Fe(Ⅱ)络合阻止了Fe(Ⅱ)的氧化,所以最终表现为Fe(Ⅱ)消耗量较低,·OH的产量较低[27]。还可能是因为·OH作为强氧化剂,介导了有机质的矿化,·OH被迅速消耗,导致其表观产量低[27]。水稻秸秆生物炭和生物有机肥都能向土壤中引入大量有机质,但二者对土壤·OH表观产量的影响却存在显著差异,这可能与SOM的组分不同有关。相关研究表明,SOM会参与·OH的产生[23],同时也是·OH的淬灭剂,其分子量大小、腐殖化程度、官能团、芳香性和饱和度影响着·OH的产生与积累[28]。不同来源的同种有机质组分以及同一来源的不同有机质组分均可能影响·OH的产生机制,然而目前学界对于促进·OH的产生或猝灭·OH仍缺乏系统研究[28]。此外,水稻秸秆生物炭和海泡石均具有复杂的孔隙体系和高比表面积,这使得二者均可作为载体且具有较强的吸附性,但是二者对·OH表观产量的影响存在着较大差异[29]。经水稻秸秆生物炭处理的·OH表观产量无显著变化,而经海泡石处理的·OH表观产量显著提高。水稻秸秆生物炭和海泡石均具有吸附性能[30-31],添加生物炭导致对重金属离子的吸附量增加,从而引起反应体系Fe(Ⅱ)质量分数降低[32-33]。由此推测,水稻秸秆生物炭可能对铁进行吸附固定,从而限制了芬顿反应的进行。同时,水稻秸秆生物炭也可作为载体,能够通过与催化剂的协同作用增强催化剂的芬顿反应性能[34]。水稻秸秆生物炭与海泡石对·OH表观产量影响不同,这或许与它们在充当载体时,催化作用和吸附性能的相对强弱有关,但目前这方面的研究成果尚不足,仍需进行更深入的研究。
2.1. 不同土壤改良剂处理下酸化紫色水稻土的基本性质
2.1.1. 不同土壤改良剂处理下酸化紫色水稻土pH值和Eh值的变化
2.1.2. 不同土壤改良剂处理下酸化紫色水稻土SOM的变化
2.2. 不同土壤改良剂处理的酸化紫色土·OH表观产量
2.3. 不同土壤改良剂处理的酸化紫色水稻土Fe(Ⅱ)的作用
2.4. 不同土壤改良剂对酸化紫色水稻土·OH表观产量差异性分析
-
1) 土壤改良剂的施用改变了酸化紫色水稻土的基础性质。相较于CK处理组,各改良剂处理组的pH值均有所提高。而土壤Eh值的变化因改良剂类型而异:水稻秸秆生物炭、海泡石及石灰处理组的Eh值显著低于CK处理组,猪粪处理组Eh值显著高于CK处理组。此外,有机改良剂的处理组SOM显著增加,而无机改良剂处理组与CK处理组无显著差异。
2) 土壤改良剂的施用影响了酸化紫色水稻土Fe(Ⅱ)的初始质量分数。水稻秸秆生物炭处理组Fe(Ⅱ)初始质量分数显著低于CK处理组,而生物有机肥处理组Fe(Ⅱ)初始质量分数与CK处理组无显著差异。相比之下,猪粪、海泡石及石灰处理组的Fe(Ⅱ)初始质量分数均显著高于CK处理组。
3) 土壤改良剂的施用对酸化紫色水稻土中·OH的表观产量具有显著影响。不同改良剂对土壤·OH生成的影响存在显著差异:除水稻秸秆生物炭处理组外,其余处理组·OH的表观产量均显著高于CK处理组。这与土壤改良剂对酸化紫色水稻土基础性质与Fe(Ⅱ)初始质量分数的调控作用关系密切,同时也受改良剂本身性质的影响。然而,关于酸化土壤改良剂影响·OH生成的具体途径及其机制仍需进一步深入研究。



 下载:
下载: