-
开放科学(资源服务)标识码(OSID):

-
战争、交通事故、自然灾害的发生,容易导致人体大出血。据报道,全世界30%以上的创伤性死亡是由过度失血造成的,因此,生产具有快速止血作用的止血剂至关重要[1-2]。理想的止血剂应能在极短时间内迅速控制表面外伤或深部组织的大量活动性出血,防止低血容量和低灌注; 还应具有良好的生物相容性,且应现成、易使用、质量轻、稳定、价格便宜。传统的止血方法(如按压止血),虽已被证明对常规出血有效,但在特殊环境中,它们往往无法止住由小口径火器或爆炸装置造成的深层、不可压缩性伤口的出血[3]。
壳聚糖(CS)是从贝类中提取的一种天然碱性糖胺聚糖,具有水溶性、无毒、抗菌、可降解的特性[4-5]。CS具有众多的功能化学基团,作为组织再生的支架材料,可以提供一定的机械支撑,促进细胞附着、增殖和分化[6-7]。壳聚糖还具有止血、可生物降解、生物相容性等特殊性能,被广泛认为是一种良好的生物医学材料,在药物输送系统、伤口敷料、组织工程支架等方面有着广泛的应用[8-9]。有研究表明,壳聚糖具有优异的止血性能,因为它能够形成阳离子簇,与红细胞上的阴离子相互作用,从而诱导血小板聚集,最终阻止出血[10-11]。然而,这些壳聚糖产品具有局限性,纯壳聚糖止血材料对于严重出血的止血效果并不稳定,如它们无法对不可压缩性创口进行有效止血,或在按压伤口时很容易破裂被分解,因此,需结合其他凝血因子和止血材料等来增强其止血效果[12-14]。
桃胶(PG)为蔷薇科植物桃树皮受损后分泌出来的不规则块状或泪滴状物质,特别是在机械损伤后,受到微生物的攻击而形成。在大型桃园中,因为不断修剪导致真菌感染,从而产生大量大小不一、表面淡浅黄色或黄棕褐色的琥珀状半透明固体桃胶。桃胶主要是由阿拉伯糖、甘露糖、葡萄糖、木糖、鼠李糖、葡萄糖醛酸等单糖按一定的比例和连接顺序形成的[15]。近年来,关于桃胶在医药方面应用的报道有所增多,主要集中在桃胶多糖对糖尿病患者降血糖、降血脂的机理研究方面,也有一部分是关于临床应用的。通过注射糖尿病模型小鼠,证实桃胶多糖有降血糖的作用,同时具有提高胸腺和脾脏指数、促进肠蠕动的免疫调节和杀菌等功能[16-17]。在创伤治疗方面,桃胶能改善烧伤创面局部的微循环,具有明显的保护作用并且能在一定程度上起到抗感染、杀菌的功效,能明显促进烧伤创面的愈合[18]。
选用单宁酸作为交联剂[19],采用冷冻干燥法制备壳聚糖/桃胶(CS/PG)止血海绵,旨在找到一种可快速吸水膨胀、对深度不可压缩性出血有止血功能的材料。为了准确评价CS/PG止血海绵作为一种可吸收的活体止血材料的可行性,我们测定了止血海绵在体外和体内的止血效果,并与其他市场上常见的止血材料进行比较,系统地评价这些材料的特性、止血效果和生物相容性。
全文HTML
-
开州油桃种植园(重庆)收集桃树(P. persica)树干的桃胶,壳聚糖由上海麦克林生化有限公司提供,小鼠L929细胞由中国科学院细胞库提供。
-
可溶性桃胶的制备参照文献[20]略作修改。取10 g原桃胶溶入600 mL去离子水中,浸涨后用镊子等工具清除附着在桃胶表面的杂质,对桃胶悬浮液用纱布过滤除杂; 恒温磁力搅拌器上85 ℃缓慢不停地搅拌,控制水解加热时间3 h; 将水解后的桃胶溶液抽滤除去不溶物,冷却后调节pH值至中性; 冷冻干燥后,得到水解后的可溶性桃胶冻干粉末,备用。
-
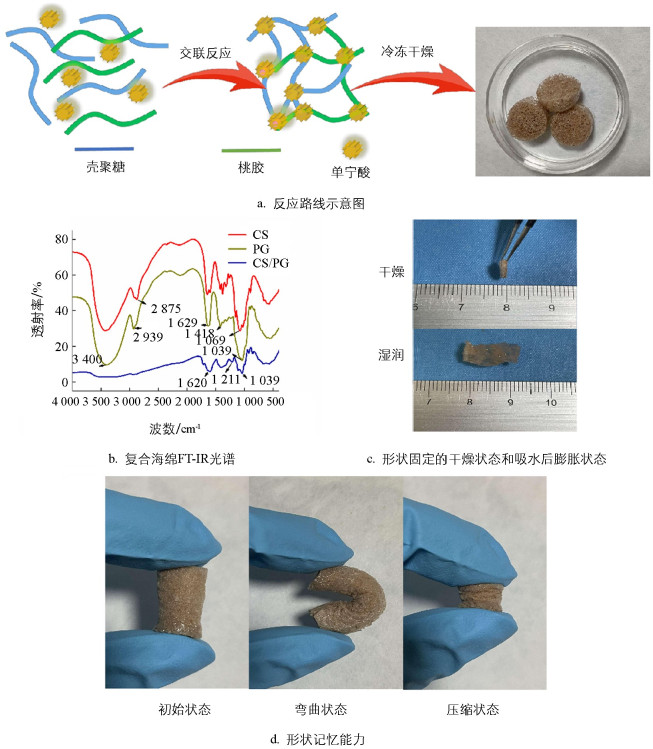
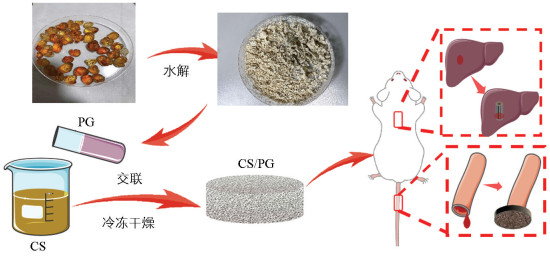
壳聚糖和桃胶冻干粉完全溶解在0.1 mol/L的抗坏血栓溶液中,在室温下得到5%溶液,制备4种不同PG浓度(0%、10%、30%和50%)的海绵样品(CS/PG0、CS/PG10、CS/PG30和CS/PG50),为了交联,加入浓度比为0.05%的单宁酸,并在60 ℃条件下搅拌20 min,直到观察形成棕色的凝胶,然后取20 mL凝胶加入0.7 mL甘油放入培养皿中进行-50 ℃冷冻24 h,最后冷冻干燥48 h,形成多孔海绵支架,CS/PG止血海绵合成过程见图 1。
-
扫描电子显微镜(SEM)评估材料的表征结构和形貌特性,用来联系应力和变形、表面粗糙之间的关系,从而提供有关结构及其功能的关键信息。为了进行分析,不同桃胶比例的复合海绵材料样品被金溅射涂层,并放置在双面碳带上,在扫描电子显微镜中成像,以确定有代表性的泡沫形态,用数码相机记录每个CS/PG止血海绵样品的形貌。
-
将等体积(直径1.5 cm,高1 cm)的样品预先称质量(Wd),试验中医用纱布和明胶海绵作为对照,不施加外力放入PBS溶液中保持60 s,然后取出测试,用滤纸吸去样品表面的水分,测定湿质量(WW)。根据公式计算各产品的吸水率(R),每个样品在相同条件下测3次。
-
生物相容性是评估生物材料应用的重要前提,确保材料与生物体的相互作用不致引发不良反应。本研究使用中国科学院细胞库提供的小鼠成纤维细胞L929进行生物相容性试验,评估CS/PG对细胞的生物相容性:首先将CS/PS用75%酒精浸泡4 h,PBS冲洗5次后,紫外线照射2 h,加入α-MEM培养基孵育过夜。将小鼠成纤维细胞L929以5×104个/孔的密度接种在48孔板中,24 h后加入灭菌过后的海绵材料,放置在细胞培养箱中培养,采用MTS法检测L929的增殖活力。MTS是一种四氮唑盐化合物,可被活细胞线粒体中的多种脱氢酶还原,生成蓝紫色的甲臜(Formazan)结晶,其颜色深浅与活细胞数在一定范围内呈高度相关。
其次在预定时间点(48 h)取出细胞板,吸除培养基加入500 μL PBS小心清洗1次,每孔加入500 μL MTS工作液(MTS∶α-MEM=1∶4)后放置在细胞培养箱中避光孵育2 h。最后轻轻吹匀上清液,每孔吸取100 μL上清液加入96孔板中,通过酶标仪(Synergy H1,Biotek美国) 490 nm波长下检测吸光度。将接种在含有10% PBS的α-MEM培养基中的细胞用作对照,其吸光度用于确定细胞的100%存活率,其中Ap为阳性对照组的吸光度,An为阴性对照组的吸光度,Ae为实验组的吸光度,根据公式计算细胞活力(V)。
细胞染色是将细胞接种到样品上,在48 h时进行LIVE/DEAD染色。在PBS中制备染色液,其中包含30 μL的1.5 mmol/L碘化丙啶(美国光大)和5 μL的4 mmol/L钙黄绿素AM(美国光大),在每个样品中加入100 μL的染色液,在室温下孵育20~30 min,然后使用荧光显微镜(Olympus,BX3-SSU,日本)观察,活细胞被染成绿色,死细胞被染成红色。
-
经过前期试验验证,找到1个PG配比的CS多孔海绵(CS/PG30)具有良好的生物相容性和理化性能,更加符合临床要求,并在紫外线下进行灭菌; 商用止血纱布和明胶海绵用作对照,使用肝损伤模型和截尾模型评估所有材料的止血效果。本工作得到西南大学动物护理和伦理委员会的批准(IACUC-20210415-09),选用健康的Sprague-Dawley大鼠(雄性,体质量200~220 g)构建止血模型。
-
大鼠舒泰麻醉后尾根部5 cm处用外科剪刀剪掉制作截尾模型,切除后,将大鼠尾部置于空气中10 s,以保证正常失血,将每个试验样品(纱布、明胶海绵、CS/PG30)覆盖在伤口上。止血成功定义为10 min内无活动性出血,记录止血时间及出血量。
-
大鼠麻醉后,剪掉其腹毛,剖开腹腔,露出肝脏,用活检针(内径4 mm)造出肝脏穿孔容积缺损(直径4 mm、深度5 mm的圆柱形创面),自由出血持续5 s以确保正常失血,然后分别用不同样品覆盖伤口。提前将直径为8 mm,高度为5 mm的CS/PG30压缩成新的尺寸(直径为4 mm,高度为5 mm),市售明胶海绵切成同样大小,然后立即将海绵放入缺损伤口内,并在肝脏底部放置滤纸和纱布以评估失血量,无出血后记录止血时间及失血量。
-
所有测试进行3次重复,数据以x±s表示。统计学比较采用t检验,p<0.001(***)、p<0.01(**)和p<0.05(*)表示差异有统计学意义。
1.1. 材料
1.2. 可溶性桃胶制备
1.3. 壳聚糖/桃胶(CS/PG)止血海绵的制备
1.4. 壳聚糖/桃胶止血海绵的形态表征
1.5. 壳聚糖/桃胶止血海绵的吸水率分析
1.6. 体外细胞毒性
1.7. 动物(SD大鼠)模型中的止血研究
1.7.1. 尾静脉止血
1.7.2. 肝脏体积缺损止血
1.8. 统计学分析
-
我们通过混合壳聚糖、桃胶、单宁酸和甘油的预冷溶液,冷冻干燥技术伴随着交联反应,制备了有形状记忆功能的可生物降解的生物海绵复合物,具有良好的生物相容性和快速的水诱导形状恢复性(图 2)。由图 2a可知,单宁酸作为交联剂使CS和PG相互产生了交联反应,形成互穿网络聚合物Interpenetrating Polymer Network (IPN)[21],产生了稳定的三维网络结构,具有良好的机械强度和优良的机械稳定性,具有IPN结构的压缩海绵与水接触后可以快速恢复形状。
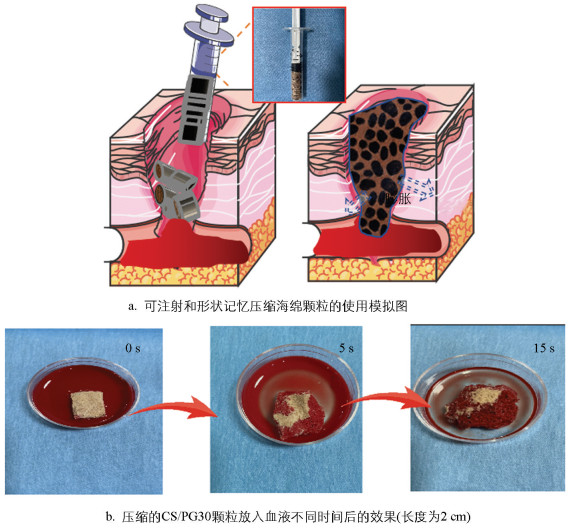
从图 2中还可以看出壳聚糖和桃胶经交联反应后形成的CS/PG止血海绵的红外光谱存在一定的差别,CS和PG在3 400 cm-1处有明显-NH2收缩振动峰[22]; 壳聚糖是一种带醚键的多糖,1 069 cm-1处为C-O-C收缩振动峰,为多醚(糖苷键)的特征峰; 桃胶为复杂多糖,1 629 cm-1处为多糖-CHO中C=O收缩振动峰; 与CS/PG比较,糖苷键特征峰移到1 090 cm-1处,多糖的C=O收缩振动峰移到1 620 cm-1,2 939 cm-1和2 875 cm-1处-CH2-收缩振动峰基本消失; 1 418 cm-1和1 211 cm-1为苯环中C=C骨架振动峰,这可能归因于单宁酸氧化反应与桃胶和壳聚糖中的氨基产生了交联反应,使得生成物中的-NH2吸收峰消失,形成了稳定的互穿网络结构[23]。图 3b展示了压缩材料颗粒在放入血液中后不同时间的一系列照片,可以看出压缩颗粒在接触血液后不到20 s就可以重新膨胀到原来的形状,并对周围的血液进行吸收,同时为出血的血管施加压力进行止血。CS/PG多孔海绵这种可注射和形状可恢复的特性(图 3),能根据不同的应用场景,通过简单压缩固定成不同的形式,表明其在不可压缩和可压缩出血中的应用潜力巨大。
-
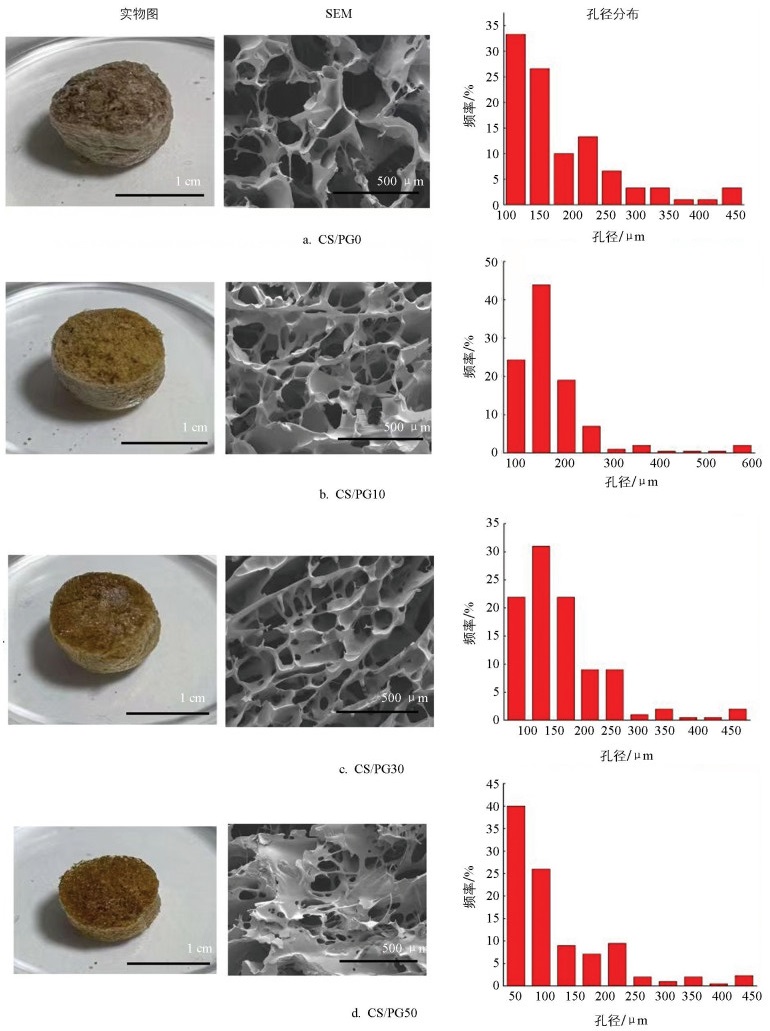
图 4显示,不同浓度PG对海绵孔洞分布影响明显。各组样品孔径主要集中在50~200 μm,这个范围有利于细胞的大量接种、细胞和组织的生长、胞外基质的分泌、氧气和营养的传输、代谢产物的排泄以及血管和神经的内生长,同时还能提供细胞所需的各种信号,诱导细胞黏附、增殖与分化,最终形成特定的组织。观察显示,各组多孔支架内部的孔形态基本呈不规则的椭圆形,每个孔的内壁还有很多小孔和大孔,这样保证了支架中各个孔之间的连通性,从而有利于细胞在支架中的生长和迁移。孔径分布情况虽然相差不大,但是不同浓度PG的加入,对各个孔之间连接有明显的改变,PG的加入可以起机械支撑和可加强连接的作用,导致海绵的形态更加稳定。从SEM图中可以看到,CS/PG0材料的孔有部分结构坍陷,随着PG浓度的增加,海绵的塑形越来越紧密,到30%时空隙结构相对均匀、大部分保持完好且孔径大小合适,但当PG浓度达到50%时复合多孔海绵因表面部分过于连接呈现出不规则的连片形状。总的来说,通过在CS中加入30%的PG,利用交联和冷冻干燥可以制备出相对形态良好的三维多孔支架,用于临床敷料,能促进细胞的增殖和分化,还能促进细胞的黏附和迁移。
-
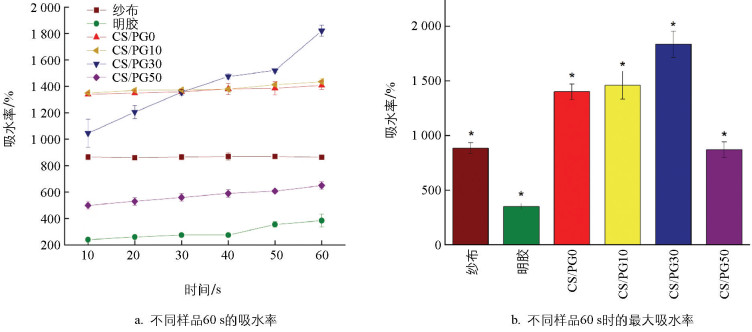
多孔海绵材料在临床中具有重要作用,特别是其吸水率和吸水速度对组织的修复和止血至关重要。这种材料能吸收数倍于自身质量的水分,这得益于其特殊的多孔结构,既保持了稳定又为机体提供了营养与废物交换的通道。研究对比了不同配比的壳聚糖/明胶(CS/PG)止血海绵与商用止血材料,结果显示,与纱布相比,明胶海绵吸水慢,而CS/PG止血海绵吸水迅速(图 5)。在10 s内,纱布吸水率为865%,而CS/PG0和CS/PG10分别达到1 340%和1 350%,显示出明显的优势,特别是CS/PG30,在10 s内吸水率为1 045%,60 s时吸水率达到了1 820%,非常适合临床应用。CS/PG50吸水率虽然也不错,但吸水速度较慢,不适合紧急止血。综合考虑,CS/PG30因其在吸水速度与吸水能力之间均较好,更适合复杂的临床需求。
-
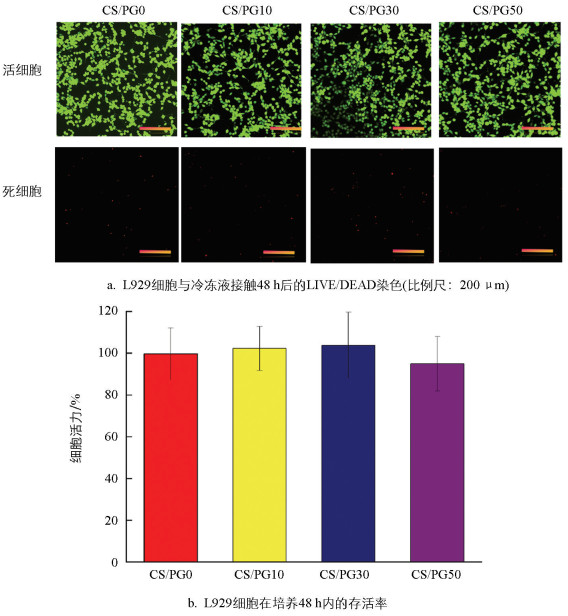
图 6显示,细胞在不同组别中均匀分布,大多数细胞呈规则的圆形或椭圆形,各组细胞的分化行为没有明显差异。
经过培养48 h后,各组细胞的活力值均超过90%,表明多孔海绵材料对细胞的生长和存活没有明显的不良影响。为了进一步评估多孔海绵材料的细胞相容性,我们进行了活/死细胞的活力测定,结果显示,几乎所有的L929小鼠成纤维细胞都被钙黄绿素AM染为绿色,细胞形态正常,仅存在少量的死亡细胞,并且不同浸提液组的细胞数量和形态之间差异无统计学意义。这可能是因为多孔海绵材料由天然壳聚糖和桃胶等多糖原料组成,对细胞表现出优异的生物相容性。CS/PG所有样品的细胞生长良好,证明其可作为一种有效且无毒的生物材料。
-
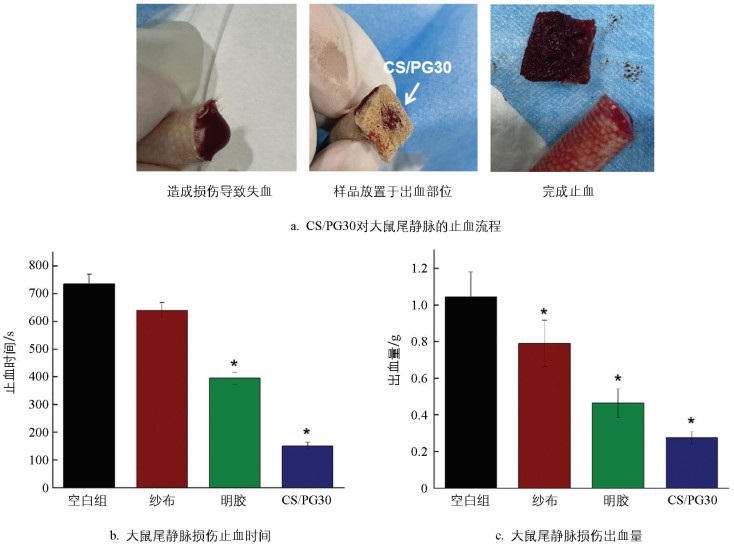
根据各个样品相关检测结果,选用性能更适合临床需求的CS/PG30进行体内止血测试。为了评价CS/PG30的体内止血性能效果,建立了大鼠截尾模型和肝损伤模型。从图 7中可以看出大鼠切尾,在没有任何预防措施的情况下,止血时间为(735±35) s,出血量为(1.04±0.13) g。应用不同的止血材料后,止血时间和出血量均有所减少,尤其是CS/PG30,止血时间和出血量效果更为显著,为(150±14) s和(0.27±0.03) g,与其他商用止血材料相比效果更佳。使用纱布直接按压鼠尾,可以发现纱布可以防止血液流出,但不会促进血液凝固,即使长时间后,血液也会从纱布中渗出。明胶止血产品的机械性能较差,遇到血液后,极易破损,因此对于大的伤口出血很难止住。CS/PG30可以快速吸收血液并有一定的黏附性,有利于紧贴创面,多孔结构又会使血液的黏度增大,吸附血小板,启动内源性凝血,促进血块的形成,从而达到最佳的止血效果。
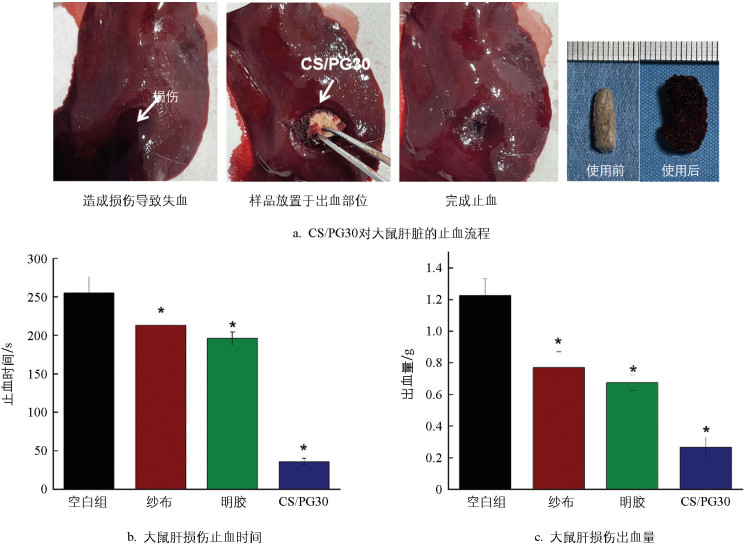
临床中,对于狭窄和深度的不可压缩性出血,传统的止血材料往往效果不佳。本研究利用打孔设备在大鼠的肝脏制造贯穿伤,模拟大鼠肝损伤模型以此评价材料在体内深窄非压缩性出血的止血效果。图 8显示,与空白组比较,所有样品材料均比空白组出血量少,止血时间短。商用明胶海绵有一定的止血效果,但对于出血较多的部位,容易被血液溶解,极易破损,从而无法紧贴创面,对于血细胞,牵拉能力也十分弱,进而达不到更好的止血效果[24]。止血纱布虽然有较好的力学性能,但对于深、窄的伤口运用效果非常有限,无法全面无死角地堵塞复杂的出血部位。CS/PG30多孔海绵的止血能力明显优于其他商用止血材料,止血时间和出血量分别为(36±4) s和(0.26±0.06) g,主要是因为多孔海绵不仅能吸收伤区血浆,集中血细胞,增强凝血功能,还因为它的填塞效果好。CS/PG30多孔海绵独特的形状恢复功能赋予了它的可注射性,并允许它们可以快速应用于狭窄、深、不规则的伤口中。压缩的CS/PG30多孔海绵一旦接触到血液,就会迅速吸收血液,扩大体积,填满伤口腔体,同时浓缩血细胞和血小板,加速血液凝固,从而促进止血。多孔海绵膨胀时施加一定的膨胀力为出血部位提供了持久的压力,以帮助止血和防止材料在血流下分散。上述结果表明,CS/PG30多孔海绵不仅能促进血液凝固,还能促进止血,特别是在狭窄和深层不可压缩性出血的止血应用中潜力巨大。
2.1. 形状记忆功能
2.2. 电镜扫描结果
2.3. 吸水率
2.4. 多孔海绵材料的细胞毒性分析
2.5. CS/PG30大鼠肝脏和尾静脉损伤的止血
-
本研究通过单宁酸作为交联剂冷冻干燥制备CS/PG止血海绵,在保留壳聚糖止血优点的同时,进一步促进了液体的吸收,提高了力学性能。CS/PG30多孔海绵体外和体内止血试验均表明,与止血纱布和明胶海绵相比,该多孔海绵可显著减少失血量,缩短止血时间。更重要的是,它的原料是天然的壳聚糖和桃胶,与机体有很好的相容性和生物安全性。复合海绵具有相互连通的多孔结构,机械强度稳定,只需简单压缩即可固定,由于海绵具有多孔稳定的高吸水能力,可通过内源性凝血途径显著黏附、激活红细胞/血小板,形成稳健的血凝块。多孔海绵体外测试还发现,压缩的海绵与液体接触后,具备记忆功能体积可快速膨胀,并表现出独特的形状适应能力,可用于填充大型的、不规则的深度伤口。压缩的海绵还可以通过套管或注射器输送到受伤部位,然后在与血液接触后的几秒内重新膨胀至原来的形状。图 3所示为压缩材料的颗粒包装和注射到复杂创口的过程。CS/PG止血海绵这种可注射和形状可恢复的特性,可根据不同的应用场景,通过简单压缩固定成不同的形式,表明其在不可压缩和可压缩出血中的应用潜力巨大。综上所述,多孔海绵具有吸水性好、力学性能好、溶血率低、无细胞毒性、反复压迫后恢复能力好、止血能力强等特点,是一种可以转化为临床安全、快速的民用和军用创伤急救止血生物材料。



 下载:
下载: