-
开放科学(资源服务)标识码(OSID):

-
大豆尖孢镰刀菌(Fusarium oxysporum)是全球十大植物病原真菌之一,其引发的大豆根腐病是一种分布广、危害重且防治困难的土传病害。该病在大豆整个生育期均可发生:幼苗期侵染种子导致烂种,出土后危害茎基部引发猝倒,生长期侵染茎秆造成植株矮化或枯死,最终导致大豆产量降低[1]。为提前预防和及时干预,迫切需要能够在大豆种植前检测土壤或发病前及时干预的检测技术,解决减产问题。
已知的尖孢镰刀菌研究初期是采用培养基菌落平板稀释法进行分析的,其优点是制作材料廉价,操作难度较低,但是实验周期较长,效率和灵敏度较低,难以实现更准确、更快速的检测[2]。自分子检测技术的快速发展,常规PCR、实时定量PCR因其较好的灵敏度和准确性被广泛应用于植物病原真菌的检测,但需要专业的技术人员操作大型的仪器设备,且实验时间长,不利于快速便捷的检测。酶促重组等温扩增技术(ERA)是一种新型核酸等温扩增技术,利用重组聚合酶单链DNA结合蛋白和链置换酶,即可在25~42 ℃的恒温环境下完成靶基因数百万倍扩增,具有反应条件简单、不需昂贵仪器、操作便捷、灵敏度高和特异性好等一系列优势,满足快速准确检测的需要[3]。近年来,ERA技术已经广泛应用于植物真菌检测中,例如对玉米锈病菌[4]、黄氏根腐病[5]、梨火疫病菌[6]等的检测,表明ERA在植物病害检测方面,技术已经逐渐成熟,这为大豆尖孢镰刀菌的检测奠定了基础。
本研究使用ERA技术,针对大豆尖孢镰刀菌设计特异性引物,预期建立一种能够快速、便捷、高灵敏的检测体系,实现对大豆尖孢镰刀菌的早期诊断和快速筛查,在提高经济效益的同时也为吉林省大豆根腐病的快速筛查提供新的检测技术与检测产品。
HTML
-
大豆尖孢镰刀菌(Fusarium oxysporum)、大豆疫霉菌(Phytophthora sojae)[2]、大豆灰斑菌(Cercospora sojina)、茄腐镰刀菌(Haematonectria haematococca)、东北霜霉菌(Peronospora manschurica)、锐顶镰孢菌(Fusarium acuminatum)、腐皮镰孢菌(Fusarium solani)均为吉林农业科技学院农学院赠送。
-
基础型核酸扩增试剂盒(ERA法)购自苏州先达基因科技有限公司;十二烷基磺酸钠(SDS)、DL 500bp DNA Marker购自上海生物工程有限公司;十六烷基三甲基溴化铵(CTAB)、月桂酰肌氨酸钠(N-Methylglycinol)购自天津福晨化学试剂有限公司;四正丁基溴化铵(TBAB)购自上海生物工程有限公司;自聚乙烯吡咯烷酮(PVP)购自飞科生物科技有限公司;β-巯基乙醇(BME)购自天津大茂化学科技有限公司;核酸提取磁珠(通用型)购自迈途医药科技有限公司;DL 15000bpDNA Marker、Premix Ex Taq Version 2.0(Loading dye Mix)购自宝日医生物技术有限公司[3]。
-
台式高速冷冻离心机(Centrifuge 5430R,德国艾本德公司);恒温水浴锅(HH-12468,常州郎越仪器制造有限公司);电泳仪(DYY-60,北京六一生物科技有限公司);紫外分光光度计(BioSpec-nano,日本岛津公司);高压灭菌锅(MVS-83,北京冠普佳科技有限公司);凝胶成像仪(GenoSens 2000,上海勤翔科学仪器有限公司)。
1.1. 主要材料
1.2. 主要试剂
1.3. 主要仪器
-
将用液氮研磨提取后的粉末状真菌,立即用800 μL预热后的SDS裂解液溶解,并加入40 μL β-巯基乙醇,振荡混匀,55 ℃水浴40 min,且每隔5 min振荡混匀1 min,12 000 r/min、4 ℃条件下离心10 min[7]。取上清液于新管中,加入等体积的事前配制好的酚-氯仿-异戊醇(25∶24∶1),上下颠倒1 min混匀后,12 000 r/min、4 ℃条件下离心10 min[8]。取上清液加入2倍体积预冷的无水乙醇,-20 ℃冰箱静置20 min,离心管内会出现半透明的絮状沉淀,离心管朝一个方向轻轻旋转,使絮状基因组缠绕,12 000 r/min、4 ℃条件下离心8 min,沉淀用预冷的70%乙醇洗涤后10 000 r/min离心5 min(重复2次),弃上清液,然后在超净工作台上放在冰上晾干,然后加入30 μL TE溶解和3 μL RNaseA去除RNA,测浓度后于约20 ℃冰箱保存备用。
-
将用液氮研磨提取后的粉末状真菌装管后立即加入预热的SDS-盐酸胍混合裂解液1 mL,振荡混匀,55 ℃水浴40 min,且每隔5 min振荡混匀1 min,其后步骤同SDS法[8]。
-
将用液氮研磨提取后的粉末状真菌,迅速装管后加入预热的月桂酰肌氨酸钠裂解液1 mL,振荡混匀,55 ℃水浴40 min,且每隔5 min振荡混匀1 min,后续操作同SDS法[9]。
-
将用液氮研磨提取后的粉末状真菌装管后,立即加入预热后含有2.5 mol/L四正丁基溴化铵的SDS-盐酸胍混合裂解液1 mL,振荡混匀,55 ℃水浴40 min,且每隔5 min振荡混匀1 min,后续操作同SDS法[10]。
-
将用液氮研磨提取后的粉末状真菌,装管后迅速加入800 μL预热的2% CTAB裂解液,20 μL蛋白酶K,振荡混匀,55 ℃水浴40 min,且每隔5 min振荡混匀1 min,其后步骤同SDS法。
-
利用已知引物EF、ITS、RPB2(引物序列见表 1)对大豆尖孢镰刀菌进行多次常规PCR扩增鉴定,PCR扩增体系为:正反向引物2.5 mmol/L各添加2 μL,终浓度为30 ng/μL的基因组0.8 μL,Premix Ex Taq Version 2.0(Loading dye Mix)12.5 μL,用水补充至25 μL。程序设定:预变性94 ℃ 5 min,变性94 ℃ 30 s,退火57 ℃ 30 s,延伸72 ℃ 1 min,30个循环,后延伸72 ℃10 min。琼脂糖凝胶电泳检测后,将PCR反应产物送至生工上海生物工程有限公司测序并与NCBI上大豆尖孢镰刀菌进行序列比对[11]。
在NCBI上选择并下载大豆尖孢镰刀病菌和本实验中所用真菌的基因组序列,利用SnapGene软件和NCBI网站进行比对分析,同时进行文献筛查,最终经过多个基因的筛选确定能特异性扩增的基因CYP 505,作为特异性片段并进行引物设计[10]。
-
根据目的片段的基因序列,利用Primer 5.0引物设计软件设计引物如表 1所示,均交于生工上海生物工程有限公司合成[4]。
-
使用苏州先达基因科技有限公司的基础型ERA试剂盒进行ERA扩增。首先将基础反应试剂从-20 ℃冰箱中取出并室温放置10 min。反应体系:ddH2O 21 μL、溶解剂20 μL、正反向引物各2.5 μL、10 ng/μL基因组2 μL、激活剂2 μL(加入到管盖内侧,防止激活剂提前进入反应管内开始反应而影响试验),同时用ddH2O制备阴性对照,混匀离心后立即于40 ℃水浴锅中孵育20 min,取出加入6×loading buffer于56 ℃孵育5 min,最后用2.5%琼脂糖凝胶电泳鉴定,电泳条件设定为80 V恒压,电泳时间55 min,电泳结束后对6个引物组合的电泳结果进行分析,筛选出最佳引物对[12]。
-
确定最佳引物探针浓度组合,设置37 ℃、38 ℃、39 ℃、40 ℃、41 ℃、42 ℃ 6个反应温度[13]。根据步骤“2.4”中筛选出的最佳引物对配制相同反应体系,并利用ddH2O制备阴性对照,于相对应的6个温度条件下孵育20 min,时间到后立即取出并加入6×loading buffer,于56 ℃孵育5 min,反应结束后进行2.5%琼脂糖凝胶电泳鉴定,电泳条件设定为80 V恒压,电泳时间55 min[5],电泳结束后对电泳结果进行分析。
-
以10 min为反应起始时间,每隔5 min设置一个反应时间直到30 min.,根据步骤“2.4”中筛选出的最佳引物对配制相同反应体系,并利用ddH2O制备阴性对照,采用步骤“2.5.1”中最佳反应温度分别孵育10 min、15 min、20 min、25 min、30 min,时间到后取出并加入6×loading buffer,于56 ℃孵育5 min,反应结束后进行2.5%琼脂糖凝胶电泳鉴定,电泳条件设定为80 V恒压,电泳时间55 min,电泳结束后对电泳结果进行分析[14]。
-
将大豆尖孢镰刀菌的DNA浓度依次稀释为9×107、9×106、9×105、9×104、9×103、9×102、9×10、9 fg/μL 8个模板浓度,以步骤“2.4”中筛选出的最佳引物对配制反应体系并检测灵敏度[15]。按不同浓度制备扩增体系,ddH2O制备阴性对照,在最优反应温度和最优反应时间条件下孵育,时间到后立即取出并加入6×loading buffer,于56 ℃孵育5 min,反应结束后进行2.5%琼脂糖凝胶电泳鉴定,电泳条件设定为80 V恒压,电泳时间55 min,确定ERA对大豆尖孢镰刀菌DNA的最低检测限。
-
用筛选出的ERA体系对大豆尖孢镰刀菌、大豆疫霉菌、大豆灰斑菌、茄腐镰刀菌、东北霜霉菌、锐顶镰孢菌、腐皮镰孢菌的DNA进行检测,设置ddH2O为阴性对照,时间到后立即取出并加入6×loading buffer,于56 ℃孵育5 min,反应结束后进行2.5%琼脂糖凝胶电泳鉴定,电泳条件设定为80 V恒压,电泳时间55 min,评价该检测方法的特异性。
-
从田间采集自然发病的大豆尖孢镰刀菌菌丝、未感染大豆尖孢镰刀菌的大豆植株、感染尖孢镰刀菌大豆植株、感染大豆疫霉菌大豆植株、大豆灰斑菌菌丝、茄腐镰刀菌菌丝、锐顶镰孢菌菌丝样品提取DNA稀释至均一浓度,并利用ddH2O制备阴性对照,在上述实验得到的最适反应条件下孵育,时间到后立即取出并加入6×loading buffer,于56 ℃孵育5 min,反应结束进行2.5%琼脂糖凝胶电泳鉴定,电泳条件设定为80 V恒压,电泳时间55 min,电泳结束后对电泳结果进行分析,用以验证此试验是否能在生产生活中得到应用。
2.1. 基因组DNA提取
2.1.1. SDS法
2.1.2. 改良SDS法
2.1.3. 月桂酰肌氨酸钠法
2.1.4. 改良SDS-季铵盐法
2.1.5. 改良CTAB法
2.2. 大豆尖孢镰刀菌的鉴定及特异性片段的筛选
2.3. ERA引物设计
2.4. 基础型ERA反应体系建立及最佳引物对筛选
2.5. 基础ERA反应条件的优化
2.5.1. 最优反应温度确定
2.5.2. 最优反应时间确定
2.6. 试验验证
2.6.1. 灵敏度验证
2.6.2. 特异性验证
2.6.3. 试验样本验证
-
不同提取方法对大豆尖孢镰刀菌基因组的提取结果如表 2所示。在生物学研究中,纯基因组DNA的OD260/280比值处于1.8~1.9时,通常被视为样品DNA纯度良好的标志。该比值大于1.9,往往意味着样品可能受到了RNA或其他杂质的污染;当该比值小于1.8时,则表明样品可能存在蛋白质或酚类物质的污染情况。综合以上及数据所得,改良SDS-季铵盐法和改良SDS法提取的基因组浓度较高,但改良SDS的OD260/230值低于2时,可能有杂质污染,因此,改良SDS-季铵盐法提取效果更好。
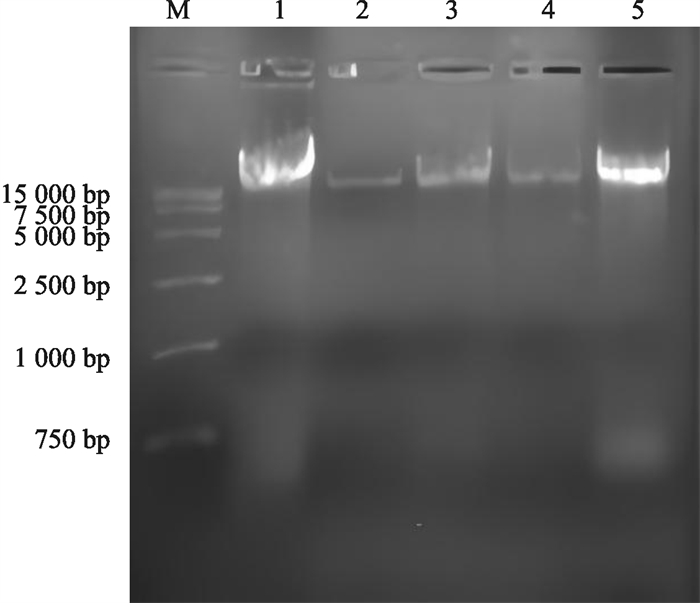
将不同种提取方法的DNA进行0.7 %凝胶电泳验证,不同提取方法的电泳结果如图 1所示。所有泳道均有条带,说明5种方法均能提取出尖孢镰刀菌DNA;第1、5泳道提取结果条带最明亮,说明改良CTAB法、改良SDS-季铵盐法均能获得较好浓度和纯度的DNA,但改良CTAB法存在少量DNA降解现象;第2、3、4泳道条带较暗,说明SDS法、改良SDS法、月桂酰肌氨酸钠法提取浓度低于其他方法,但也能满足后续PCR扩增。
-
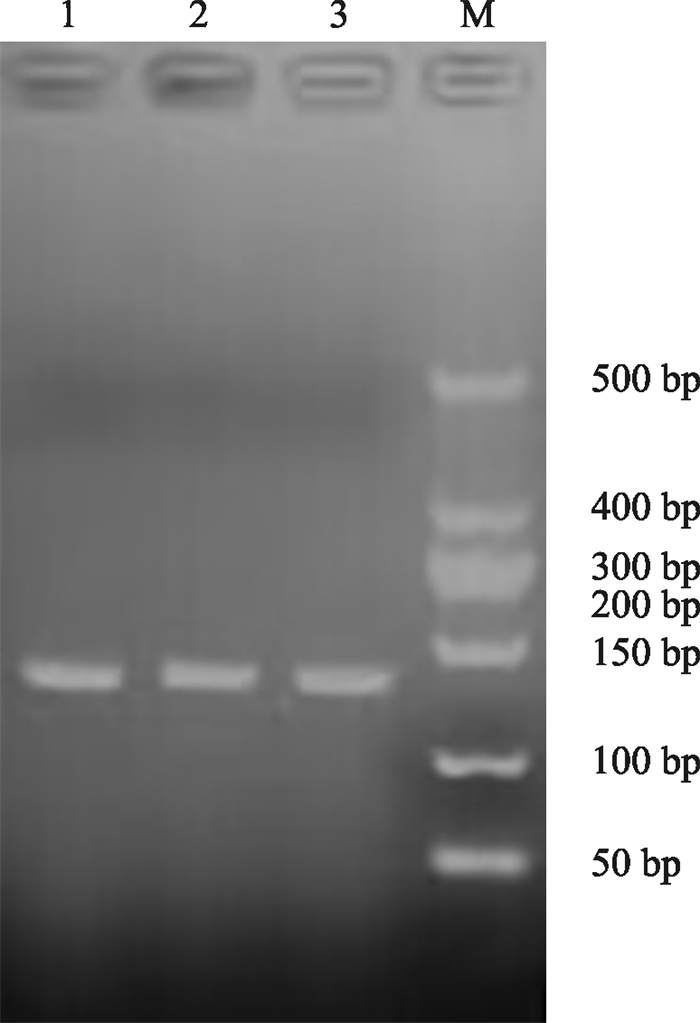
利用已知特异性引物CYP505 PCR扩增大豆尖孢镰刀菌全基因组,进行3次重复实验并电泳验证(图 2),显示结果与预期大小相符,送交生工上海生物工程有限公司测序并进行序列比对,与NCBI上大豆尖孢镰刀菌的同源性达到99%以上,满足设计RPA引物的需要。
-
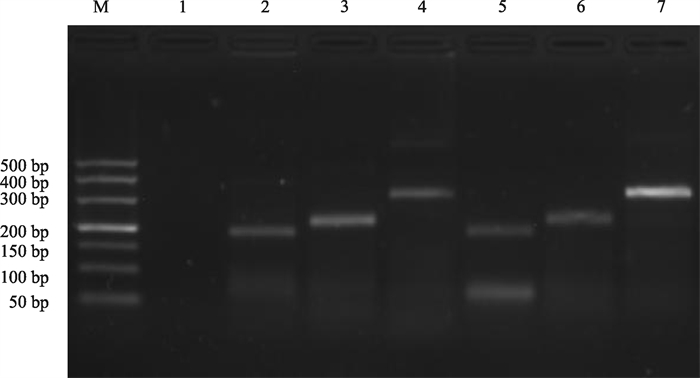
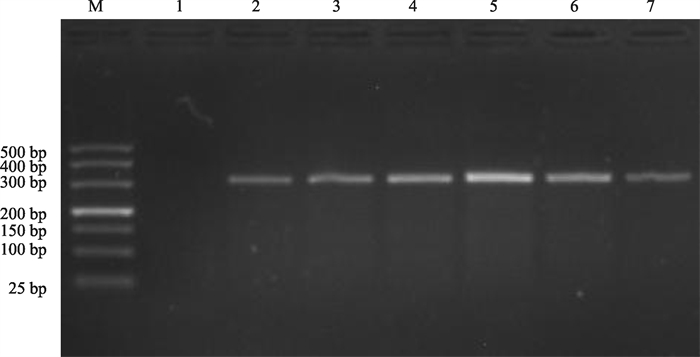
由图 3可知,参与实验的6对引物,均可扩增出特异性条带。其中,泳道2、3、4、5均出现非特异性条带,泳道6比泳道7条带较暗,扩增效果不如泳道7。经多次验证,第7泳道对应引物的扩增效果更好,由此得出最适引物对为F29/R335,扩增长度为247 bp。
-
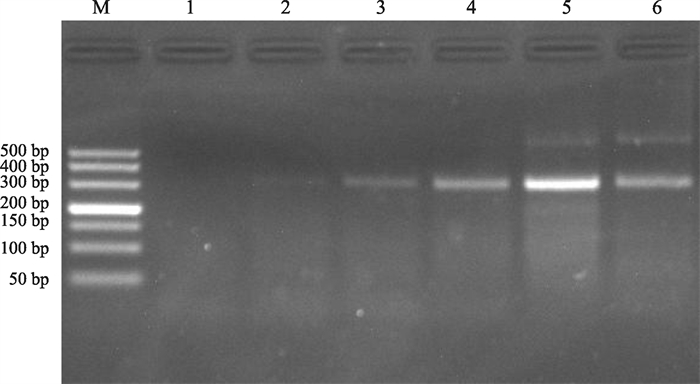
设置反应温度梯度为37 ℃、38 ℃、39 ℃、40 ℃、41 ℃、42 ℃。根据图 4显示,以上反应温度均可出现条带,但泳道5明显亮于其他条带,其中泳道2、3、4可能因为温度较低不能使酶反应充分,而泳道6、7可能因为温度较高而反应酶部分失活。综上,在泳道5的温度下,条带更亮,反应更充分,40 ℃为最优反应温度。
-
从图 5可以看出,所有泳道均出现条带,泳道2、3、4无非特异条带,其中泳道2、3条带较暗,而泳道4较于泳道2、3条带更亮,表明扩增效果更好;泳道5、6出现非特异性条带,原因可能是反应时间过长,发生了非特异性扩增。因此,最终确定最佳反应时间为20 min。
-
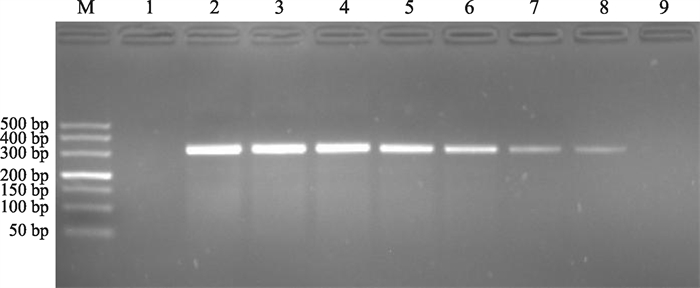
灵敏度结果如图 6,随着DNA浓度的不断降低,各泳道的亮度也在不断减弱,RPA检测方法在9×10 fg/μL的时候仍可见较浅的条带,但是到第9泳道9 fg/μL时,所拍照片肉眼观察不到条带。因此,可以得出RPA的检测限为90 fg/μL。
-
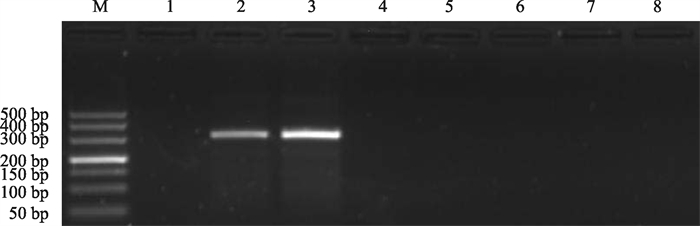
特异性验证结果如图 7所示,在相同扩增条件下,只能检测出第8泳道的大豆尖孢镰刀菌,而其他泳道的大豆疫霉菌、大豆灰斑菌、茄腐镰刀菌、东北霜霉菌、锐顶镰孢菌、腐皮镰孢菌均未出现目的条带,证明本试验具有较高的特异性。
-
试验样本验证结果如图 8所示,感染大豆疫霉菌大豆植株、大豆灰斑菌菌丝、茄腐镰刀菌菌丝、东北霜霉菌菌丝、锐顶镰孢菌菌丝均未扩增出条带,与阴性对照相同;只有第2、3泳道的感染尖孢镰刀菌大豆植株、大豆尖孢镰刀菌菌丝在实际样本验证时仍具有较强特异性。
3.1. 尖孢镰刀菌DNA提取结果
3.2. 特异性引物验证
3.3. 最优引物对筛选
3.4. 最优反应温度确定
3.5. 最优反应时间确定
3.6. 灵敏度验证
3.7. 特异性验证
3.8. 试验样本验证
-
随着大豆尖孢镰刀菌造成的减产危害愈来愈大,须及时高效地检测病害,以减少经济损失[16]。目前的检测技术有菌落平板稀释法、常规PCR、实时定量PCR,但其中存在着实验周期长,需要大型仪器的问题,不能实现快速的现场检测。本研究应用等温扩增的ERA技术建立了针对该菌的快速检测方法,并创新应用了2.5 mol/L四正丁基溴化铵与SDS相结合的方法,提取出了较好的大豆尖孢镰刀菌的基因组。季铵盐在乙醇等有机溶剂中的溶解度也更高,因此,在相同工作浓度条件下具有更低的成本,可得到浓度和纯度较好的基因组DNA。根据NCBI上下载的大豆尖孢镰刀菌基因CYP 505的特异性区段,并运用Primer 5设计了两对正向引物和三对反向引物并进行实验筛选,确认了F29/R335为最佳引物对。通过不断地优化检测体系,与其他检测植物病虫害的体系相比:在检测灵敏度方面,本研究的检测下限可达90 fg/μL,而同样应用ERA技术仅检测到10 μg/μL的样本;在检测时间方面,本试验最优反应时间为20 min,而王春伟等[5]则需要30 min。因此,本试验建立的反应体系具有更灵敏、更快速的优势。
综上,本研究应用ERA技术建立的针对大豆尖孢镰刀菌检测方法可以在常温40 ℃、20 min内即可显现结果,最低90 fg/μL时即可检出,具有操作快速、准确、灵敏的优势,可实现现场化的快速检测,为大豆尖孢镰刀菌的检测提供了一个新的方向,对于该病的田间检测和早期诊断有重要意义。





 DownLoad:
DownLoad: