-
根据国家培养创新型人才的要求,高校的人才培养不仅要培养学生扎实的专业知识和技能,更需要发挥其创新意识及创造能力. 为使材料类学生达到培养要求,综合材料实验教学是一种有效的方法[1-4]. 材料综合实验是结合所学的材料基础制备表征知识,通过综合实验的巧妙教学设计及实施,来调动学生学习的积极性、主动性和创造性,从而培养学生的创新能力和研发能力[5-8]. 综合实验的设计应向综合性创新实验及国家重大需求的研究领域倾斜[9],为此,依托郑州航空工业管理学院材料学院本科生专业实验平台及航空材料与应用技术河南省重点实验室材料表征平台,紧密围绕近代科技发展中清洁能源材料方向,涉及光催化加氢材料的制备、表征、性能测试及机理分析,面向全体材料类、化学类本科专业开设了纳米材料制备及光催化加氢性能综合实验,通过综合实验的学习,加强了材料科学基础理论知识与实践的结合度,加深了对材料结构设计及性能构效关系的理解,提高了学生的实验观察能力、实践能力和创新思维能力.
对于综合实验加氢目标产物的选择,以芳香族苯胺类化合物作为目标产物,因为芳香族苯胺类化合物及其衍生物是合成染料、聚合物高分子材料、药物等的一种重要的中间体[10],在工业生产中起着至关重要的作用. 这些中间体通常的合成方法一般是通过催化剂还原对应的芳硝基化合物获得,对于这个反应来说,有效的加氢催化剂是此反应的关键,在芳硝基化合物的催化加氢中,贵金属催化剂虽然表现了优异的催化活性,但是仍有许多不足,例如,贵金属的储量低、价格高昂、毒性较高、反应时间长、高耗能、高污染等都限制了贵金属催化剂的应用. 为了解决这些问题,人们已在不断尝试合成其他性能优良且廉价的金属催化剂,而廉价金属(如Fe,Co,Ni,Cu等)[11-16]储量丰富、价格低廉,在催化加氢领域具有很大的应用潜力,但是,廉价金属催化剂的活性一般较贵金属催化剂低很多. 另一方面,在芳硝基化合物的催化加氢中,氢源一般为氢气,氢气在反应溶液中的溶解性较低,与反应底物接触较为困难,使得硝基的还原反应进行缓慢,因此,如何提高廉价催化剂的活性并增加氢源的活性是该领域的研究重点之一. 纳米材料在光催化条件下若能够一步实现产氢并还原芳硝基化合物的串联反应,将是一种清洁快速制备芳香族苯胺类化合物的有效方法. 传统单一的半导体光催化产氢材料(例如CdS基材料)虽然具有可调带隙及较好的捕获光子能力,但是巨大的电子-空穴快速复合损失无法满足对光催化产氢的实际应用. 因此,为了解决此问题,可以尝试在CdS基材料的基础上通过添加其他元素调整带隙来改变光的吸收以及构建一维异质结构来促进空间电荷分离,借此两种途径的协同作用来提高电荷的利用效率. 一维的Cu1.94S-Zn0.23Cd0.77S是通过在CdS基材料中加入Cu和Zn两种元素来改变其带隙并形成异质结构来提高其电荷分离效率的,可满足上述功能材料集成的要求,此材料是具有单分散性的单晶材料,在可见光的照射下表现出高的产氢性能,其光解水产氢性能可达7 735 μmol/(h·g)[17]. 因此,本实验选择具有学科前沿性的一维Cu1.94S-Zn0.23Cd0.77S异质结构纳米棒作为产氢材料进行有机物的加氢实验.
全文HTML
-
1) 试剂:醋酸铜、醋酸锌、醋酸铬、十二硫醇、十二醇、油酸、硫化钠、亚硫酸钠、巯基丙酸、三氯甲烷、环己烷、甲酰胺、无水乙醇,均为分析纯. 去离子水(自制).
2) 仪器:电子天平(METTLER TOLEDO),数显式恒温磁力搅拌器(IKA RCT),鼓风式烘箱(STIK VOS-30A),高速离心机(HC-3018),数控超声清洗器(KQ-3200DE),微量移液枪(北京大龙),X射线衍射仪(Bruker D8 Advance),透射电子显微镜(Hitachi-7700),高分辨透射电镜(FEI Tecnai G2 F20 S-Twin),光催化综合测试系统(LABSOLAR-H2),气相色谱仪(GC-QP2010).
-
1) 实验流程
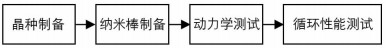
基本实验流程如图 1,包括Cu1.94S晶种的制备和Cu1.94S-Zn0.23Cd0.77S一维纳米棒异质结构材料的制备,光催化加氢动力学测试及循环性能测试4个步骤.
2) 样品制备
Cu1.94S纳米球晶种的制备:将0.24 g醋酸铜加入到盛有混合均匀的30 mL十二硫醇和30 mL十二醇三口烧瓶中,再放入油浴中,在磁力搅拌下加热至220 ℃保温8 min,自然冷却后,用环己烷和无水乙醇分别洗涤3次,将Cu1.94S分散在28 mL环己烷中备用.
Cu1.94S-Zn0.23Cd0.77S一维纳米棒异质结构材料的制备:先将0.4 mmoL醋酸锌和0.6 mmoL的醋酸铬加入到4 mL油酸中混合均匀并加热保温至110 ℃形成溶液①. 再将上述Cu1.94S晶种取出1.6 mL加入到6 mL十二硫醇与26 mL油酸混合液中保持110 ℃形成溶液②. 将2.4 mL溶液①缓慢滴加至溶液②中,保持搅拌情况下升温至250 ℃保温半小时,自然冷却,与制备上述晶种同样的方法洗涤后分散在环己烷中备用.
由于制备一维纳米棒是在油相中反应,要进行后续水相中的光催化加氢测试,必须使纳米材料表面的亲油基团置换成亲水基团,因此要进行材料表面配体交换. 将所合成的Cu1.94S-Zn0.23Cd0.77S材料分散液加入体积百分比为0.06的巯基丙酸与甲酰胺混合液搅拌半小时后,用丙酮和乙醇分别洗涤3次,离心干燥,得到Cu1.94S-Zn0.23Cd0.77S一维粉末纳米材料.
3) 物相、形貌及加氢性能测试
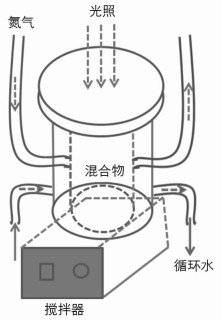
X射线衍射分析(XRD)采用Bruker D8 Advance型X射线衍射仪,配备Cu Kα辐射源λ = 1.541 8 Å进行物相分析,利用透射电子显微镜(TEM)和高分辨透射电镜进行表面形貌表征,光催化加氢测试所用仪器为光催化综合测试系统. 光催化加氢具体步骤为:取20 mg光催化剂Cu1.94S-Zn0.23Cd0.77S一维纳米棒材料和0.5 mmoL硝基苯(溶解在5 mL无水乙醇中)超声分散在50 mL 0.5 mmoL硫化钠和0.5 mmoL亚硫酸钠的水溶液中,再放入光催化加氢测试系统容器中,在N2保护下,300 W氙灯(加上只能通过可见光的滤光片)光照一定时间,加氢结果在气相色谱仪上进行测试. 图 2是光催化加氢反应装置示意图,由装有截止滤光片的氙灯光源、光催化容器、搅拌器、N2保护及冷却循环水系统组成.
1.1. 实验主要试剂与仪器
1.2. 实验方法
-
Cu1.94S纳米材料可采用简单的液相法实现球形晶种可控生长,如图 3(a)、(b)所示,从图中可以看出用该方法可以制备出直径10 nm左右,尺寸均匀的Cu1.94S球形纳米材料. 将Cu1.94S纳米材料滴在铜网上进行透射电镜观察时,由于其表面能较大,很容易自组装形成密堆积结构. Cu1.94S球形纳米颗粒直径大小具有可调性,可以通过调节溶剂中十二硫醇与十二醇比例来实现其直径大小的可控生长,该部分内容主要涉及材料分析中对电镜结果中颗粒大小的测量,有利于学生掌握如何根据材料的电镜照片并结合统计软件测量统计颗粒的大小,提高学生对所学理论知识及软件的实际应用能力.
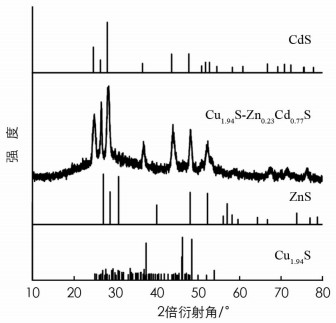
以Cu1.94S纳米球为晶种,加入一定比例醋酸锌和醋酸铬的混合溶液,通过液相外延生长的方法可制备Cu1.94S-Zn0.23Cd0.77S一维纳米棒异质结构材料,其环己烷悬浊液光学照片如图 4所示,从照片中可以观察到宏观物理颜色为黄色. 样品材料的XRD结果如图 5所示,从图中可以看出,合成样品具有六方晶结构,衍射峰的位置在标准的单斜久辉铜矿结构的Cu1.94S(JCPDS no.23-0959)、六方纤锌矿结构的ZnS(JCPDS no.80-0007)和六角硫镉矿结构的CdS(JCPDS no.70-2553)之间,说明无相分离现象,形成了固溶体的Cu1.94S-Zn0.23Cd0.77S纳米材料,Cu1.94S衍射峰强度较弱可能与相对于一维长直纳米棒其含量较低有关. 合成样品的透射电镜照片如图 3(c)、(d)所示,可以看出Cu1.94S-Zn0.23Cd0.77S材料呈一维纳米棒状,直径、长度较一致,由直径10 nm左右球状的Cu1.94S (衬度高)与80~100 nm左右棒状茎Zn0.23Cd0.77S(衬度低)组成的一维纳米棒状异质结构,其容易自组装形成密堆积结构,说明纳米棒具有大的表面能和分散性. 这种一维纳米棒异质结构能够在光照下实现快速的空穴与电子分离,提高光催化产氢效率,从而能增加有机底物的加氢性能. 一维纳米棒状异质结构的组分及长度具有可控调节性,可通过调控醋酸锌和醋酸铬的比例及加入量来实现. 该部分内容主要结合了材料科学基础、材料分析测试方法中的XRD晶体学及TEM的理论知识,通过该部分的教学有利于学生掌握XRD及透射电镜大型仪器的操作,有利于利用所学理论对实际材料的XRD及透射电镜表征结果进行分析,进而提高学生理论与实践的结合能力,在此部分教学中应该注意提醒学生大型仪器操作及在材料分析过程中的注意事项.
Cu1.94S-Zn0.23Cd0.77S一维纳米棒是由具有近红外光吸收的P型半导体Cu1.94S及具有可见光吸收活性的Zn0.23Cd0.77S所组成的异质结构材料,其高分辨透射电镜结构如图 6所示. 这种结构不仅扩大了光的吸收范围,而且有望建立起有利于空间电荷分离的亲密接触异质界面. 一维单晶Zn0.23Cd0.77S由于其复合中心(例如晶界或缺陷)比多晶少,因此是一种理想的可用于超快电荷迁移的纳米结构,此结构可实现光催化组分与功能异质结构的协同效应,为利用纳米科学技术优化光催化性能提供了有效途径. 这种结构在可见光的照射下,Cu1.94S-Zn0.23Cd0.77S纳米棒半导体带隙激发产生价带空穴和导带电子分离,Cu1.94S将空穴从Zn0.23Cd0.77S传给牺牲剂Na2S和Na2SO3消耗,同时H2O形成H+和·OH自由基(h++H2O→h++·OH),生成的·OH自由基也会被牺牲试剂快速消耗. 与此同时,电子被分离出来并在一维异质纳米结构中快速传递,最终扩散到半导体材料表面与2H+在硝基苯底物上进行结合生成亚硝基苯及水;随后,同样的过程发生在亚硝基上产生羟胺;最后,羟胺与2e-及2h+快速生成苯胺. 这一过程是从水中直接原位产生的H+活性物种及表面的电子实现同步加在硝基苯上形成苯胺完成加氢反应的. 同时,Cu1.94S半导体光照所分离出来的电子,同样会被分布在半导体的表面,有利于加氢反应的进行,这种独特的纳米棒异质结构有利于电荷分离,决定了其光催化加氢的良好性能. 光催化加氢反应过程避免了普通催化剂加氢过程中的氢分子先解离再加成的过程,也避免了高温高压的苛刻反应条件,同时采用的非贵金属催化剂也降低了催化成本,所以利用Cu1.94S-Zn0.23Cd0.77S半导体光催化材料进行加氢反应是一种行之有效且环境友好的科学方法. 该部分理论分析主要反映学生在材料结构与性能课程中所学的有关光催化性能部分的理论知识,通过引导学生结合材料的微观结构对光催化加氢产生过程的理论分析,加深其对材料结构与性能之间构效关系的认识和理解,有利于培养学生的思维能力与综合创新能力,提高其对材料微观世界的认知,这部分教学过程中应侧重引导学生对材料性能本质微观理论的分析,培养学生对科学真理的追求.
为了检验所制备的一维光催化材料的光催化加氢性能,首先将合成出的Cu1.94S-Zn0.23Cd0.77S一维光催化材料进行配体交换,目的是为了将油相合成的样品转变成亲水的光催化材料,随后将配体交换后的烘干样品进行光催化测试. 取20 mg干燥的Cu1.94S-Zn0.23Cd0.77S纳米棒材料,0.5 mmoL硝基苯为底物,0.5 mmoL的硫化钠与0.5 mmoL的亚硫酸钠为牺牲剂进行超声分散均匀,在溶液温度达到10 ℃时,打开氙灯光源,可见光照射反应一定时间,用乙酸乙酯进行萃取,取少许萃取液稀释后进行底物转化率的检验. 硝基苯转化为苯胺的转化率用气相色谱法进行检测,硝基苯随时间转化为苯胺的转化率如表 1所示,从表中可以看出,生成苯胺的量随时间的增加迅速增长,在反应进行30 min时,硝基苯的转化率超过了90%,当时间达90 min,硝基苯即可基本完全转化为苯胺(转化率为99.44%),此过程中的选择性均为100%. 说明在可见光照射下,即使在较低的温度仍然能实现催化材料的高活性和选择性,与Cu1.94S-Zn0.23Cd0.77S一维光催化材料的异质纳米结构有利于电子与空穴的分离有关,因此,Cu1.94S-Zn0.23Cd0.77S一维纳米棒是一种能在温和条件下,实现硝基苯高活性和高选择性一步光催化加氢的纳米材料. 此部分涉及材料性能分析中的动力学分析,通过对材料反应性能中间过程的分析,观察中间过程材料性能随相关参数的变化规律,从而确定有效的分析材料性能的方法,这也是材料分析中常用的方法之一. 通过中间过程分析,可培养学生实验观察能力、探索能力及逻辑思维能力,在实验学习过程中,注意引导学生掌握对材料合成动力学及反应动力学过程的分析设计技巧.
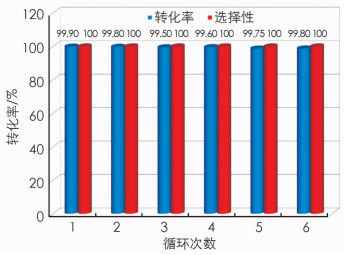
催化反应在实际应用中,循环稳定性是反映材料催化活性的一种非常重要的评价指标. 因此,在上述的催化反应条件的基础上,对Cu1.94S-Zn0.23Cd0.77S一维纳米棒异质结构材料的光催化硝基苯加氢生成苯胺的循环稳定性进行了测试,结果如图 7所示. 从图中可以看出,在6次循环中其活性及选择性均得到了很好的保持,都保持在99%以上. 在此光催化的循环反应中,并不需要对催化剂进行离心、分离和洗涤,只需要用乙酸乙酯进行萃取后,即可继续加底物进行下一次的反应,这样避免了催化剂的浪费及繁琐的洗涤分离程序. 在循环测试时,催化剂没有进行任何的处理或者激活,说明了该催化剂具有稳定的可循环性能,其光催化加氢性能实验还可以进行催化底物的扩展,例如含有硝基苯环的其他类衍生物的催化加氢反应(含卤素、羟基、甲基等官能团). 因此,Cu1.94S-Zn0.23Cd0.77S一维纳米棒异质结构光催化材料表现出了良好的催化活性、选择性及循环稳定性能,同时拥有异质催化剂的特性,在化学工业上具有潜在应用价值. 该部分材料的循环性能反映了材料实际应用过程中的使用寿命,是在众多材料性能分析中都涉及到的. 通过该部分的学习,有利于学生认识到在进行材料结构设计时,要充分考虑材料的循环寿命问题,提高其对所学材料理论到实际应用过程的认识,在教学过程中,强调材料循环寿命的重要性,可通过举例(例如电动汽车中电池的循环使用)加深学生对材料循环寿命在实际应用中的认识.
该实验可作为材料类、化学类本科生的综合实验项目,需要学生具备材料合成技术、材料科学基础、材料测试技术及材料结构与性能的基础理论知识. 因此,在已学完该部分知识的大三下学期开展该综合实验的教学活动,该综合实验总共8个学时,前4个学时主要针对Cu1.94S-Zn0.23Cd0.77S一维纳米棒光催化材料的合成及表面配体交换,后4个学时主要针对其进行透射电镜及光催化性能的测试、表征和分析.
-
本实验通过简单的液相法成功地合成了Cu1.94S-Zn0.23Cd0.77S一维纳米棒光催化材料,该材料具有Cu1.94S与Zn0.23Cd0.77S结合的一维异质纳米结构,将此材料成功应用于硝基苯的光催化加氢反应,即使在较低的温度下(10 ℃),90 min即可将硝基苯加氢基本完全转化为苯胺,且具有较高的活性、选择性及循环稳定性能,为高性能和环境友好的光催化材料的制备、设计提供了新的思路和手段. 通过透射电子显微镜、光催化综合测试仪器及气相色谱仪的应用,使学生掌握材料表征及光催化的测试方法,通过该实验的学习,有助于巩固学生的专业课程基本理论知识,加深对材料结构与性能之间构效关系的理解. 在该综合实验的基础上,对于有兴趣和精力的同学可以进行实验的拓展创新,比如进行一维光催化新材料的设计、成分可控调节、微量贵金属掺杂或改性等,为学生参加全国大学生挑战杯、互联网+、创新创业大赛、材料专业竞赛等活动做准备. 该综合实验不仅有利于教师将自己的科学研究与教学紧密结合,让学生了解到材料领域的科学前沿知识,也有助于培养本科生的科学思维及综合创新能力.



 下载:
下载: