-
开放科学(资源服务)标识码(OSID):

-
兔肉具有高蛋白、高赖氨酸、高磷脂、低脂肪、低胆固醇的特点,既易于消化吸收,又能降低血脂,被誉为“美容肉”与“保健肉”[1]。近年来,玉米、豆粕等传统原料价格居高不下,饲料成本占养殖总成本的比重逐年攀升,成为制约兔产业发展的关键因素。在此背景下,开发新型工业副产品替代饲料已成为畜牧业降本增效的重要突破口。木薯被誉为“淀粉之王”,广泛用于生产淀粉、生物乙醇、饲料等生物产品。然而,木薯的粗蛋白质(CP)含量较低,营养成分不均衡,作为动物饲料使用存在局限性[2]。此外,木薯中的生氰糖苷亚麻苦苷在水解时会产生对动物有毒的氢氰酸,这种毒素可以通过粉碎、发酵或加热来消除[3]。木薯酒精渣(Cassava Alcohol Residue,CAR)是木薯生产燃料酒精的副产物,含纤维素、木质素及少量的蛋白质和脂肪[4]。经微生物发酵处理后,CAR的粗蛋白质含量显著提升,氢氰酸含量可有效降至安全阈值以下,从而实现饲料成本降低、畜禽生长性能改善及免疫功能增强的综合效益[5]。虽然木薯加工副产物年产量较高,但当前的综合利用率仍处于较低水平。CAR的资源化利用不仅能显著降低饲料成本,还可有效降低环境污染,实现经济、生态双重效益。研究表明,饲料中添加发酵木薯渣可增加蛋鸡的采食量、降低饲料成本[6],提高育肥猪的日增重[7],增强饲料适口性并改善奶牛的瘤胃发酵特性[8]。然而,现有研究多集中于反刍动物,针对肉兔的饲用研究较少。鉴于此,本试验通过探究CAR对肉兔生长性能、养分表观消化率和肌肉品质的影响,旨在为其在肉兔产业的应用提供科学依据。
全文HTML
-
木薯酒精渣(CAR)购自金源生物科技有限公司。
-
将160只体重相近的35日龄雄性伊拉肉兔随机分成4组,每组5个重复,每个重复8只肉兔。在各处理组的日粮中分别添加0%(对照组)、8%、16%和24%的CAR,肉兔在试验期间均可自由采食和饮水。试验期为35 d,其中预饲期7 d,正试期28 d。肉兔基础日粮组成及营养水平分别见表 1、表 2。CAR的营养水平见表 3。
-
干物质(DM)依据《饲料中水分的测定》(GB/T 6435—2014)方法测定,粗蛋白质(CP)依据《饲料中粗蛋白的测定凯氏定氮法》(GB/T 6432—2018)方法测定,粗脂肪(EE)依据《饲料中粗脂肪的测定》(GB/T 6433—2006)方法测定,粗灰分(Ash)依据《饲料中粗灰分的测定》(GB/T 6438—2007)方法测定,粗纤维(CF)依据《饲料中粗纤维的含量测定》(GB/T 6434—2022)方法测定,酸性洗涤纤维(ADF)依据《饲料中酸性洗涤纤维的测定》(NY/T 1459—2022)测定,中性洗涤纤维(NDF)依据《饲料中中性洗涤纤维(NDF)的测定》(GB/T 20806—2022)测定,钙(Ca)依据《饲料中钙的测定》(GB/T 6436—2018)方法测定,磷(P)依据《饲料中总磷的测定分光光度法》(GB/T 6437—2018)方法测定。
-
在试验第1、15和29 d的08:00对肉兔进行空腹体重称量,并计算各阶段的平均日采食量(ADFI)、平均日增重(ADG)和料重比(F/G)。
-
从试验第16 d起,将外源指示剂二氧化钛添加到日粮中,并在各处理组中随机采集250 g日粮,保存于4 ℃冰箱中。在试验结束前5 d清除粪球上的兔毛并收集粪样。将采集的粪样分成两份,一份加入10%的硫酸固氮测定粗蛋白质,另一份用于测定常规营养成分。养分表观消化率=[1-(粪中某营养物质含量/粪中二氧化钛含量)]/(日粮中某营养物质含量/日粮中二氧化钛含量)×100%。
-
每个处理组随机选取10只肉兔进行心脏采血,采血后3 000 r/min离心10 min制备血清,-20 ℃保存待测。使用DXC 800型生化仪分析测定血清中碱性磷酸酶(ALP)的活性和总蛋白(TP)、总胆固醇(TC)、血清白蛋白(ALB)、甘油三酯(TG)、尿素氮(BUN)、葡萄糖(GLU)、Ca、P的含量。
-
取肉兔背最长肌样本分装并保存于4 ℃冰箱待测。熟肉率:将2.5 cm厚的肉块称重,将其蒸煮后取出冷却,吸去水分后称量。熟肉率=蒸煮后重量/蒸煮前重量×100%。失水率:称取10 g样品,在8 000 r/min条件下离心30 min,取出样品吸去水分后称量。失水率=[(离心前重-离心后重)/离心前重]×100%。pH值的测定:取0.5 g样品和10倍体积的生理盐水放入离心管中进行混合,匀浆后再用酸碱度计测定pH值。肉色:采用Ultra Scan PRO测色仪测定屠宰后肉样的亮度(L*)、红度(a*)和黄度(b*)。肉兔背肌DM、CP和Ash含量参照AOAC方法测定[9]。
-
参照文献[10]的方法用Shimadzu GC-A型气相色谱仪测定肉兔背肌脂肪酸的含量。
-
通过SPSS 27.0将数据进行单因素方差分析,并用Duncan's法进行多重比较,使用GraphPad Prism 9对数据进行绘图,结果用“平均值±标准差”表示。*或p<0.05表示差异显著,p>0.05表示差异不显著。
1.1. 试验材料
1.2. 试验设计
1.3. 样品采集及分析方法
1.3.1. 营养水平测定方法
1.3.2. 生长性能
1.3.3. 常规养分表观消化率
1.3.4. 血清生化指标
1.3.5. 肌肉品质和营养成分测定
1.3.6. 肌肉脂肪酸含量
1.4. 数据分析
-
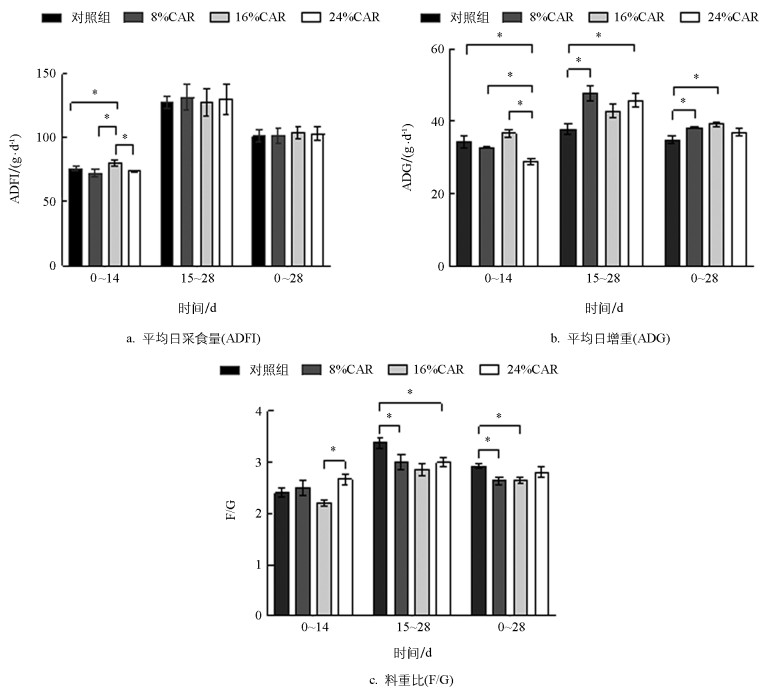
如图 1所示,16%CAR处理组0~14 d的ADFI显著高于对照组、8%CAR处理组和24%CAR处理组(p<0.05),但各处理组15~28 d和0~28 d的ADFI均未表现出显著性差异(p>0.05)。24%CAR处理组在0~14 d的ADG显著低于对照组、8%CAR组和16%CAR处理组(p<0.05);8%CAR处理组和24%CAR处理组在15~28 d的ADG显著高于对照组(p<0.05);8%CAR处理组和16%CAR处理组在0~28 d的ADG显著高于对照组(p<0.05)。就F/G而言,24%CAR处理组在0~14 d显著高于16%CAR处理组(p<0.05);8%CAR处理组在15~28 d与0~28 d,16%CAR处理组在0~28 d,24%CAR处理组在15~28 d均显著低于对照组(p<0.05)。
-
如表 4所示,24%CAR处理组CP的表观消化率显著低于对照组、8%CAR处理组和16%CAR处理组(p<0.05)。各CAR处理组Ash的表观消化率显著低于对照组(p<0.05),且24%CAR处理组显著低于8%CAR处理组和16%CAR处理组(p<0.05)。8%CAR处理组、24%CAR处理组中性洗涤纤维(NDF)的表观消化率显著高于对照组和16%CAR处理组(p<0.05)。CAR对ADF和DM的表观消化率无显著影响(p>0.05)。8%CAR处理组、16%CAR处理组Ca的表观消化率显著高于对照组和24%CAR处理组(p<0.05)。24%CAR处理组P的表观消化率显著低于对照组、8%CAR处理组和16%CAR处理组(p<0.05)。
-
如表 5所示,24%CAR处理组ALP含量显著低于对照组、8%CAR处理组、16%CAR处理组(p<0.05)。16%CAR处理组和24%CAR处理组ALB含量显著高于对照组和8%CAR处理组(p<0.05),且16%CAR处理组ALB含量显著高于24%CAR处理组(p<0.05)。16%CAR处理组、24%CAR处理组GLU含量显著低于对照组和8%CAR处理组(p<0.05)。24%CAR处理组BUN含量显著低于对照组和16%CAR处理组(p<0.05),且8%CAR处理组显著低于对照组(p<0.05)。24%CAR处理组TP含量显著高于8%CAR处理组(p<0.05)。CAR对血清TC、TG、Ca和P无显著影响(p>0.05)。
-
如表 6所示,8%CAR处理组背肌L*显著高于16%CAR处理组和24%CAR处理组(p<0.05)。各CAR处理组a*值和b*值均显著低于对照组(p<0.05)。各处理组背肌pH、熟肉率和失水率的差异不显著(p>0.05)。16%CAR组背肌DM含量显著高于8%CAR组(p<0.05)。各处理组背肌Ash、CP含量均未达到显著差异(p>0.05)。
-
如表 7所示,16%CAR处理组、24%CAR处理组背肌肉豆蔻酸(C14:0)和花生酸(C20:0)含量显著低于对照组和8%CAR处理组(p<0.05),且8%CAR处理组C14:0和C20:0分别显著低于和高于对照组(p<0.05)。16%CAR处理组背肌棕榈酸(C16:0)和硬脂酸(C18:0)含量显著高于对照组(p<0.05),且C18:0含量也显著高于8%CAR处理组和24%CAR处理组(p<0.05)。
各处理组背肌的饱和脂肪酸(SFA)总量的差异不显著(p>0.05)。各CAR处理组背肌油酸(C18:1n-9c)含量显著高于对照组(p<0.05)。16%CAR处理组、24%CAR处理组背肌的单不饱和脂肪酸(MUFA)总量显著高于对照组和8%CAR处理组(p<0.05),且16%CAR处理组显著高于24%CAR处理组(p<0.05)。16%CAR处理组背肌反式亚油酸(C18:2n-6t)含量显著高于对照组和24%CAR处理组(p<0.05)。24%CAR处理组背肌二十碳三烯酸(C20:3n-3)含量显著低于对照组、8%CAR处理组和16%CAR处理组(p<0.05)。16%CAR处理组背肌的不饱和脂肪酸(UFA)总量、多不饱和脂肪酸(PUFA)总量、多不饱和脂肪酸与饱和脂肪酸的质量比显著高于对照组、8%CAR处理组和24%CAR处理组(p<0.05)。
2.1. 木薯酒精渣对肉兔生长性能的影响
2.2. 木薯酒精渣对肉兔养分表观消化率的影响
2.3. 木薯酒精渣对肉兔血清生化指标的影响
2.4. 木薯酒精渣对肉兔肌肉品质和营养水平的影响
2.5. 木薯酒精渣对肉兔肌肉脂肪酸组成的影响
-
研究表明,发酵木薯渣不会影响荷斯坦杂交犊牛的瘤胃特性与饲料利用率,但能增加微生物蛋白质合成速率,可作为反刍动物的蛋白质来源,提高牛的日增重[11-12]。Lei等[13]发现,在饲料中加入CAR可以降低抗营养作用,增加蛋白质等营养物质的含量,提高肉鸭的生长性能。Wang等[14]指出,在生长猪的日粮中添加15%苜蓿草粉会显著降低F/G,并且能提高盲肠中的丁酸浓度,增加肠道菌群的均匀度。在本试验中,与对照组相比,16%CAR处理组在0~14 d的ADFI显著升高,而24%CAR处理组的ADFI有降低的趋势,与上述研究基本一致。这是因为木薯在发酵过程中会产生醇类、醛类和酯类等挥发性芳香物质,从而改善木薯的适口性和风味,增加动物采食量[15]。然而,当CAR添加量超过16%时,挥发性物质对嗅觉和味觉的刺激作用占主导,但超过该阈值后,过量的纤维通过迷走神经传导引起胃部扩张信号增强,导致动物在进食后产生更强的饱腹感,从而减少其饲料摄入量[16]。值得注意的是,各处理组在15~28 d和0~28 d的ADFI没有差异,可能是因为肉兔的盲肠微生物能通过调节厚壁菌门与拟杆菌门来增强纤维分解能力,有助于维持肠道屏障功能并促进营养物质的吸收转化[17]。此外,8%和16%CAR处理组在0~28 d的ADG均高于对照组,F/G均低于对照组。其原因可能是发酵饲料中富含大量有机酸和维生素等活性物质,这些活性物质会提高饲料的营养价值,促进肉兔生长发育[18]。而24%CAR组的F/G未显著改善,可能与其不溶性纤维含量过高有关。当CAR添加量大于16%时,纤维基质形成的物理屏障会降低消化酶与底物的接触效率,同时未被消化的纤维在后肠过度发酵导致能量损失增加,进而减缓肉兔的生长速度[19]。
-
养分表观消化率可以评估动物对饲料的消化吸收能力。本试验中,各CAR处理组的DM和Ash的表观消化率均有一定程度的下降,其中24%CAR处理组的DM和CP的消化率较对照组分别降低2.7%和8.5%。这一现象与CAR的高纤维特性直接相关:高含量的粗纤维会形成物理屏障,减少消化酶与底物的接触机会[20];可溶性纤维含量高导致食糜粘度升高,延缓食糜通过速率,进而缩短小肠的有效吸收时间[21];高黏度环境刺激杯状细胞分泌黏蛋白(Muc2),加速肠黏膜细胞脱落并增加内源性氮损失,进而抑制CP消化率和生长性能[22]。上述机制与朗德鹅研究中高纤维含量会抑制能量、CP和粗脂肪消化率的结论一致[23]。值得注意的是,尽管16%CAR处理组的DM消化率较对照组下降,但肉兔的ADG仍提高,这可能是CAR发酵产生的短链脂肪酸(SCFAs)通过激活肝脏PPARγ通路,提升脂肪酸氧化效率,同时盲肠纤维分解能力增强,部分补偿了纤维导致的能量损失[24]。而24%CAR处理组因纤维抑制效应过强,其F/G改善幅度显著低于8%和16%CAR处理组[25]。
-
血清ALP主要来源于动物的骨组织,其活性升高有利于提高动物的ADG[26]。在本研究中,8%和16%CAR处理组的ADG和ALP均有一定程度的上升,这说明CAR中的纤维物质发酵产生的SCFAs能激活成骨细胞PPARγ通路,促进焦磷酸盐和吡哆醛-5-磷酸等多种底物水解释放磷酸基团加速骨骼矿化,进而加快肉兔的生长速度并增加体重[27]。然而,24%CAR处理组因纤维含量过高(NDF超过43.74%)形成物理屏障抑制钙磷吸收,导致ALP活性显著下降。GLU能给生物体细胞提供能量和碳源,对于维持生物体的正常功能至关重要。Powthong等[28]指出,饲料中纤维含量升高会降低GLU和脂质的吸收及分解率,防止进食后血糖和胆固醇水平过高。本研究显示,16%和24%CAR处理组血清GLU较对照组降低,源于可溶性纤维吸附GLU并抑制α-淀粉酶和α-葡萄糖苷酶活性,减少酶与底物的接触面积,从而降低血清GLU[29]。但16%CAR处理组可以通过SCFAs激活肝脏糖异生维持能量平衡[30],而24%组因食糜黏度升高,延缓GLU向肠上皮细胞扩散[21]。
血清TP具有维持机体正常免疫功能和调节组织液平衡的作用[31]。本试验中,与对照组相比,8%CAR处理组血清TP含量有一定程度的下降,这可能是8%CAR处理组的饲料对胃肠道的刺激较小,未能有效激活肠道菌群调控肝脏蛋白合成[32]。雷帕霉素的机制靶标(mTOR)信号通路能通过激活下游蛋白S6K1参与细胞分化、增殖和蛋白质合成。16%CAR处理组的肉兔能通过厚壁菌门的代谢产物丁酸刺激mTOR通路使机体TP恢复至正常水平[33-34]。BUN是体内蛋白质代谢的终产物,较低的BUN能反映动物良好的生长性能[35]。本试验中,各CAR处理组的BUN含量均有不同程度的下降,表明CAR处理组肉兔的生长性能有所提升。其原因可能是CAR中的纤维发酵促进盲肠微生物增殖,增强氨氮固定,同时SCFAs降低肠上皮通透性,减少BUN肠肝循环吸收[36]。
-
肉品质主要通过失水率、pH值和熟肉率等指标进行评估,其优劣直接影响消费者的购买欲望。肉品质受到动物饲养管理、日粮结构和营养水平等多种因素的影响。Broch等[37]指出,饲喂干木薯渣对鸡胸肉的pH值和失水率没有影响。Fasae等[38]的研究也表明,饲料中添加不同含量木薯干草对西非侏儒羊肉质的蒸煮损失和pH值没有显著差异。本试验与前人的研究结果一致。肌肉的a*值与肌红蛋白含量有关,a*值越高表明肉的品质越好[39]。本研究中,与对照组相比,各CAR处理组的a*值降低,但16%CAR处理组的a*值降幅最小,这一现象可能是CAR发酵产生的SCFAs能促进肌肉多不饱和脂肪酸(PUFA)沉积,易受肌红蛋白高度氧化的影响,使肌肉更容易发生氧化反应,导致a*值下降[40]。研究表明,PUFA沉积增加与抗氧化能力提升能协同维持肉色稳定性。盲肠发酵产生的丁酸通过激活Nrf2通路增强肌肉抗氧化能力,但过量纤维会因纤维抑制效应过强导致抗氧化物质吸收受阻,加剧脂质氧化,促使氧合肌红蛋白向高铁肌红蛋白转化,从而影响肌肉的颜色和品质[41]。
水分、粗脂肪和CP是肌肉组织的主要营养成分,能反映肌肉品质的色泽、口感和质构特性[42]。文献[43]的研究表明,添加木薯粉的湿啤酒残渣青贮饲料对羔羊腿肌的Ash和CP水平无影响。此外,Abrahāo等[44]也发现,用木薯淀粉提取湿残渣替代玉米后,肌肉中Ash和CP的含量没有差异。本研究与上述结果相似,说明在饲粮中添加CAR对肉兔肌肉的营养水平无负面影响。
-
肌肉中脂肪酸的组成和比例直接影响肉的风味及营养价值,而肌内脂肪(IMF)作为决定肉质的重要指标,其含量越高,肉的适口性通常越好[45]。本试验肉兔背肌中脂肪酸的组成、含量与文献[46]报道的类似。研究表明,肌肉的风味主要由UFA氧化后产生的酮、醛、醇、呋喃、吡嗪和噻吩等物质来决定[47],而脂肪的硬度与其所含脂肪酸的熔点密切相关。Pewan等[48]指出,MUFA的熔点低于SFA,这种特性会使肉的风味、嫩度和多汁性提高。研究表明,PUFA是对人类有益的脂肪酸,具有影响炎症过程、减少氧化应激和保护心血管等多种生物学作用[49],其含量增加有助于改善肉的风味和脂质氧化[50]。C18:2n-6t是哺乳动物合成长链PUFAs的前体,可通过上调肝脏中低密度脂蛋白(LDL)受体活性、蛋白质和mRNA来降低血液中总胆固醇和LDL的水平,从而减少患动脉粥样硬化和相关心脏疾病的风险[51]。本试验中,与对照组相比,各CAR处理组背肌C18:1n-9c含量和C18:2n-6t含量显著升高,且16%CAR处理组背肌的C20:3n-3、MUFA总量和PUFA总量也显著增加,其机制在于CAR发酵产生丙酸等SCFAs激活PPARγ/CEBPα信号通路,上调脂蛋白脂肪酶表达,从而促进脂肪细胞分化与IMF沉积[52]。这种调节效应在8%CAR处理组表现较弱,而24%CAR处理组因纤维抑制效应过强,导致维生素E等脂溶性维生素吸收受阻,引发氧化应激,反而削弱PUFA沉积优势。然而,富含纤维的饲料和发酵饲料在调节肉品质方面起着关键作用。Cardoso等[47]指出,用木薯渣代替玉米饲喂羔羊可以改善羊肉中的UFA含量并增强其肌肉风味。Ma等[53]发现,在饲料中添加紫花苜蓿干草可显著增加腰最长肌IMF中MUFA和背膘中PUFA比例并降低SFA的含量,从而提高猪肉品质。此外,Choi等[54]研究表明,发酵饲料可增加母猪脂肪生成基因CEBPα、PPARγ、SREBP1和FABP4等的mRNA表达量,从而改善肉质和脂肪酸组成。
肉类中PUFA和SFA的比例是用于评估肉类营养和健康价值的最重要因素,其推荐范围为大于等于0.4[50, 55]。以往有研究表明,SFA摄入量与心血管疾病发病率之间存在很强的正相关关系[50]。在本研究中,16%CAR处理组背肌PUFA与SFA的比值大于推荐范围,这说明CAR中的可溶性纤维通过吸附胆汁酸,减少肠道SFA重吸收,促进机体合成有益脂肪酸[56]。据报道,FASN基因编码的脂肪酸合酶是一种蛋白质复合物,可控制长链脂肪酸的从头生物合成,其中编码硫酯酶结构域的4个外显子通过水解酰基-S-磷酸二甲酸硫酯催化脂肪酸合成,其产物以C16:0为主,而C14:0的合成量可以忽略不计。另外有一项研究表明,C14:0和C16:0能生成少量胆固醇,其中C14:0导致动脉粥样硬化或高胆固醇血症的风险是C16:0的5~6倍[57]。本试验中,16%CAR处理组C16:0含量升高,这可能是因为盲肠厚壁菌代谢产生的丁酸能上调肝脏FASN基因表达,促进C16:0合成。此外,丁酸通过抑制HDAC活性提高组蛋白乙酰化水平,诱导染色质开放与转录激活,进而促进脂肪酸合成通路的表达,上调CEBPα、PPARγ和FABP4等脂质代谢关键基因,提高PUFA的沉积与转运效率。这种代谢调控网络使16%CAR组在维持IMF适口性的同时,显著提升营养健康价值。
-
综上,肉兔饲喂CAR能增加ADG并降低F/G,改善其ALP、GLU、TP和BUN等血清生化指标及肌肉品质,同时不会影响DM和ADF的表观消化率。在本实验条件下,日粮中添加16%的CAR可提高肉兔的生长性能,优化肌肉脂肪酸组成。



 下载:
下载: