-
开放科学(资源服务)标识码(OSID):

-
辣椒(Capsicum annuum)作为一种重要的香料作物,我国辣椒种植总面积超过1 500 km2[1],是世界第二大辣椒生产国,占全球辣椒总产量的24%[2]。由炭疽菌属复合体引起的炭疽病高发期多集中在雨季,每年7月中旬至8月中旬最为严重,可导致我国辣椒产量损失高达40%[3]。
胶孢炭疽菌作为我国辣椒炭疽菌属物种中的优势种之一[4],适宜在温度25~28 ℃、相对湿度高于95%的条件下生长[5];其分生孢子和菌丝体可通过种子、水流和气流等途径传播[6],并在种子或土壤中的植物残体上越冬[7]。在侵染过程中,胶孢炭疽菌首先在生物营养阶段形成黑色化附着胞以穿透寄主表皮,并形成胞外囊泡和初级菌丝;随后,坏死性的次生菌丝进一步扩展并侵染邻近细胞,最终导致感染部位出现明显病斑,并在感染组织表面形成大量孢子[8]。典型的炭疽病症状多在成熟辣椒果实上显现,表现为凹陷的坏死斑点,周围常伴有明显的黑色同心轮纹。现有化学药剂虽然能够抑制菌丝生长,但对孢子萌发和诱导宿主抗性的作用有限,且长期使用易导致病原菌产生抗药性[3]。
近年来,随着对天然产物次生代谢产物研究的不断深入,基于天然化合物结构优化开发的绿色农药逐渐受到关注。南开大学汪清民教授团队与山东京博农化科技股份有限公司合作开发了抗植物病毒化合物氯吲哚酰肼(Chloroinconazid,CHI),并于2025年在柬埔寨成功获得新农药登记证,商业化进展顺利[9]。CHI作为一种新型四氢-β-咔啉衍生物类绿色植物源农药,已被证明具有广谱抗病毒和抗菌活性。与常规防治药剂不同,CHI对植物株高、根长等主要生长性状未表现出明显毒性或不利影响[6]。然而,CHI对胶孢炭疽菌的抑制作用仍缺乏系统研究。本研究旨在评估CHI对胶孢炭疽菌的抑制活性及其对辣椒炭疽病的防控效果,以期揭示CHI通过干扰病原菌生殖发育并增强植物抗性的双重防控机制,为辣椒炭疽病的可持续治理提供新的策略。
全文HTML
-
辣椒种子为“遵辣一号”,由贵州省农业科学院馈赠;供试辣椒植株在温室条件下培养,室温为25 ℃,相对湿度为75%,光照周期为光照14 h/黑暗10 h;供试青椒购自山东临沂菜市场,果实成熟,完好无损。
-
PDA培养基:200 g土豆、20 g葡萄糖、20 g琼脂、1 000 mL ddH2O。
10% V8固体培养基:10 mL V8汁、90 mL ddH2O、0.02 g CaCO3、2 g琼脂。
10% V8液体培养基:50 mL V8汁、0.5 g CaCO3、90 mL ddH2O。
-
辣椒胶孢炭疽菌菌株由西南大学植物保护学院植物免疫与病害生态防控实验室提供。
-
氯吲哚酰肼(CHI)购自山东京博农化科技股份有限公司;苯醚甲环唑(Difenoconazole)购自天津市汉邦植物保护剂有限责任公司。
-
通过预试验筛选合适的质量浓度梯度,将CHI用二甲基亚砜(Dimethyl Sulfoxide,DMSO)配制成1 000 μg/mL母液,并加入PDA培养基中,使其最终质量浓度分别为40、50、160、200、240、320、400、800 μg/mL,每个质量浓度设3个重复。以83 μg/mL苯醚甲环唑作为阳性对照,0.1% DMSO作为阴性对照,无菌水作为空白对照。
将辣椒炭疽病菌株接种于PDA培养基上,在28 ℃恒温黑暗条件下培养5 d。随后用直径5 mm的打孔器从菌落边缘切取菌饼,并接种于含相应药剂的PDA培养基中央,继续在28 ℃黑暗条件下培养7 d。
-
辣椒炭疽菌产孢量试验中孢子悬浮液的制备:以无菌水作为空白对照,苯醚甲环唑作为阳性对照,将纯化后的辣椒胶孢炭疽菌接种于含药PDA培养基上,并在28 ℃黑暗条件下培养7 d。随后向每个培养皿中加入5 mL无菌水,洗脱菌落表面的孢子以制备孢子悬浮液[8]。
辣椒炭疽病菌孢子萌发试验中带药孢子悬浮液的制备:将纯化后的辣椒胶孢炭疽菌接种于PDA培养基上,在28 ℃黑暗条件下培养7 d。加入5 mL ddH2O洗脱菌落分生孢子,并以0.1%葡萄糖溶液作为原药溶液制备孢子悬浮液。孢子萌发试验参考《农药室内生物测定试验准则杀菌剂》(NY/T 1156.1—2006)孢子萌发法,将孢子悬浮液与药液按体积比1∶1混匀,以无菌水处理为空白对照,83 μg/mL苯醚甲环唑为阳性对照,每个处理设3个重复。取200 μL混合液滴于灭菌凹玻片上,将凹玻片平放于含少量无菌水的培养皿中,在28 ℃恒温培养箱黑暗条件下培养。每隔6 h用光学显微镜在10×20倍镜下观察孢子萌发情况。
-
供试辣椒果实处理:选取新鲜、无机械损伤的青椒果实,用ddH2O清洗3次,并用无菌滤纸吸去果实表面残留水分,随后在室温下风干1 h。
胶孢炭疽菌的接种方法:采用创伤接种法,用无菌大头针在供试青椒果实表面刺4个深约1 mm的小孔,将10 μL孢子悬浮液(制备方法同上)接种于果实伤口处,在28 ℃黑暗条件下密封保湿培养[10]。
药剂处理方法:为测定CHI的保护作用和治疗作用,使用400 μg/mL CHI溶液喷洒果实;以83 μg/mL苯醚甲环唑作为阳性对照;未处理对照组喷洒无菌蒸馏水。每个处理设4个重复果实,试验重复2次。杀菌剂分别在接种前12 h(保护作用)和接种后12 h(治疗作用)进行施用。
辣椒炭疽病病情分级标准见表 1,病情指数和防治效果计算公式如下:
-
辣椒种子萌发试验:在培养皿中铺放2层滤纸并编号,选取饱满度一致的辣椒种子300粒,每组50粒置于培养皿中。配制400 μg/mL CHI溶液,用10 mL CHI溶液浸种处理,以ddH2O处理为空白对照。在28 ℃光照培养箱中保湿培养7 d,根据如下公式统计发芽率[11]。
辣椒植株生长试验:在辣椒植株生长至四叶期时进行药剂处理,试验组连续5 d喷施CHI乳剂,空白对照组连续5 d喷施清水。随后每日观察并记录辣椒植株的农艺性状变化。
-
本研究所有试验均至少包含3次独立重复,试验数据以“平均值±标准差(SD)”表示。试验数据采用SPSS 27.0软件进行单因素方差分析,并使用Duncan多重比较法进行显著性差异检验(设p < 0.05为差异显著)。相关数据图表均使用Origin 2021软件进行绘制。
1.1. 材料
1.1.1. 供试植物
1.1.2. 培养基
1.1.3. 供试菌株
1.1.4. 主要试剂
1.2. 方法
1.2.1. CHI对辣椒胶孢炭疽菌营养生长的影响
1.2.2. CHI对辣椒胶孢炭疽菌生殖生长的影响
1.2.3. CHI对辣椒胶孢炭疽菌侵染青椒果实的影响
1.2.4. CHI对辣椒种子萌发和植株生长的影响
1.3. 数据处理与统计学分析
-
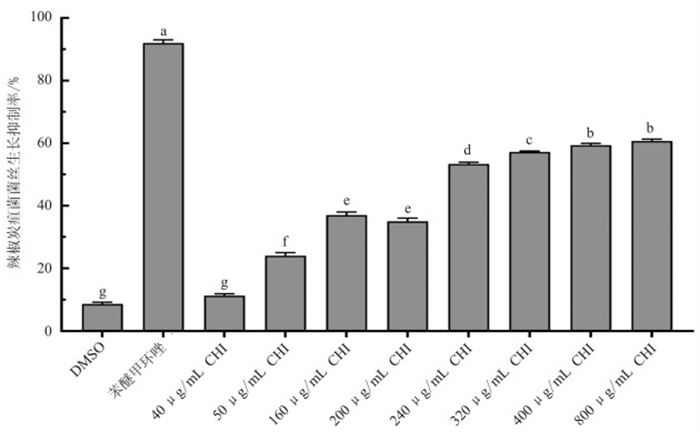
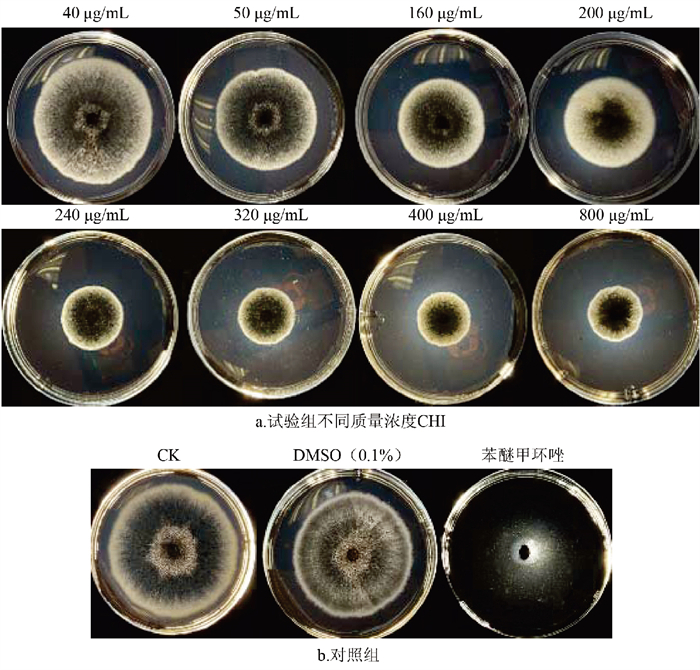
由试验结果可知,随着CHI质量浓度的升高菌丝抑制越明显(图 1)。CHI在平皿试验中对胶孢炭疽菌的最佳抑制浓度为400 μg/mL,经Duncan多重比较分析,该质量浓度的抑制率与其他低质量浓度处理在p<0.05水平下差异显著,此时菌丝生长抑制率最高达到60.21%。当质量浓度提高至800 μg/mL时,抑制率较400 μg/mL处理未表现出显著提升(图 2)。CHI对胶孢炭疽菌菌丝生长的EC50值为297.36 μg/mL,其毒力回归方程为Y=2.140 9+1.156 0X,相关系数r为0.931 7(表 2)。综上表明,CHI对辣椒胶孢炭疽菌菌丝生长具有一定抑制作用,但其活性低于阳性对照药剂。
-
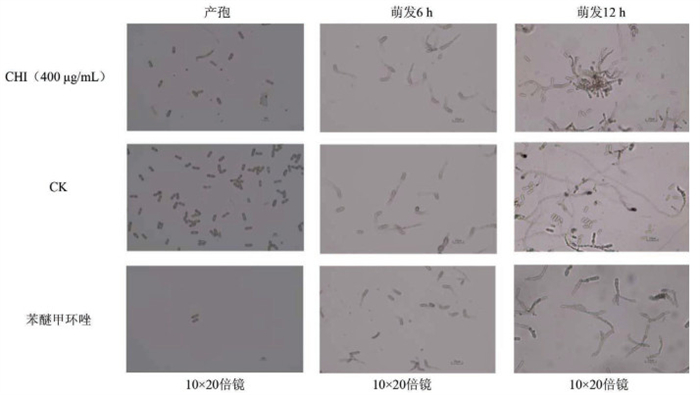
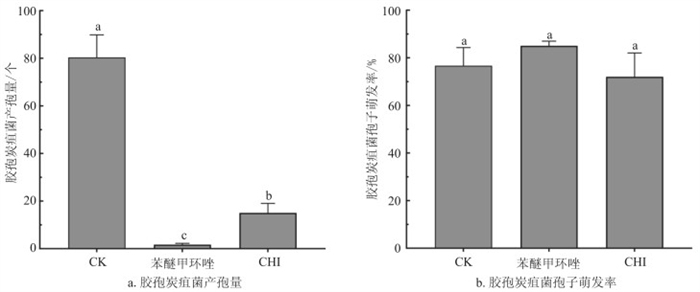
在10×20倍光学显微镜下观察400 μg/mL CHI对辣椒胶孢炭疽菌产孢量的影响。结果表明,CHI处理对孢子的大小及隔膜形成无显著影响(图 3),但能够明显降低产孢量(图 4a)。进一步在10×20倍光学显微镜下分别于培养6 h和12 h观察400 μg/mL CHI对辣椒胶孢炭疽菌孢子萌发的影响。结果显示,在培养6 h时,空白对照组约80%的胶孢炭疽菌孢子已萌发(图 3),而CHI处理组和苯醚甲环唑处理组均未对孢子萌发率产生明显抑制作用(图 4b)。
培养12 h后观察发现,各处理对芽管生长产生不同程度影响。CHI和苯醚甲环唑处理均表现出对芽管伸长的抑制作用,并出现明显的畸形膨大现象;而空白对照组芽管粗细均一且迅速伸长。具体而言,CHI处理组的萌发孢子呈现一定程度的聚集现象,芽管表现为膨大、扭曲并伴有分枝肿胀的形态;阳性对照组的畸形程度显著高于CHI处理组,萌发孢子相对分散,芽管分枝减少且局部出现突起结构。此外,当胶孢炭疽菌孢子在叶片或其他硬质表面萌发时,通常会形成大量黑色附着胞以穿透宿主表皮,而在本试验条件下,培养12 h内仅空白对照组观察到附着胞的形成(图 3)。
-
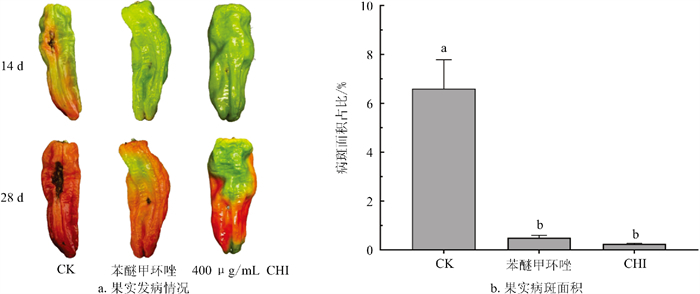
由试验结果可知,接种后14 d辣椒炭疽病发病程度较轻;至28 d时,空白对照组出现明显病害症状,病斑面积占比达到66%,并与各处理组之间比较,差异具有统计学意义(p<0.05)(图 5)。在离体果实接种试验中,CHI对辣椒炭疽病的防控效果与平皿试验中浓度筛选结果基本一致。400 μg/mL CHI在接种前喷施处理表现出较好的保护作用,果实病斑面积仅占2.25‰。如表 3所示,在接种后第28 d,400 μg/mL CHI处理组的病情指数明显低于空白对照组,仅为空白对照组病情指数的22.22%,防治效果达到77.78%,且优于苯醚甲环唑处理的66.67%。
-
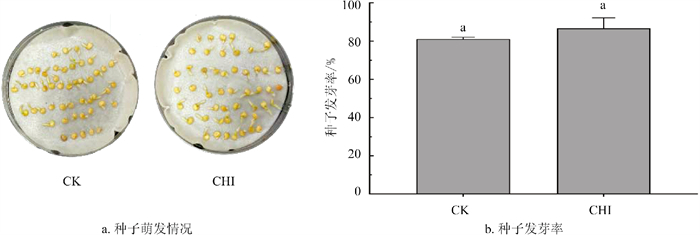
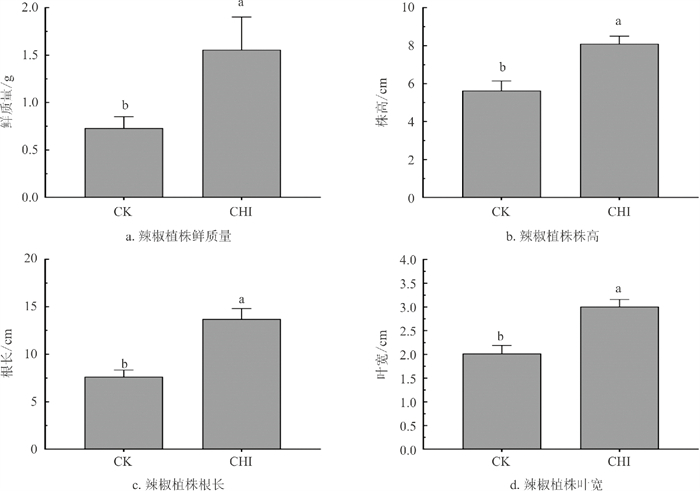
植物源农药在应用过程中面临的重要问题之一是其是否会对植物自身生长产生不利影响。由试验结果表明,CHI处理组与空白对照组的种子萌发情况基本一致,发芽率均达到90%以上(图 6),说明CHI处理基本不会影响辣椒种子的萌发。已有研究表明,CHI能够调节植物光合作用相关基因的表达[6]。因此,在喷施CHI后第6 d对辣椒植株的生长状况进行观察。观察结果显示,喷施CHI的植株整体长势良好(图 7);由图 8可知,CHI处理的辣椒植株株高、鲜质量、叶宽和根长明显优于空白对照,且差异具有统计学意义(p<0.05),表明CHI对辣椒植株具有良好的促生作用。根据试验结果推测,CHI可能通过增加叶片宽度,提高叶片的光合能力,从而促进光合产物的积累,并最终有助于提高作物产量。
2.1. 菌丝生长室内毒力测定
2.2. CHI对胶孢炭疽菌产孢和孢子萌发的影响
2.3. CHI对辣椒离体果实的保护和治疗活性
2.4. CHI对辣椒种子萌发情况及植株生长的影响
-
化学农药抗药性风险的增加推动了对天然来源抗菌剂的研究。研究发现,将酰肼基团作为中间体引入β-咔啉母核,并通过4-氯苯取代合成的氯吲哚酰肼(CHI),能够在一定程度上克服天然化合物稳定性和活性不足等缺点,并表现出优于先导化合物的抗菌活性[12]。根据杀菌剂的作用方式,其可能影响病原菌侵染过程中的一个或多个关键环节,包括菌丝生长、孢子萌发以及芽管伸长等。作为真菌生命周期中的关键阶段,菌丝生长通常始于孢子的萌发,这一过程标志着病原菌由休眠状态向活跃生长状态的转变。
本研究首次揭示了CHI通过抑制菌丝生长并干扰孢子萌发后发育的双重途径实现对辣椒炭疽病的防控,同时表现出一定的促生作用。体外抑制试验和活体接种试验结果表明,CHI对辣椒胶孢炭疽菌具有显著的抑制作用,其EC50值为297.36 μg/mL。与苯醚甲环唑相比,CHI对菌丝生长的抑制活性相对更低,这与四氢-β-咔啉衍生物通常靶向真菌细胞壁合成而非麦角甾醇代谢途径的作用特性一致[13-14]。Su等[15]设计并合成了一类新型1,2,3,4-四氢-β-咔啉衍生物,研究发现其对水稻白叶枯病和柑橘溃疡病均表现出较好的体内抑菌效果,并推测该类化合物可能通过干扰细胞氧化还原系统平衡,损伤细胞膜并诱导病原细菌细胞凋亡。相关研究表明,四氢-β-咔啉衍生物具有广谱活性、结构可塑性强以及活体防效较好的特点,有望成为新一代绿色农用杀菌剂的重要先导骨架。
此外,本研究发现CHI对孢子萌发率本身无显著影响,但能够诱导芽管发生明显畸形。其作用机制可能与破坏微管蛋白聚合、阻碍孢子萌发后菌丝的极性生长有关,这一现象与骆驼蓬碱对灰霉病菌的作用机制具有一定相似性[16]。尽管CHI在离体果实试验中表现出77.78%的保护性防效,但其EC50值相对较高(约为苯醚甲环唑的3.6倍),因此在实际生产中可能需要较高的施用剂量才能达到理想的防控效果。
同时,本研究表明CHI对辣椒种子萌发无负面影响,并能够显著促进辣椒植株生长。因此,后续研究可进一步聚焦于解析CHI与植物生长素信号通路之间的互作机制。张建建等[17]的研究发现,10%氯吲哚酰肼悬浮剂在番茄病毒病田间药效试验中的防控效果显著优于2%香菇多糖水剂和20%盐酸吗啉胍可湿性粉剂等药剂;李洁[18]的研究表明,氯吲哚酰肼与霜脲氰等常规药剂混配后,可显著提高对黄瓜霜霉病的田间防效;黄涛等[19]的研究发现,CHI处理能够显著提高小麦的发芽势、发芽率以及分蘖数。由此可见,CHI在已有研究中表现出较强的跨病害防控潜力、多机制协同效应以及多样化的生物活性,在广谱抗病、混配增效以及抗病与促生协同等方面具有广阔的研究与应用前景。然而,本研究也发现CHI几乎不具有治疗活性(接种后处理防效< 10%),说明其主要发挥保护性作用。未来可通过结构修饰或纳米载体包埋等策略(如借鉴(Mn2+-PDA)@CNC体系[20])提升CHI的稳定性和生物利用度。
已有研究表明,生长素合成关键酶的活性直接影响植物器官发育过程[21-22]。本研究中CHI处理显著提高了辣椒植株的株高和鲜质量,提示其可能通过上调生长素合成相关基因表达或增强生长素极性运输能力,从而促进植株顶端优势的形成。未来可利用同位素标记技术追踪CHI处理条件下IAA合成前体的代谢通量变化,并结合生长素转运蛋白的亚细胞定位分析,进一步验证CHI对生长素空间分布调控的作用机制[23-24]。此外,有研究表明ABP1-TMK膜受体系统能够在数秒内激活质子泵(如H+-ATPase),通过细胞壁酸化促进细胞伸长[23]。因此,CHI诱导的植株生长加速现象可能与跨膜生长素信号的快速响应有关。后续研究可通过非损伤微测技术实时监测CHI处理条件下根尖H+流速变化,或利用ABP1基因敲除突变体观察CHI促生效应的变化程度,以进一步解析其与快速信号通路之间的互作层级。
综上所述,本研究为基于天然产物结构优化与纳米技术结合的新型农药开发提供了试验依据,也为辣椒病害的绿色防控策略提供了新的思路。CHI作为一种新型四氢-β-咔啉衍生物,具有广谱抗菌和抗病毒活性,同时对植物生长具有促进作用。相关研究成果不仅为辣椒病害绿色防控提供了科学依据,也为其他作物病害的可持续管理提供了重要参考。



 下载:
下载: