-
开放科学(资源服务)标识码(OSID):

-
蜂蜜是蜜蜂采集植物的花蜜、分泌物或蜜露,并与自身分泌物混合后在蜂巢中充分酿制而成的天然甜物质。研究发现,蜂蜜在抗氧化、抑菌、抗炎、抗菌、抗糖尿病、伤口和晒伤愈合等方面具有显著作用,并有助于评估环境污染物的存在[1-9]。蜂蜜因其独特的风味、高营养价值和健康益处而受到广泛的关注和研究。蜂蜜的化学成分比较复杂,主要由糖和水组成,还含有少量的酶、矿物质、维生素、氨基酸、有机酸、类黄酮等酚类化合物和芳香物质。这些化合物的组成和比例决定了每种蜂蜜的颜色、口感及营养价值的差异[8, 10-11]。蜂蜜的成分和性质受环境、地理条件、植物种类、昆虫来源以及加工和储存方式等因素的影响,这些因素决定了市场上蜂蜜品种和功效的多样性[12]。因此,系统分析蜂蜜的理化性质不仅对明确其特征具有重要作用,而且对其功能性成分的开发具有重要经济意义。
葡萄糖和果糖是蜂蜜中的主要成分,影响蜂蜜的风味。蜂蜜中葡萄糖和果糖的比例主要取决于花蜜的来源[13],研究发现,果糖/葡萄糖比值不仅可表明蜂蜜的结晶能力,还有助于单花蜂蜜的分类[14]。酚类化合物可分为酚酸类和黄酮类化合物,是蜂蜜的重要抗氧化物质,其含量与蜂蜜的颜色、感官特征密切相关[15-16],深色蜂蜜通常含有更多的总酚酸和总黄酮,抗氧化能力也更强[17]。由于酚酸和黄酮是植物产生的一类次生代谢物,也被认为是蜜源植物和地理来源、蜂种来源的潜在标志[18-19]。除了抗氧化能力外,蜂蜜中的酚酸类和黄酮类物质还具有许多药理作用,包括促进伤口愈合,保护皮肤细胞和组织免受氧化损伤等[20]。蜂蜜中蛋白质含量相对较少,通常不超过0.7%,但几乎含有所有重要的生理氨基酸,其中脯氨酸含量最高,占总氨基酸的50%~85%,脯氨酸也是衡量蜂蜜成熟度的标准,天然蜂蜜中脯氨酸含量在200 mg/kg以上[11]。游离氨基酸作为蜂蜜中的重要营养成分,对其组成的分析不仅可用于评价蜂蜜的品质,也有助于明确蜂蜜的植物来源[21],研究人员发现可根据游离氨基酸的含量将不同地区的蜂蜜区分开来[22]。植物的花粉和花蜜是蜜蜂的主要食物来源,也是蜂蜜的主要成分。蜂蜜中花粉粒的组成不仅反映了蜜源植物的种类,还可推断蜂蜜的地理来源和品质[23-24]。
中华蜜蜂(简称中蜂)是中国的本土蜜蜂,是东方蜜蜂的一个主要亚种。与意大利蜜蜂相比,中蜂的嗅觉灵敏度较高,善于发现和采集分散、零星蜜源。中蜂蜜因其花蜜周期长,来源广泛而具有较高营养价值和药用价值[25]。然而,由于中蜂产蜜能力较弱,产量有限,人们对中蜂蜜的了解也十分有限。目前,对于蜂蜜的研究主要集中在意大利蜜蜂所产蜂蜜或单花蜜的营养组成、理化性质和抗炎、抗氧化活性等方面[19, 26-28],而对中蜂蜜的研究报道较少。重庆是中国养蜂业发展的优势区域,丰富的野生和人工栽培的蜜源植物为养蜂提供了充足的蜜源基础。据统计,2023年重庆市蜂群保有量超过160万群,年产蜂蜜2.2万t,居中国第六位。目前,关于重庆市中华蜜蜂的研究主要集中在遗传、疾病等方面,而对于中蜂蜜本身品质的研究暂无相关报道。渝东北、渝西、渝东南作为重庆市的重要生态保护发展区,生态环境优良,山区多以饲养中华蜜蜂为主。因此,本实验选择了渝东北、渝西、渝东南3个区域所产的中蜂蜜为试验材料,对其理化指标、抗氧化能力、游离氨基酸含量、植物来源进行了测定和分析,旨在加强对中蜂蜜的科学研究,也为重庆渝东北、渝西、渝东南地区中蜂蜜的开发利用提供重要的理论依据。
HTML
-
本实验所用中蜂蜜样品于2024年6月分别采集自重庆渝东北、渝西、渝东南3个区域,每个区域采集5个样品,所有蜂蜜样品避光保存在4 ℃条件下备用。实验中所用的果糖、葡萄糖、蔗糖、原儿茶酸(纯度≥98%)、槲皮素(纯度≥98%)标准品均购自上海源叶生物科技有限公司;16种氨基酸混合标准液(2.5 μmol/mL)购自上海金畔生物科技有限公司;总抗氧化能力检测试剂盒ABTS、DPPH购自生工生物工程(上海)股份有限公司,FRAP试剂盒购自北京索莱宝科技有限公司。
-
使用的仪器包括:Waters 2695高效液相色谱仪,美国Waters公司;Multiskan GO全波长酶标仪,美国Thermo Scientific公司;L-8900型氨基酸分析仪,日本HITACHI公司。
-
果糖、葡萄糖、蔗糖含量参照《食品安全国家标准食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖的测定》 (GB 5009.8—2016)[29]的方法进行测定。
-
总酚酸含量的测定参考文献[30],采用福林酚(Folin-Ciocalteu)分光光度比色法,并适当调整。称取5.0 g蜂蜜样品,加入超纯水溶解并定容至50 mL,8 000 r/min离心5 min,吸取上清液1 mL,加入1 mol/L福林酚试剂1 mL、1 mol/L碳酸钠溶液5 mL,超纯水定容至10 mL,混匀,于室温、避光条件下反应1 h后,在760 nm处测定吸光度值,平行测定3次。以蒸馏水为空白对照,以原儿茶酸浓度(2~12 μg/mL)为横坐标,吸光度值为纵坐标,绘制标准曲线,根据回归方程计算样品中总酚酸含量(单位mg/kg)。
-
总黄酮含量的测定参考文献[30],采用三氯化铝(AlCl3)分光光度比色法检测,并适当调整。称取10.0 g蜂蜜样品,加入超纯水溶解并定容至15 mL,8 000 r/min离心5 min,吸取上清液3 mL,加入1%三氯化铝溶液1 mL,95%乙醇定容至10 mL,摇匀,室温静置10 min后,在405 nm处测定吸光度值,平行测定3次。以蒸馏水为空白对照,以槲皮素浓度(4~40 μg/mL)为横坐标,吸光度值为纵坐标,绘制标准曲线,根据回归方程计算样品中总黄酮含量(单位mg/kg)。
-
采用总抗氧化能力检测试剂盒(DPPH)方法测定蜂蜜抗氧化能力。0.1 mL蜂蜜溶液中加入1 mL DPPH提取液,混匀后4 ℃、12 000 r/min离心10 min。取20 μL上清液和380 μL DPPH工作液混匀后室温避光反应20 min,在515 nm波长下测定其吸光度值。同时做空白对照。以Trolox溶液(0.01~0.3 μmol/mL)为横坐标,吸光度值为纵坐标绘制标准曲线,回归方程为y=0.532 4x-0.006 9 (R2=0.999 7)。根据回归方程计算样品DPPH自由基清除能力(单位μmol/mL)。
-
采用总抗氧化能力检测试剂盒(FRAP法)检测蜂蜜的抗氧化能力。0.1 mL蜂蜜溶液中加入1 mL FRAP提取液,混匀后4 ℃、10 000 r/min离心10 min,取上清。取6 μL上清,再依次加入180 μL FRAP工作液、8 μL蒸馏水,充分混匀,室温反应10 min,在593 nm波长下测定其吸光度值。同时做空白对照。以FeSO4·7H2O浓度为横坐标,吸光度值为纵坐标,绘制标准曲线,求得回归方程。根据回归方程计算样品FRAP抗氧化能力(单位μmol/mL)。
-
采用总抗氧化能力检测试剂盒(ABTS)方法测定蜂蜜抗氧化能力。0.1 mL蜂蜜溶液中加入1 mL ABTS提取液,混匀后4 ℃、10 000 r/min离心10 min。取10 μL样品,加入190 μL ABTS工作液,充分混匀,静置20 min,在734 nm波长下测定其吸光度值,同时做空白对照。以Trolox溶液浓度(0.01~0.3 μmol/mL)为横坐标,吸光度值为纵坐标绘制标准曲线,回归方程为y=0.55x+0.000 6 (R2=0.999 2)。根据回归方程计算样品ABTS阳离子自由基清除能力(单位μmol/mL)。
-
蜂蜜中游离氨基酸参照《蜂蜜中18种游离氨基酸的测定高效液相色谱-荧光检测法》 (SN/T 5223—2019)[31]的方法进行测定,并做适当修改。称取1.0 g蜂蜜样品于50 mL离心管内,加入10 mL超纯水振荡,充分溶解后过0.22 μm滤膜,待上机检测。采用氨基酸分析仪进行测定,检测器类型为荧光检测器,检测波长为570 nm/440 nm,色谱柱为离子交换柱,柱温为60 ℃,进样体积10 μL,柱后反应温度为135 ℃。氨基酸标准曲线的绘制:将16种氨基酸混合标准溶液用0.1 mol/L的盐酸溶液稀释成浓度为0.50、1.0、2.5、5.0、10.0、25.0 nmol/mL的标准工作液,上机测定,以氨基酸峰面积y对氨基酸浓度x进行回归处理,绘制标准曲线,计算蜂蜜样品中游离氨基酸的含量。
-
参考文献[32]的方法进行花粉提取,并做适当调整。将20 g蜂蜜样品置于50 mL的无菌离心管中,加入20 mL蒸馏水,搅拌均匀后,5 000 r/min离心15 min,倒掉上清液。沉淀中再次加入20 mL蒸馏水并搅拌均匀,重复上述步骤2次。弃去上清液,将沉淀取出,置于培养皿上,摊放于防尘处进行自然干燥。将少许干燥后的花粉均匀地粘在黏有导电胶的样品台上,在离子溅射仪中喷金、镀膜后,放置在冷场发射扫描电子显微镜(日立,SU8010)上寻找外形完整饱满、具有代表性的花粉粒,在3 500~5 000倍下进行拍照,将所拍花粉的电镜图片与植物花粉图片进行对照,根据花粉大小、赤道面观、极面观、表面纹饰等对蜂蜜中的花粉种类进行鉴别。
-
所有蜂蜜样品均测定3次,结果以“平均值±标准差”表示。采用SPSS 20.0软件对所得数据进行显著性分析和相关性分析。首先用SPSS 20.0软件中One-Way ANOVA过程对所得数据进行方差齐性检验:若方差齐性,采用Tukey法比较各组间的差异;若方差不齐,采用Tamhane's T2法比较各组间的差异。p<0.05表示组间存在显著差异。
1.1. 样品与试剂
1.2. 仪器与设备
1.3. 实验方法
1.3.1. 理化指标测定
1.3.2. 抗氧化成分及活性测定
1.3.2.1. 总酚酸含量的测定
1.3.2.2. 总黄酮含量的测定
1.3.2.3. DPPH自由基清除能力测定
1.3.2.4. FRAP抗氧化能力测定
1.3.2.5. ABTS阳离子自由基清除能力测定
1.3.3. 游离氨基酸含量的测定
1.3.4. 蜂蜜孢粉学分析
1.4. 数据处理
-
重庆3个区域蜂蜜样品的理化指标测定结果见表 1。糖类成分是蜂蜜中最主要的成分,我国行业标准[29]规定蜂蜜中果糖和葡萄糖的含量总和不低于60%,蔗糖的含量不高于5%。渝东北、渝西、渝东南3个区域的中蜂蜜中果糖、葡萄糖和蔗糖含量均满足行业标准,且各组间均无显著差异,表明3个区域的中蜂蜜均符合行业标准规定。
-
重庆3个区域的中蜂蜜样品抗氧化能力测定结果如表 2所示。由表 2可知,3个区域的中蜂蜜抗氧化成分总酚酸的含量远高于总黄酮的含量,且各区域间总酚酸和总黄酮含量均无显著差异,但从整体上来看,各区域总酚酸和总黄酮含量由高到低的顺序为渝东南、渝东北、渝西。3个区域的中蜂蜜均有不同程度的抗氧化作用,其中DPPH自由基清除能力、FRAP抗氧化能力由强到弱的顺序为渝东南、渝东北、渝西,而对于ABTS阳离子自由基清除能力,3个区域中以渝东北最强,渝西最弱。
-
重庆3个区域中氨基酸种类及含量结果见表 3。由表 3中可知,除苏氨酸和蛋氨酸外,3个区域的中蜂蜜样品共检测出14种氨基酸。比较分析发现,重庆3个区域的中蜂蜜样品中总游离氨基酸含量差异不显著,其中渝西蜂蜜样品中总游离氨基酸含量最高(1 890.70 mg/kg),渝东北蜂蜜样品中含量最低(1 188.33 mg/kg);3个区域中蜂蜜中均以苯丙氨酸(184.00~1 319.60 mg/kg)和脯氨酸(313.80~868.20 mg/kg)为主要的游离氨基酸,其中渝东北和渝西区域蜂蜜样品中苯丙氨酸的含量高于脯氨酸的含量,渝东南区域蜂蜜样品中苯丙氨酸含量低于脯氨酸含量,且渝东南区域蜂蜜样品中脯氨酸的含量显著高于渝东北和渝西区域(p<0.05)。其他游离氨基酸中,渝东北区域蜂蜜样品中天门冬氨酸、丝氨酸、谷氨酸、甘氨酸、缬氨酸、异亮氨酸、亮氨酸、酪氨酸的含量均高于渝西和渝东南区域,除渝西区域异亮氨酸含量显著低于渝东北和渝东南区域外,其他区域间氨基酸含量差异均不显著。此外,3个区域蜂蜜样品中EAA、MAA含量的高低顺序为渝西、渝东北、渝东南。
-
重庆3个区域中蜂蜜抗氧化成分、氨基酸(脯氨酸、苯丙氨酸)与抗氧化活性相关性如表 4-表 6所示。由表 4可知,渝东北区域蜂蜜样品中总酚酸含量与总黄酮含量(r=0.927,p=0.05)、DPPH自由基清除能力(r=0.929,p=0.05)呈显著正相关,与ABTS阳离子自由基清除能力呈极显著正相关(r=0.965,p=0.01);总黄酮含量与脯氨酸含量(r=0.880,p=0.05)呈显著正相关,与苯丙氨酸含量(r=0.983,p=0.01)、DPPH自由基清除能力呈极显著正相关(r=0.998,p=0.01);脯氨酸含量与ABTS阳离子自由基清除能力呈显著正相关(r=0.885,p=0.05),苯丙氨酸含量与DPPH自由基清除能力呈极显著正相关(r=0.979,p=0.01)。由表 5可知,渝西区域蜂蜜样品中总酚酸含量与DPPH自由基清除能力呈显著正相关(r=0.923,p=0.05),总黄酮含量与脯氨酸(r=0.994,p=0.01)、苯丙氨酸(r=0.991,p=0.01)含量呈极显著正相关;脯氨酸含量与苯丙氨酸呈极显著正相关(r=0.985,p=0.01)。由表 6可知,渝东南区域蜂蜜样品中总酚酸含量与总黄酮(r=0.985,p=0.01)、DPPH自由基清除能力呈极显著正相关(r=0.961,p=0.01),与FRAP总抗氧化能力呈显著正相关(r=0.913,p=0.05);总黄酮含量与DPPH自由基清除能力呈极显著正相关(r=0.961,p=0.01),与FRAP总抗氧化能力呈显著正相关(r=0.921,p=0.05)。
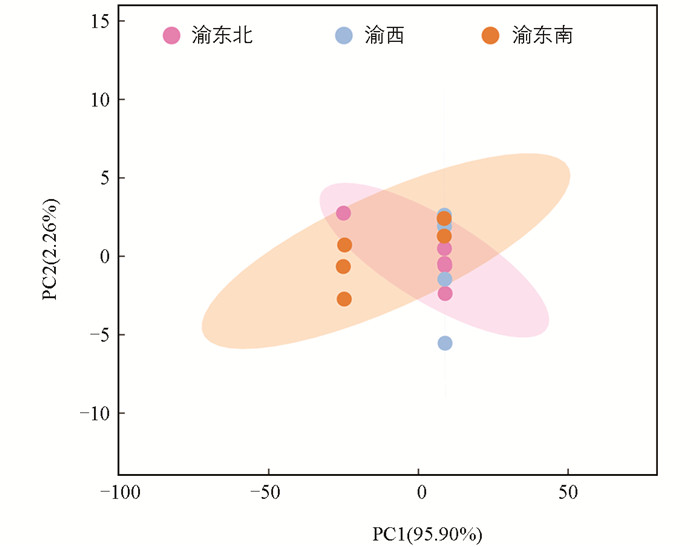
此外,利用测定得到的中蜂蜜理化指标(葡萄糖、果糖、蔗糖)、抗氧化能力指标(总酚酸、总黄酮、DPPH、FRAP、ABTS)、氨基酸(脯氨酸和苯丙氨酸)这些参数对3个区域的中蜂蜜样品进行PCA分析,一共提取出两个主成分,得分分别为95.90%和2.26%,PCA图见图 1。由图 1可知,重庆3个区域的中蜂蜜样品分布较为分散,样品均有重合,仅渝西区域样品聚集较为紧密,且都分布于PC1正半轴,这可能与3个区域地理条件和植物种类有关。
-
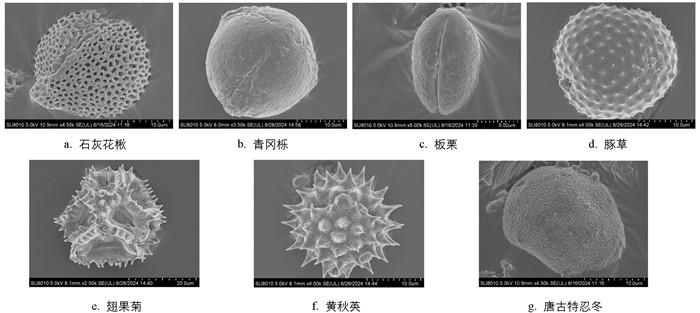
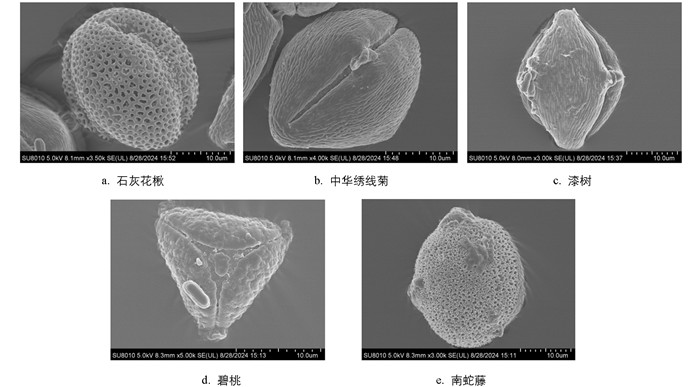
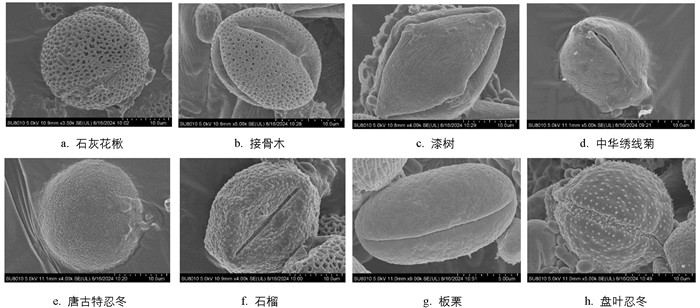
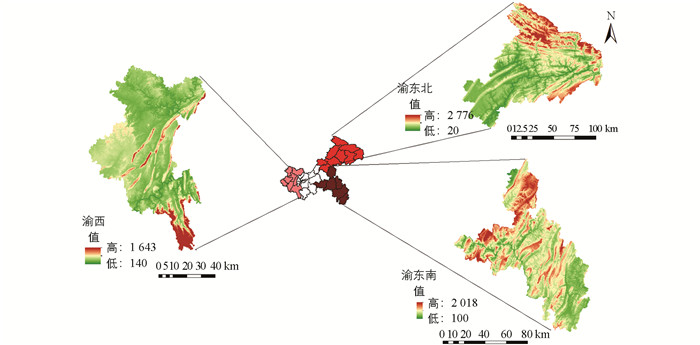
本研究利用孢粉学对重庆3个区域蜂蜜样品中的花粉粒进行鉴定分析,花粉形态结果见图 2-图 4。由图 2-图 4可知,重庆3个区域蜂蜜样品的蜜源植物较为丰富,共鉴定到7科13属14种植物。7科包括蔷薇科、壳斗科、菊科、忍冬科、漆树科、卫矛科和石榴科;13属包括花楸属、栎属、栗属、豚草属、莴苣属、秋英属、忍冬属、绣线菊属、漆属、李属、南蛇藤属、接骨木属和石榴属。受到该区域海拔、气候等因素的影响,不同区域的蜜源植物存在差异。这3个区域的地形地貌如图 5所示,由图 5可知,渝东南和渝东北的海拔均高于渝西地区,其中:石灰花楸花粉在3个区域均有发现;渝东北区域蜂蜜样品中发现有青冈栎、翅果菊和黄秋英花粉,而在渝西和渝东南两个区域均未发现;渝西区域蜂蜜样品中花粉种类较少,但碧桃、南蛇藤的花粉在其他两个区域均未发现;渝东南区域蜜源植物较多,与其他两个区域均有重叠,但接骨木和石榴花粉在其他两个区域均未发现。
2.1. 理化指标分析
2.2. 抗氧化能力分析
2.3. 游离氨基酸含量分析
2.4. 不同区域蜂蜜抗氧化成分、氨基酸与抗氧化活性相关性分析
2.5. 花粉种类分析
-
蜂蜜的成分和品质受到多种因素的影响,包括植物来源、地理条件、蜜蜂品种、季节变化以及蜂群环境等,导致不同产地的蜂蜜存在差异。中蜂蜜兼具食品价值与药用价值[19],然而,关于中蜂蜜的研究相对较少,目前在中国仅见对湖北省神农架林区不同区域、秦岭地区、四川、江西地区中蜂蜜理化性质、抗氧化能力及抗菌活性的研究报道[25, 32-36]。本研究对重庆3个主要区域(渝东北、渝西、渝东南)中蜂蜜的理化指标、抗氧化能力、游离氨基酸含量及蜜源植物来源进行了系统分析,填补了重庆市中蜂蜜品质研究的空白。
果糖和葡萄糖的浓度及其比值是影响蜂蜜品质的重要因素,在蜂蜜成熟过程中,蔗糖被不断转化为单糖(果糖和葡萄糖),低蔗糖含量的液态表明蜂蜜已经成熟[37],在本研究中,果糖与葡萄糖比值均在1.10左右,且为液体状态,表明样品均为成熟蜂蜜。总酚酸和总黄酮是反映蜂蜜抗氧化能力的重要成分,不同区域和不同植物来源蜂蜜样品之间总酚酸和总黄酮含量的差别较大,是判断蜂蜜植物和地理来源的重要指标性物质[18]。本研究发现,渝东南区域总酚酸和总黄酮的含量最高,这与文献[36]中对神农架林区研究结果相似;3个区域蜂蜜的DPPH自由基清除能力、FRAP总抗氧化能力与总酚酸和总黄酮的含量趋势一致,均以渝东南区域最高;而ABTS阳离子自由基清除能力以渝东北区域最高。结合相关性分析结果可知重庆3个区域中蜂蜜品质符合标准,渝东北、渝东南中蜂蜜的抗氧化能力强于渝西,这与之前报道的蜂蜜样品中总酚酸含量与DPPH自由基清除能力和ABTS阳离子自由基清除能力存在显著正相关的研究结果相似[33, 38]。
游离氨基酸是蜂蜜中的重要营养成分,为蜂蜜植物来源及其品质评价提供重要信息[39]。本研究共检测到14种氨基酸,其中渝西区域蜂蜜样本中总游离氨基酸的含量最高(1 890.70 mg/kg),高于新疆黑蜂蜂蜜总游离氨基酸含量(458.98~805.94 mg/kg)[40],低于藏红花中总游离氨基酸含量(3 104.27~9 814.64 mg/kg)[22],表明重庆渝东南、渝西、渝东北3个区域的中蜂蜜游离氨基酸含量较为丰富,脯氨酸含量均高于天然蜂蜜(200 mg/kg)[11],脯氨酸的含量可直接影响蜂蜜的自由基清除能力[41]。本实验发现渝东北蜂蜜中脯氨酸含量与ABTS阳离子自由基清除能力、苯丙氨酸含量与DPPH自由基清除能力存在显著正相关,而在其他区域未发现相关性,可能是样品中的其他抗氧化物质造成蜂蜜抗氧化活性差异[41]。蜂蜜所含必需氨基酸的组成和比例越接近人体必需氨基酸的组成和比例,其发挥的营养价值也就越高。本研究发现,重庆3个区域中渝西区域蜂蜜样本中EAA/TAA比例达到72.27%,EAA/NEAA比例为260.61%,该结果远高于FAO/WHO所提到的理想蛋白质的标准(EAA/TAA为40%,EAA/NEAA为60%),表明渝西区域蜂蜜营养价值较高。此外,我们发现不同区域MAA的含量也存在明显差异,其中渝西区域蜂蜜中MAA/TAA比例最高,为76.58%,远高于新疆黑蜂蜂蜜(37.92%~57.94%)、中药材西藏冬虫夏草(55.03%~57.54%)和山茱萸(60.06%~68.46%)[40]。研究发现,MAA中的苯丙氨酸在抑制多发性骨髓瘤、改善认知功能及能量摄入方面发挥着重要作用[42];谷氨酸则对保护神经元免受外源自由基和线粒体自由基的损伤、促进大脑健康至关重要[43],同时能够促进毛发生长[44];赖氨酸可抑制肿瘤增殖、促进细胞生长、伤口愈合、介导血管生成、维持肌肉质量和促进骨骼发育[45]。综上所述,渝西区域的中蜂蜜具有良好的药用价值,这可能与该地区独特的地理气候条件及蜜源植物有关,未来可将该区域作为优质药材资源开发与利用的理想地区。
PCA分析显示,3个区域的植被资源存在差异,植被资源分布呈现显著的地理特征,尽管重庆属于亚热带季风性湿润气候范畴,但渝东北、渝东南与渝西3个地貌单元存在显著环境梯度差异。具体而言,海拔呈现明显梯度特征(由高到低依次为渝东北、渝东南、渝西)[46],这与蜜源植物唐古特忍冬在渝东北、渝东南两地蜂蜜中检出吻合,也与该植物对高海拔生境的生态适应性一致[47]。进一步分析表明,渝东南处于武陵山脉与乌江水系交汇之处,全年降水分配均衡、年均相对湿度较高,因此该区域蜜源植物丰富度最高;渝东北地区受大巴山地形抬升效应与三峡库区水域调节影响,蜜源植物丰富度次之;相比之下,渝西地区受四川盆地地形屏蔽效应影响,年降水量最低,导致其蜜源植物多样性最低,这与文献[48]中对重庆市植被覆盖值的研究结果一致。孢粉学分析也发现相似结果,14种蜜源植物在3个区域既存在重叠又有差异性。结合蜂蜜抗氧化能力及游离氨基酸含量分析结果,渝东南区域蜂蜜抗氧化能力强,这可能与该地区丰富的蜜源植物相关,如接骨木、石榴等。据报道,接骨木的茎叶、果实中含有丰富的酚酸类和黄酮类物质[49],石榴的叶、花、果皮、籽和汁中含有丰富的糖类、黄酮、多酚、生物碱等活性成分,具有抗炎、抗氧化等功效。渝西蜂蜜中氨基酸含量丰富,尤其是药用氨基酸含量丰富,可能与该区域种植的南蛇藤相关。南蛇藤是卫矛科南蛇藤属植物,含有萜类、脂肪类、苷类以及黄酮类化合物等多种药理活性成分,在祛风除湿、消肿抗炎及调节脂质代谢、降脂减肥和保肝方面具有广阔的药用价值。综上所述,地形地貌显著影响蜜源植物多样性和差异性,研究结果为重庆渝东北、渝东南、渝西3个区域蜂蜜的营养价值评价、蜜源植物资源开发以及功能成分的挖掘等提供了重要的理论指导。
-
本研究对重庆市渝东南、渝西、渝东北3个区域的中蜂蜜特征进行了全面深入地分析。结果显示,样品的理化指标均符合行业标准,表明重庆地区蜜源植物丰富,中蜂蜜品质优良。在3个区域样品中均检测到14种游离氨基酸,其中渝西区域蜂蜜的必需氨基酸、药效氨基酸含量最高,渝东北、渝东南区域蜂蜜的抗氧化能力较强。孢粉学分析在3个区域共鉴定出7科13属14种植物,分析表明接骨木、石榴、南蛇藤等蜜源植物可能是影响中蜂蜜抗氧化能力与氨基酸含量的关键因素。综上所述,本研究为解析重庆渝东北、渝西、渝东南区域中蜂蜜的特征、品质提供了重要科学数据。未来,可运用多组学技术解析蜜源植物功能成分与蜂蜜活性物质的关联机制,针对区域特性定向开发功能化产品(如渝东北抗氧化、渝西高氨基酸等功能蜂蜜),实现蜂蜜产业从品质解析到功能化、生态化的全链条技术体系生产,为重庆山地特色农业的高质量发展提供理论支撑与实践范式。





 DownLoad:
DownLoad: