-
开放科学(资源服务)标识码(OSID):

-
魔芋(Amorphophallus Blume)是天南星科魔芋属的多年生草本植物,也是唯一可提供大量葡甘聚糖的经济作物,起源于亚洲中南半岛北部和云南南部,其始祖种是森林下层的留居者,主要有白魔芋、珠芽魔芋、花魔芋等多个种[1]。魔芋葡甘聚糖作为良好的可溶性膳食纤维,具有预防高血压、高血脂以及减脂瘦身等功效,在医药、食品加工和功能材料等方面都有十分重要的作用[2]。魔芋在生产中常受到病害的侵袭,通常有软腐病、白绢病、病毒病、日灼病、叶枯病等,其中软腐病最普遍,一旦发病会导致魔芋减产和品质下降,造成难以挽回的经济损失,被称为魔芋的“癌症”[3-4]。
魔芋软腐病是细菌性病害,主要由果胶杆菌属(Pectobacterium)、迪基氏菌属(Dickeya)和一些未知菌株引起[5],在高温、高湿环境及雨季或排水不良的田间易暴发。软腐病主要侵染魔芋的叶片、叶柄和球茎。叶片染病时,先出现水浸状的暗绿色小斑,组织逐渐腐烂并伴有汁液流出,叶片泛黄最后干枯;叶柄染病时,出现水浸状条斑或叶柄基部发生溃烂,汁液沿叶柄逐渐蔓延,导致叶柄腐烂离解,植株朝发病一侧倒伏;球茎染病时,发病部位表现暗褐色水浸状病斑,逐渐朝内部侵染,出现灰褐色黏液状腐烂并散发臭味,叶片萎蔫卷缩,后期地上部全株或半边发黄[6-8]。
化学防治是魔芋软腐病防控的主要手段,应用广泛的农用链霉素已退出农药市场,目前噻菌铜、氢氧化铜、波尔多液等化学农药应用普遍。研究表明青枯立克、四霉素水剂、噻森铜等均对软腐病有良好的防治效果[9]。化学农药虽然效果显著、用药成本低、操作简单,但是施用过多不仅会致使病原菌出现耐药性,还易造成环境污染、药物残留等问题[10],不符合绿色健康可持续发展的要求。因此,在生产中应选择安全健康、选择性高、无药害、低残留的农药。生物农药又称天然农药,可源自植物(例如其分泌物、精油以及树皮、根和叶的提取物)、微生物(例如代谢物)以及生物来源的纳米颗粒(例如银和金纳米颗粒)等[11-12],具有环境友好、来源广泛、选择性强的特点,应用范围正在逐步扩大。生物农药在防治魔芋软腐病方面的研究较少,主要有枯草芽孢杆菌、大蒜素、木醋液等[13-14]。采用生物农药防治魔芋软腐病能大大减少化学农药所带来的污染,避免抗药性问题,减少对魔芋自身生长的影响[15]。但生物农药易受环境因素干扰,防治效果缓慢,生产成本高,将生物农药与化学农药合理复配,不仅能增强防治效果,减缓病原菌抗药性,还能降低生产成本,减少对环境的影响。
为探究不同农药对魔芋软腐病病原菌的防治效果,本研究从魔芋发病植株中分离纯化魔芋软腐病病原菌,选用市售常见的6种生物农药和8种化学农药,分别探讨其对魔芋软腐病病原菌的抑制效果,并进一步探究二者在复配条件下的抑制效果,以期为魔芋软腐病防治提供高效、环境友好的绿色防治方案,同时为魔芋安全生产提供技术支撑和科学依据。
HTML
-
2024年6月从重庆市北碚区西南大学歇马魔芋资源圃采集发病的白魔芋植株。
-
NA培养基:蛋白胨10 g/L,牛肉膏3 g/L,NaCl 5 g/L,琼脂15~20 g/L,pH值7.0;LB液体培养基:蛋白胨10 g/L,酵母提取物3 g/L,NaCl 10 g/L,pH值7.0;LB固体培养基:蛋白胨10 g/L,酵母提取物3 g/L,NaCl 10 g/L,琼脂15~20 g/L,pH值7.0。
-
供试6种生物农药种类及名称见表 1,供试8种化学农药种类及名称见表 2,细菌基因组DNA提取试剂盒由天根生化科技(北京)有限公司生产。
-
采用划线分离法分离病原菌[16],采集发病魔芋植株并清理表面泥土,流水冲洗30 min,用75%酒精对材料表面进行消毒,在超净工作台中吹干,用灭菌刀切下病健交界处,放入75%酒精浸泡2 min,用无菌水漂洗3次;将病样组织放入含有1 mL无菌水的灭菌离心管中,用无菌玻璃棒捣碎,静置2 min后用接种环蘸取液体,在NA培养基上划线,28 ℃培养24 h,将单菌落进行多次划线培养获得纯化菌株。
-
用灭菌牙签蘸取单菌落接种在LB液体培养基中,在28 ℃摇床(180 r/min)中培养24 h,制成OD600≈0.6的菌悬液。选择无病害的白魔芋球茎,流水冲洗干净,75%酒精表面消毒并在超净工作台中吹干;将球茎切成厚0.5 cm左右的方块,培养皿中放入无菌滤纸,加入2 mL无菌水保湿,在切片中央划出十字形伤口,用移液枪吸取20 μL菌悬液接种在伤口处,保鲜膜密封,28 ℃培养24 h。对照接种无菌水,设置3次重复。将培养后发病的魔芋球茎再次分离病原菌,根据柯赫氏法则进行验证。
菌株致病能力强弱根据病斑平均长度(L)[17]评价:0级,无明显病斑,标注为“-”;1级,L<10 mm,标注为“+”;2级,10≤L<15 mm,标注为“++”;3级,15≤L<20 mm,标注为“+++”;4级,L≥20 mm以上,标注为“++++”。
-
球茎接种同1.2.2,对照接种无菌水,设置3次重复。叶柄接种:选择生长健壮的叶柄,流水冲净,75%酒精表面消毒,吹干后用灭菌刀切开,每段8 cm左右,将叶柄形态学下端用湿润的无菌棉球包住,放入培养皿,灭菌牙签在中间扎3个小孔,移液枪吸取20 μL菌悬液接种在伤口处,保鲜膜密封,28 ℃培养24 h,对照接种无菌水,设置3次重复。叶片接种:选择生长健壮的叶片,流水冲净,75%酒精表面消毒,吹干后用湿润的无菌棉球包住小叶柄,放入培养皿,灭菌牙签在中间扎3个小孔,移液枪吸取20 μL菌悬液接种在伤口处,保鲜膜密封,28 ℃培养24 h,对照接种无菌水,设置3次重复。
-
提取病原菌菌株DNA,利用细菌16S rDNA通用引物27F/1492R(27F:AGAGTTTGATCCTGGCTCAG;1492R:TACGGCTACCTTGACGACTT)[16]进行PCR扩增。2%琼脂糖凝胶电泳检测扩增产物,回收纯化产物后送测序。将测序结果进行BLAST比对,下载相关同源序列,利用MEGA11软件并采用邻接法(Neighbor-joining,NJ)构建系统发育树,明确病原菌菌株的分类地位。
-
挑取菌株单菌落在NA培养基上划线,放置在28 ℃培养箱中培养24 h,观察菌落形态、颜色等特征,进行革兰氏染色鉴别菌株,在扫描电子显微镜下进一步观察病原菌的形态特征。
-
选取新鲜无病害的芋、番薯、马铃薯、芹菜、胡萝卜、白萝卜、白菜7种不同植物的根茎、块根、块茎、茎或叶进行试验。材料用流动的水冲洗干净,75%酒精表面消毒,番薯、马铃薯、芋、白菜切成3 cm×2.5 cm×0.5 cm的方块,胡萝卜和白萝卜分别切成0.5 cm的圆片和三角片,芹菜切成8 cm长的小段。将切好的材料放进含有无菌滤纸的培养皿中,加入2 mL无菌水保湿,用灭菌牙签在中央扎3个小孔,移液枪吸取20 μL菌液接种在伤口处,保鲜膜密封,28 ℃培养24 h,观察发病情况。对照接种无菌水,设置3次重复。
-
采用抑菌圈法[18]进行测定,提前制备OD≈0.6的菌悬液并用无菌水配制6个不同浓度的药液。将药液同样配成6个不同浓度。配制LB固体培养基并灭菌,待温度降到45 ℃左右倒板,每皿20 mL,培养皿凝固晾干后用一次性无菌棉签蘸取菌悬液涂板备用,在平板中间用直径0.65 cm的打孔器打孔,吸取50 μL药液加入,密封后28 ℃培养24 h。对照加入无菌水,设置3次重复。抑菌圈直径采用十字交叉法测量并计算药液抑制率,使用DPS 9.01进行毒力回归方程计算,并比较不同杀菌剂的抑制中浓度(EC50)。
-
依据1.2.7试验结果进行药剂复配最佳组合筛选,分别配制各药剂母液,浓度为50倍EC50,按照0∶10、1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1、10∶0的比例混合,同样采用抑菌圈法测定。培养结束后测量抑菌圈直径,计算实际抑制率、理论抑制率、毒效比率,按照毒效比率<1为拮抗作用、毒效比率=1为相加作用、毒效比率>1为增效作用的标准进行评定[19]。
理论抑制率(%)=单剂A实际抑制率×单剂A所占比例+单剂B实际抑制率×单剂B所占比例
-
用无菌水配制浓度为50倍EC50的药液,按照1.2.8中有增效作用的比例进行混合配成母液,2倍稀释法稀释成5个浓度梯度,按照1.2.7方法进行抑菌圈试验,得到毒力回归方程和EC50。依据Wadley法[20-21]进行药剂增效作用评价,即当SR>1.5时为增效作用,0.5≤SR≤1.5时为相加作用,SR<0.5时为拮抗作用。
增效系数(SR)的计算公式:
式中:A、B为杀菌剂在混剂中的比例;EC50(A)、EC50(B)为单剂抑制中浓度;EC50(TH)为理论抑制中浓度;EC50(OB)为实际抑制中浓度。
-
试验数据整理用Excel 2016进行,使用DPS 9.01计算毒力回归方程,使用SPSS 26.0并采用Duncan's新复极差法进行差异显著性分析。
1.1. 试验材料
1.1.1. 供试材料
1.1.2. 供试培养基
1.1.3. 供试药剂
1.2. 试验方法
1.2.1. 病原菌分离纯化
1.2.2. 菌株致病性初步鉴定
1.2.3. 病原菌致病性鉴定
1.2.4. 病原菌分子生物学鉴定
1.2.5. 病原菌形态学鉴定
1.2.6. 病原菌寄主范围测定
1.2.7. 单药剂对魔芋软腐病病原菌XM-6抑制作用测定
1.2.8. 复配药剂对魔芋软腐病病原菌XM-6抑制作用测定
1.2.9. 复配药剂对魔芋软腐病病原菌XM-6的协同增效作用
1.3. 统计分析
-
本试验共分离24株菌株,命名为XM-1~XM-24。接种试验结果表明,有2株菌株存在致病性,接种后球茎出现水浸状腐烂并散发恶臭,菌株XM-6的致病能力强于菌株XM-7,菌株XM-6致病能力表现为4级,菌株XM-7为3级(表 3)。科赫氏法则验证结果显示,接种后发病球茎中分离出的菌株与接种菌株一样,证明接种菌株为魔芋软腐病致原菌。
菌株XM-6和菌株XM-7致病性鉴定试验表明,接种24 h后魔芋球茎、叶柄和叶片(图 1b、c、e、f、h、i)都出现明显的发病情况,组织软化腐烂,并散发恶臭,且叶片和叶柄的发病速度比球茎快,对照组无发病症状(图 1a、d、g)。菌株XM-6在球茎、叶片和叶柄上的发病面积与严重程度均高于菌株XM-7,因此,后续室内药剂筛选试验以菌株XM-6为研究对象。
-
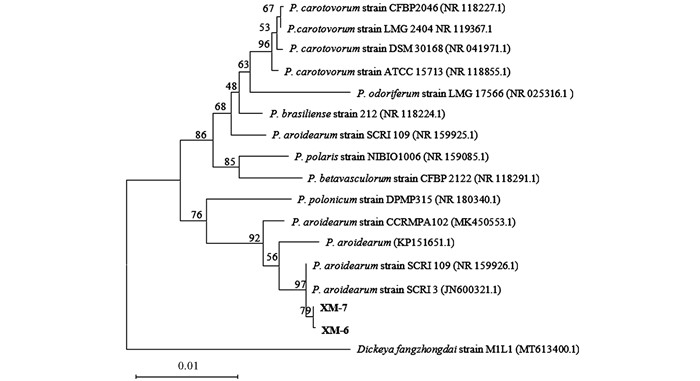
菌株XM-6和菌株XM-7的16S rDNA序列长度均为1 404 bp,序列相似性为99%,GenBank登录号分别为PV361861、PV361862。将测序结果进行BLAST比对,发现菌株XM-6和菌株XM-7的16S rDNA序列与已报道的标准菌株Pectobacterium aroidearum strain SCRI 109(NR159926.1)同源性最高,分别为99.86%、99.93%。以Dickeya fangzhongdai strain M1L1 (MT613400.1)为外群构建系统发育树(图 2),结果表明菌株XM-6和菌株XM-7与P. aroidearum strain SCRI 109、P. aroidearum strain SCRI 3、P. aroidearum strain CCRMPA102、P. aroidearum聚集在一个类群,因此菌株XM-6和菌株XM-7初步鉴定为Pectobacterium aroidearum。
-
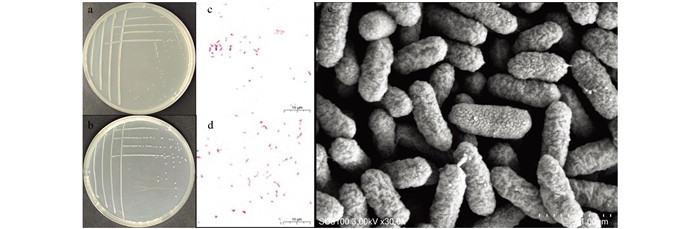
菌株XM-6和XM-7经28 ℃培养24 h后在NA培养基上都呈乳白色圆形,表面光滑、边缘齐整(图 3a、b),革兰氏染色结果为阴性(图 3c、d)。菌株XM-6在扫描电镜下呈短杆状,菌体直或稍弯曲(图 3e),符合Pectobacterium aroidearum的形态特征。
-
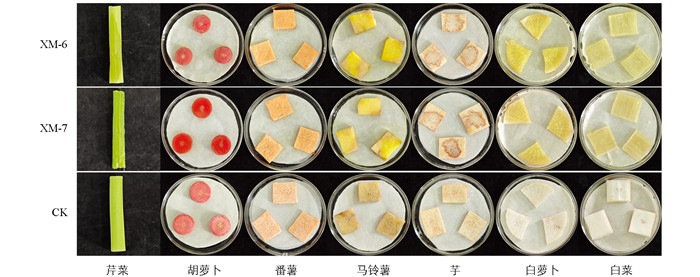
菌株XM-6和菌株XM-7对所选的7种作物均存在致病性,接种病原菌培养24 h后,芹菜(Apium graveolens)、胡萝卜(Daucus carota)、番薯(Ipomoea batatas)、马铃薯(Solanum tuberosum)、芋(Colocasia esculenta)、白萝卜(Raphanus sativus)、白菜(Brassica rapa)都有不同程度的发病(图 4),表现出水浸状病斑,组织软化溃烂并伴有浓烈的臭味。
-
供试的6种生物农药中有3种对菌株XM-6有抑制效果(表 4),分别是1%申嗪霉素SC(抗生素杀菌剂)、1%香芹酚AS(植物源杀菌剂)和0.5%大黄素甲醚AS(植物源杀菌剂);供试的8种化学农药中有4种对菌株XM-6有抑制作用(表 5),分别是80%福美双WG、3%噻霉酮ME、6%春雷霉素AS和50%咪鲜胺SC。将上述有抑制作用的药剂进行EC50测定,在生物农药中,1%香芹酚AS抑制活性最好,EC50为58.959 8 mg/L;1%申嗪霉素SC和0.5%大黄素甲醚AS抑制活性相差不大,EC50分别为306.545 5 mg/L、326.263 6 mg/L,但1%申嗪霉素SC在低浓度时无抑制作用(表 6)。在化学农药中,80%福美双WG抑制活性最好,EC50为10.863 3 mg/L,其次是EC50为35.576 9 mg/L的3%噻霉酮ME和EC50为112.133 9 mg/L的6%春雷霉素AS,50%咪鲜胺SC对菌株XM-6最不敏感(表 6)。
-
根据单剂测定结果,选择EC50低的药剂按不同比例进行复配,即生物农药1%香芹酚AS与化学农药80%福美双WG、3%噻霉酮ME分别进行复配。毒效比率测定结果如表 7,1%香芹酚AS∶80%福美双WG(2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1)以及1%香芹酚AS∶3%噻霉酮ME(6∶4、8∶2、9∶1)的复配组合毒效比率大于1,具有增效作用,其他组合均表现相加或拮抗作用。
在确定最佳组合的基础上,根据Wadley法评价复配药剂的增效作用(表 8),1%香芹酚AS∶80%福美双WG(8∶2、9∶1)有增效作用,增效系数(SR)分别是1.55、2.19;1%香芹酚AS∶3%噻霉酮ME(9∶1)有增效作用,增效系数(SR)是1.89。除1%香芹酚AS∶80%福美双WG(2∶8、3∶7)和1%香芹酚AS∶3%噻霉酮ME(6∶4)为拮抗作用外,其余的组合均为相加作用。
2.1. 病原菌分离与鉴定
2.1.1. 病原菌分离及致病性鉴定
2.1.2. 病原菌分子生物学鉴定
2.1.3. 病原菌形态学鉴定
2.1.4. 魔芋软腐病病原菌XM-6、XM-7寄主范围测定
2.2. 室内防治药剂筛选
2.2.1. 单药剂对魔芋软腐病病原菌XM-6的抑制效果
2.2.2. 复配药剂对魔芋软腐病病原菌XM-6的抑制效果
-
近年来,随着分子生物技术在细菌分类中的应用,很多病原菌的分类发生了变化,引起植物软腐病的病原菌也经历了多次变更,原来的欧文氏菌属(Erwinia)被拆分成5个属,其中能产生果胶酶的软腐欧文氏菌群现被归入果胶杆菌属(Pectobacterium)和迪基氏菌属(Dickeya)[22]。果胶杆菌属目前包含19个种,主要是胡萝卜果胶杆菌(P. carotovorum)、黑腐果胶杆菌(P. atrosepticum)、海芋果胶杆菌(P. aroidearum)、山葵果胶杆菌(P. wasabiae)、巴西果胶杆菌(P. brasiliense)等[23]。迪基氏菌属是2005年从后称菊果胶杆菌(Pectobacterium chrysanthemi)的欧文氏菌(Erwinia chrysanthemi)中分离出来的新属[24],目前包括12个种。引起魔芋软腐病的病原菌存在多样性,吴金平[25]对收集的33份魔芋软腐病病原菌进行鉴定,发现魔芋软腐病病原菌属于胡萝卜果胶杆菌胡萝卜亚种(P. carotovorum subsp.carotovorum)和菊果胶杆菌(P. chrysanthemi),还鉴定了一株新病原菌为肠杆菌科细菌(Enterobacter. sp.)。研究人员对湖北省宜昌市魔芋软腐病病原菌进行分离鉴定,发现主要是P. aroidearum和Dickeya fangzhongdai,其中P. aroidearum占66.7%[26]。还有其他报道也表明魔芋软腐病病原菌为P. carotovorum subsp.carotovorum、P. aroidearum、Dickeya sp.等[27-29]。综上所述,魔芋软腐病致病菌大多属于果胶杆菌属(Pectobacterium)和迪基氏菌属(Dickeya)。本研究经分离纯化得到菌株XM-6和菌株XM-7,它们的16S rDNA序列与已报道的标准菌株P. aroidearum strain SCRI 109(NR159926.1)同源性高达99%以上,在构建的系统发育树中与P. aroidearum明显聚为一个类群,基于形态学及16S rDNA将其鉴定为海芋果胶杆菌(Pectobacterium aroidearum)。Pectobacterium aroidearum一般被认为主要引起单子叶植物患病,但也能侵染其他植物引发细菌性软腐病[30],在大白菜、红泡椒、马铃薯、西葫芦[31-34]等植物中也有P. aroidearum致病的报道。病原菌寄主范围测定试验也表明分离出的病原菌寄主范围广泛,不仅能侵染魔芋,还能侵染伞形科(Umbelliferae)、旋花科(Ipomoea Batatas)、茄科(Solanaceae)、十字花科(Brassicaceae Burnett)等多种植物。在实际生产中要注意田间卫生管理,及时清除发病植株残体,避免出现交叉感染,同时,还应注意与非寄主作物轮作,减少病原菌积累等情况。
化学农药作用效果快,适用范围广,用药成本低,目前仍是病害防治的主要手段。生物农药来源广泛,选择性强,且不易产生抗药性,但在当前生产应用中占比依然较少。随着人们环保意识的不断增强,未来生物农药应用会越来越广泛[35]。化学农药和生物农药各有优缺点,将两种类型农药合理混配制成农药混剂,不仅能取长补短起到增效作用,还能减少环境污染,符合可持续发展的要求。本研究进行的室内药剂筛选试验发现生物农药1%香芹酚AS和化学农药80%福美双WG、3%噻霉酮ME对病原菌抑制效果最强,赵青华等[36]研究也表明3%噻霉酮WP对魔芋软腐病病原菌抑制效果较好,80%福美双WG和1%香芹酚AS在防治魔芋软腐病中尚未见报道。1%香芹酚AS是一种植物源杀菌剂,以香芹酚母药加工而成,是天然源的单帖类苯酚,具有抗病毒、抗菌的作用[37]。香芹酚对多种细菌和真菌有抑制作用,在防治马铃薯晚疫病、葡萄霜霉病、辣椒白粉病中表现良好[38-40]。将1%香芹酚AS与其他两种抑制效果好的化学农药合理复配,有望获得高效、安全的用药方案。在复配组合中1%香芹酚AS∶80%福美双WG(8∶2、9∶1)和1%香芹酚AS∶3%噻霉酮ME(9∶1)表现出增效作用,1%香芹酚AS∶80%福美双WG(9∶1)的效果最佳。但药剂在田间的表现还未明确,下一步需开展田间试验对室内筛选结果进行验证。
-
本研究从魔芋发病植株中分离纯化出XM-6和XM-7两个魔芋软腐病病原菌,结合形态学及分子生物学鉴定均为Pectobacterium aroidearum,并以菌株XM-6为研究对象筛选出对病原菌有抑制作用的最佳复配药剂组合;在室内药剂筛选中发现1%香芹酚AS∶80%福美双WG(9∶1)表现最佳,增效系数(SR)为2.19。本试验结果为生产上防治魔芋软腐病提供了一定的科学依据。






 DownLoad:
DownLoad: