-
开放科学(资源服务)标识码(OSID):

-
爬行动物中华鳖(Pelodiscus sinensis)隶属于龟鳖目鳖科鳖属,进化分支位于动物的中间位置,是物种进化和发育生物学研究的重要模式物种。中华鳖因其营养丰富、药用价值高成为我国两栖爬行类水产品中养殖规模最大的经济物种[1]。近年来,随着对珍稀野生动物种质资源的收集保护、集约型规模化养殖以及人工杂交、胚胎移植等繁殖调控技术的普遍应用,对中华鳖产业提出了更精准可控的发展要求。生殖细胞作为遗传信息传递的唯一途径,通过减数分裂产生单倍体配子,将遗传信息代代相传,是物种优良性状传递的载体[2-3]。因此,深入了解和探讨中华鳖生殖细胞发育分化机制尤为重要。
Stra8 (Stimulated by retinoic acid gene 8)是启动生殖细胞减数分裂的特异标记基因,在有丝分裂向减数分裂转变的过程中发挥重要作用[4]。Stra8基因首先在小鼠(Mus musculus)中被鉴定出来[5],随后在人(Homo sapiens)[6]、猪(Sus scrofa)[7]等其他哺乳动物和鸡(Gallus gallus)[8]等鸟类以及南方鲇(Silurus meridionalis)[9-10]、大西洋鲑(Salmo salar)[11]等硬骨鱼类中也发现了其同源基因。在哺乳动物中,stra8的表达受视黄酸(RA)诱导[12]。视黄酸进入细胞核后,结合其特异性核受体(RARs)和视黄酸X受体(RXRs)形成异二聚体,该异二聚体再结合stra8启动子上的视黄酸反应元件(RAREs)调控stra8的表达[13-15]。通过对stra8启动子上RAREs进行突变和缺失,明确了RAREs是RA诱导stra8表达的重要元件[3]。在小鼠胚胎卵巢中,RA通过诱导stra8在雌性生殖细胞中启动减数分裂[16-18]。在胚胎睾丸中,视黄酸降解酶(Cyp26b1)通过降解RA阻断RA信号,使stra8表达缺失。13.5 d后胚胎中Cyp26bl的表达逐渐降低,Nanos2被激活并抑制stra8的表达,从而阻止雄性生殖细胞启动减数分裂[15, 17]。在出生后至成年的睾丸中,精原细胞附近的支持细胞产生RA,诱导stra8表达促使精原细胞增殖和分化[19]。
可变剪切又叫选择性剪切,在真核生物中普遍存在,指基因在转录后和mRNA形成前,被剪切形成不同的mRNA异构体,而这些mRNA异构体可能被翻译成不同的蛋白质构体。选择性剪切主要有以下5种方式:外显子跳跃、外显子互斥、5′端选择性剪切、3′端选择性剪切、内含子保留[20]。选择性剪切在真核生物的生殖繁殖、信号传导等过程中发挥重要的生物学作用。前期研究发现中华鳖stra8基因存在选择性剪切现象,本研究通过对中华鳖基因组和转录组中获取的stra8序列进行分析,发现其有19个剪切体。首先分析stra8基因结构和选择性剪切类型以及不同剪切体的转录表达水平,以获得该基因主要行使功能的转录本; 接着通过PCR克隆得到该基因的cDNA片段和启动子序列并对其进行了生物信息学分析。
HTML
-
本研究供试中华鳖购自重庆市某中华鳖养殖场。暂养后随机选取健康的1冬龄雌、雄中华鳖各3只,经酒精消毒后在无菌环境中采用MS222麻醉,然后放血解剖。收集雌、雄性的中华鳖心脏、肝脏、脾脏、肾脏、脑、卵巢和精巢组织,将其迅速在液氮中冷冻后置于-80 ℃冰箱保存用于RNA的提取。
-
中华鳖总RNA和DNA的提取采用Trizol法。将保存的中华鳖组织(心脏、肝脏、脾脏、肾脏、脑、卵巢和精巢)经冷冻研磨后,加入Trizo RNAiso Plus(Takara)进行总RNA提取,使用TlANamp Genomic DNA Kit(Tiangen)提取DNA,方法参考说明书。提取的RNA和DNA用NanoDrop 2000微量分光光度计和1%琼脂糖凝胶电泳进行检测,以确定其浓度和质量。质检合格的RNA使用Takara PrimeScript RT reagent Kit with gDNA Eraser Kit反转录获得cDNA(用于RT-PCR和RT-qPCR),于-20 ℃冰箱保存备用。
-
为了明确中华鳖stra8基因不同转录本的组织表达情况,根据NCBI中stra8的序列,设计RT-PCR定量引物,选择中华鳖的ef1α作为内参基因,引物序列见表 1。RT-PCR反应体系为:上、下游引物各0.8 μL,2×Taq Master Mix(Tiangen)10 μL,ddH2O 7.4 μL,模板cDNA 1 μL,共20 μL。反应程序为:95 ℃ 3 min,95 ℃ 10 s,60 ℃ 15 s,72 ℃ 10 s,第2-4步进行35个循环。PCR产物用2%琼脂糖电泳检测。
RT-qPCR采用CFX ConnectTM荧光定量PCR检测系统(Bio-Rad,USA)测定。不同转录异构体的特异引物序列见表 1。反应体系为上、下游引物各0.8 μL,2×TB Green® Premix Ex TaqTM(Tli RNaseH Plus)10 μL,ddH2O 7.4 μL,模板cDNA 1 μL,共20 μL。扩增程序为:在95 ℃高温环境中进行30 s预变性,5 s变性,随后在60 ℃下进行30 s扩增,变性与扩增重复40个循环。扩增程序结束后,在95 ℃下进行10 s变性,再按每0.05 s升高0.5 ℃的速度,将反应温度从65 ℃升到95 ℃,生成溶解曲线。试验设置3个生物学重复,基因的相对表达量采用2-ΔΔCT方法计算,使用SPSS 20.0对数据进行Turkey方差分析,采用GraphPad Prism 8.0作图。
-
根据NCBI stra8基因序列,分别设计stra8基因克隆和启动子克隆引物(表 1)。基因克隆以中华鳖雌、雄性腺cDNA等量混合物为模板,启动子克隆以提取的DNA为模板,均使用PrimerSTAR® Max DNA Polymerase(Takara)进行PCR。PCR产物采用rTaq酶在72 ℃下反应30 min加A后连接pGEM-T easy载体,转化大肠杆菌感受态(Top10)后进行蓝白斑筛选。挑取白色单克隆菌斑在LB(Luria-Bertani)液体培养基、37 ℃摇床180 r/min转速下过夜培养。采用2×Taq Master Mix(Tiangen)进行菌液PCR后获得阳性克隆,送重庆擎科生物科技有限公司测序。
-
本研究采用的生物信息学分析软件如表 2所示。用Vector NTI 10.0软件对推导的中华鳖Stra8氨基酸序列与NCBI数据库中其他物种Stra8的氨基酸序列进行多重比对分析。采用MEGA 7.0软件构建系统进化树,计算方法为Neighbour-Joining(NJ),boostrap值设置为1 000。使用Neural Network Promoter Prediction预测中华鳖stra8基因5′端转录起始位点(TSS); 使用PROMO、AliBaba 2.1对潜在转录因子结合位点进行预测。
1.1. 实验材料
1.2. 中华鳖组织DNA和总RNA提取及cDNA合成
1.3. Stra8基因在中华鳖不同组织中的表达分析
1.4. 中华鳖stra8基因和启动子克隆
1.5. 生物信息学在线分析
-
从NCBI数据库中获取了中华鳖stra8基因的19个mRNA序列及其参考基因组,锚定了stra8基因在基因组序列中的位置,确定了stra8基因的DNA序列全长为28 476 bp,包括10个外显子和9个内含子(图 1a),遵循GT-AG剪切规律。序列比对发现stra8基因19个转录本的第Ⅲ、Ⅴ-Ⅹ个外显子未发生剪切; 第Ⅰ个外显子在第2-5、7、10、12、16、18、19号转录本上发生了3′端选择性剪切,在第17号转录本上既发生了5′端选择性剪切又发生了3′端选择性剪切; 第Ⅱ个外显子在第1、2、5、7、9、10、14、16、18、19号转录本中发生了跳跃; 第Ⅳ个外显子在第11-19号转录本发生了跳跃,且仅在第4号转录本发生3′端选择性剪切。由此可见,stra8基因主要发生了5′端和3′端选择性剪切以及外显子跳跃等剪切事件。
-
为挖掘出stra8主要行使功能的转录本和相应的多肽序列,首先对stra8不同转录本编码的氨基酸序列进行比对,结果发现19个转录本共翻译5种多肽序列:第3号转录本编码第1种多肽序列,第4号转录本编码第2种多肽序列,第5号转录本编码第3种多肽序列,第1、2、6-10号转录本编码第4种多肽序列,第11-19号转录本编码第5种多肽序列(图 1b)。由图 1b可见,第5种多肽序列N端不再具有典型的HLH结构域。
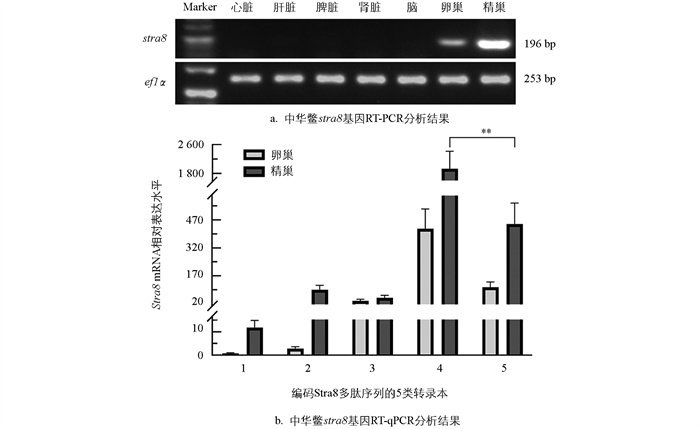
根据中华鳖stra8 19个转录本的共有序列,设计定量引物(表 1),获取1冬龄中华鳖各组织的cDNA,以ef1α作为内参基因,利用特异性引物进行RT-PCR,检测stra8基因在不同组织中的表达情况。结果显示,未在心脏、肝脏、脾脏、肾脏、脑组织中观察到stra8产物条带,仅在卵巢、精巢中分别检测到较弱、较强的条带,表明stra8 mRNA在性腺组织中特异表达,且在精巢中的表达水平高于卵巢(图 2a)。针对编码这5种多肽序列对应的转录本序列设计特异引物(表 1),在中华鳖雌、雄性腺中进行RT-qPCR。结果表明,检测的5类转录本在精巢中的表达量均高于卵巢(图 2b),与RT-PCR检测结果一致(图 2a)。在雌、雄性腺中的表达水平都最高的是编码第4种多肽序列的转录本,其次是编码第5种多肽序列的转录本,且前者在精巢中的表达水平极显著高于后者(图 2b)。由此推测,编码第4种多肽序列的转录本是stra8中主要行使生物学功能的转录本,其编码的蛋白为功能性蛋白。
-
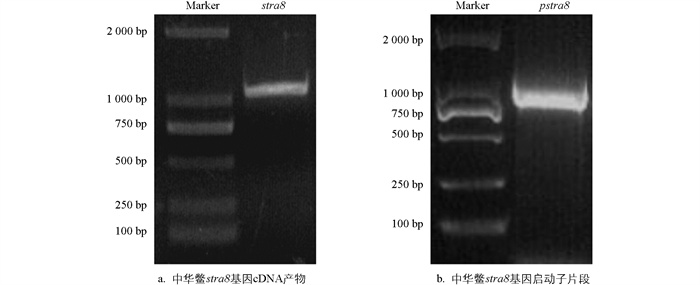
根据2.2节的研究结果可知,编码第4种多肽序列的转录本是stra8中主要行使生物学功能的转录本。根据其序列信息,设计stra8基因cDNA扩增引物(表 1)。以中华鳖性腺cDNA为模板,进行RT-PCR扩增,获得的stra8基因cDNA 1 113 bp(图 3a)包含3′端非编码区54 bp以及一个长度为1 059 bp的开放阅读框,开放阅读框共编码352个氨基酸。
此外,为获得stra8启动子片段,根据中华鳖基因组序列设计引物,以基因组DNA为模板进行PCR扩增,得到的启动子片段长度为1 052 bp(图 3b)。
-
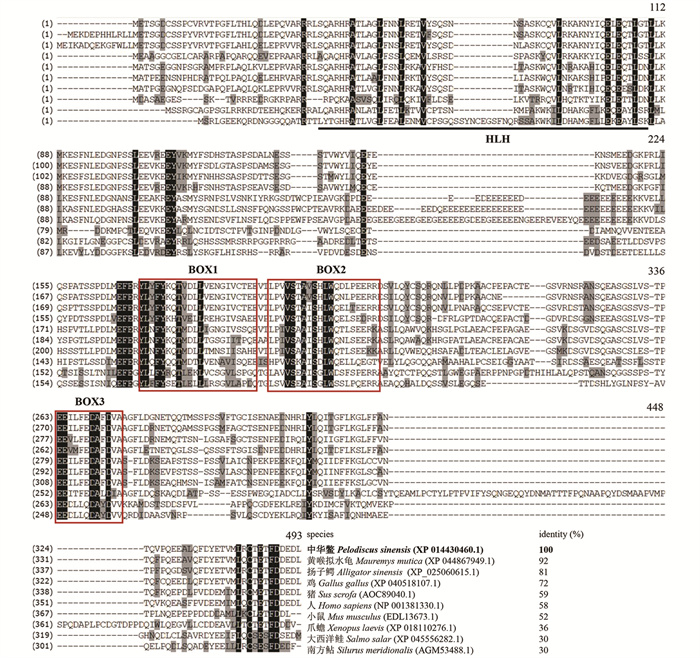
采用Vector NTI 11.0软件对中华鳖与其他物种Stra8蛋白进行多重序列比对(图 4)。结果表明,中华鳖Stra8蛋白N端含有一个保守的HLH结构域。HLH结构域是Stra8与其他bHLH转录因子互作的结构域。此外,3个BOX结构域是Stra8蛋白在脊椎动物中的保守结构域。由此可见,Stra8氨基酸序列在进化中较保守,但是因物种进化程度不同而呈现出一定的差异。中华鳖与黄喉拟水龟(Mauremys mutica)Stra8序列一致性最高,达92%; 其次与爬行动物扬子鳄(Alligator sinensis)Stra8序列一致性较高,为81%; 与鸟类鸡Stra8序列一致性可达72%; 与哺乳类动物猪、人和小鼠等Stra8序列一致性较低,分别为59%、58% 和52%; 与两栖类爪蟾(Xenopus laevis)Stra8序列一致性低至36%; 与硬骨鱼类大西洋鲑和南方鲇Stra8序列一致性最低,均为30%。
基于中华鳖和其他物种Stra8的氨基酸序列,在Mega 7.0软件中采用邻接法进行1 000次bootstraps验证构建了系统发育树,展示了中华鳖与其他物种Stra8之间的进化关系(图 5)。进化分析表明Stra8主要聚为四足动物类和硬骨鱼类两大分支。中华鳖Stra8聚类到爬行类,并与黄喉拟水龟聚类到一个分支; 与鸟类、哺乳类、两栖类亲缘关系依次降低,与硬骨鱼类亲缘关系最远。
-
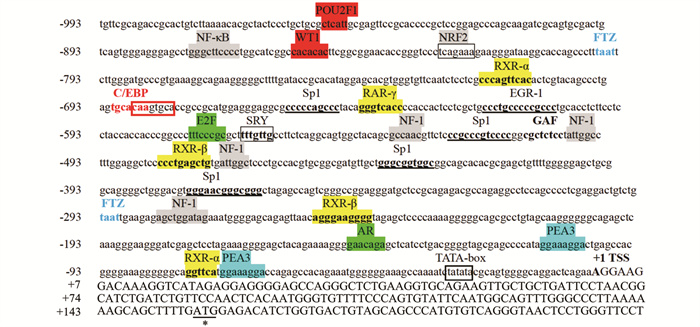
本研究扩增得到的中华鳖stra8基因启动子片段长度为1 052 bp(图 3b),而设计目标长度为1 044 bp。通过序列比对发现,获得的启动子序列有8 bp的碱基插入(图 6红色矩形框所示),其他序列相同。生物信息学分析显示stra8基因启动子区存在1处TATA box,无GAAT box; 通过Neural Network Promoter Prediction分析预测到共3个可能的TSS。结合上游-25~30 bp的TATA box位置分析,最有可能的TSS位于第993位,定为+1位(图 6)。
为预测stra8启动子上游潜在的转录因子结合位点,本研究采用PROMO、AliBaba 2.1等在线数据库进行检索与分析,结果见图 6。如图 6所示,部分预测蛋白与转录调控活性直接相关:Sp1作为序列特异性DNA结合蛋白,可调控启动子中富含GC序列的基因转录; GAF与靶基因结合并移除核小体,使启动子区域暴露,从而促进转录激活; C/EBP也被证实广泛参与转录调控过程。此外,部分蛋白主要涉及细胞生长、增殖、分化及保护等功能:RAR/RXR通过响应视黄酸信号直接调控细胞减数分裂启动; AR通过与雄激素配体结合,诱导具有性别依赖性相关基因的转录激活; E2F转录因子参与细胞周期的调控; PEA3是多种细胞的增殖、迁移、分化中重要的转录调控因子; WT1参与多个器官的发育调控,可能与性腺体细胞分化、性别控制等有关; EGR-1参与调控细胞生长、分化、应激反应及免疫反应; FTZ在类固醇的生成和性别分化过程中发挥着重要的作用; NF-1在调控细胞生长、增殖和分化过程中扮演重要角色; NRF2参与氧化还原平衡、线粒体自噬、DNA修复、屏障修复、脂质代谢等,通过解毒机制产生细胞保护作用。
2.1. 中华鳖stra8基因可变剪切分析
2.2. 中华鳖stra8 mRNA的组织特异性表达
2.3. 中华鳖stra8基因和启动子的克隆
2.4. 中华鳖stra8基因cDNA序列生物信息学分析
2.5. 中华鳖stra8基因启动子序列分析
-
目前,中华鳖是我国两栖爬行类水产养殖规模最大的经济物种,且具有明显的性别差异,雄性相比雌性具有体型大、生长速度快、脂肪少的特点[21]。已有研究表明减数分裂启动时间与性别决定和分化密切相关。减数分裂在胚胎期启动,则生殖细胞向雌性方向发育; 减数分裂在出生后启动,则生殖细胞向雄性方向发育。而stra8基因是减数分裂启动的“守门员”,在减数分裂启动中发挥重要的作用。
据统计,90%~95%的人类基因经历了一定程度的选择性剪切[22-23]。人类蛋白质编码基因的37%产生了多种蛋白亚型[24],这表明选择性剪切有助于蛋白质组复杂性的维持、细胞分化及其谱系的决定、组织身份的获取和维持、器官的发育[25]。不同物种中基因的选择性剪切均影响其生长发育,如三疣梭子蟹(Portunus trituberculatus)iag存在不同剪切体,在三疣梭子蟹雄性分化及维持中具有重要功能[26]。鸡的glut4基因通过多种剪切机制共产生14个转录本,编码12种氨基酸序列,具有明显不同的亚细胞定位,推测glut4在鸡的生长发育过程中发挥了重要的生理功能[27]。在幼年小鼠的两性性腺中,stra8缺陷(外显子2~7缺失)的生殖细胞都无减数分裂启动的分子特征,并且不能进入减数分裂[16, 18]。本研究中,stra8基因主要通过5′端选择性剪切、3′端选择性剪切和外显子跳跃等剪切事件共产生19个剪切体,共可翻译形成5种多肽序列。剪切位置主要发生在序列的5′端,尤其是在第Ⅰ个外显子上。通过序列比对发现,部分序列的第Ⅱ个外显子发生了跳跃,但不影响翻译; 而第Ⅳ个外显子发生了跳跃,导致编码蛋白的N端发生了变化。由图 1b所示,第5种多肽序列N端氨基酸序列不再具有HLH结构域。由此可见,虽然stra8基因剪切转录本多达19个,但最终只翻译形成了5种多肽序列,其目的是保证stra8的成功转录,确保功能性蛋白的形成,进而维持生命活动正常进行。但不同的蛋白异构体也可能在不同的时空发挥不同的功能,该问题有待进一步探究。
RT-PCR结果显示stra8基因在1冬龄雌、雄中华鳖性腺中特异表达,RT-qPCR结果表明所有转录本在精巢中的表达量高于卵巢。这与南方鲇stra8在精巢和卵巢的表达水平相似这一结果不同[28],与鼠、猪stra8仅在成体组织精巢中表达[29-31]的情况也不同。此外,本研究中,中华鳖stra8基因的转录表达水平在1冬龄精巢中显著高于卵巢,说明此时中华鳖卵巢绝大部分雌性生殖细胞减数分裂启动已完成,而精巢雄性生殖细胞减数分裂启动正处在高峰期,生殖细胞向雄性方向发育。中华鳖Stra8蛋白在进化中较保守,与其他物种同源蛋白一样,在N端均含有一个保守的HLH结构域,在C端均含有3个BOX结构域。其中HLH结构域是Stra8与其他bHLH转录因子互作的结构域,预示着Stra8常与其他蛋白互作发挥作用。Stra8是RA的靶基因之一,其启动子区域包含推测的RAREs[18, 32-33],在小鼠中已证实RARs直接与出生后小鼠睾丸中Stra8启动子区域的RAREs结合[34]。本研究中,RAR、RXR视黄酸受体结合位点的存在表明RA-Stra8信号的保守性,推测stra8的表达也受控制RA水平的酶Aldh1a和Cyp26a1的间接调控。
综上,本研究明确了中华鳖stra8基因含有10个外显子和9个内含子,基因在转录过程中主要发生了5′端选择性剪切、3′端选择性剪切和外显子跳跃等剪切事件。Stra8基因在性腺中特异表达,且在精巢中的表达量高于卵巢,编码第4种多肽序列的转录本是stra8主要行使功能的转录本。克隆得到了stra8基因cDNA和启动子片段:CDS编码的氨基酸序列与爬行类同源蛋白具有很高的相似性,与鱼类一致性较低,但仍比较保守。启动子片段中含有RAR、RXR等转录因子结合位点,表明stra8的转录可能受视黄酸途径相关蛋白的调控。







 DownLoad:
DownLoad: