-
开放科学(资源服务)标识码(OSID):

-
植物源农药是来源于植物体的农药,是从人工栽培或野生植物中提取的活性成分,其有效成分通常不是单一化合物,而是植物有机体中的一些、甚至大部分有机物质[1]。它可以帮助植物应对病虫害的侵袭和不良的环境条件,是植物自我防御功能进化和演变的结果。植物源农药通常都是以比较复杂的作用途径起到杀虫、杀(抑)菌、除草等效果,与化学农药相比,因其来源于自然,更容易降解,对环境污染较小;一般情况下也不会对环境和农产品造成污染,不会在环境和人体中累积,具有低毒、低残留的特性,对环境友好,不易产生抗性等[2]。研究表明,在植物源农药中使用最多的化合物是生物碱、黄酮类、萜类和挥发油等,且不同种类化合物的骨架结构各异[3]。我国幅员辽阔、植物资源丰富,多种多样的植物活性物质既可用于传统药材,又可作为筛选、开发和应用植物源农药的优质资源。
植物源农药能钝化病毒,并能诱导植物产生抗药性。如对烟草花叶病毒(tobacco mosaic virus,TMV)有明显体外钝化作用且对多种植物病毒病有良好防治效果的植物源抗病毒剂VFB,它能有效提高植物的抗病性[4]。有研究发现蛇床子提取物对TuMV具有明显的钝化效果[5]。刘学端等[6]用商陆、甘草、连翘为原材料制成的复方制剂处理烟草,结果显示,在烟草中,POD的活性明显增强,说明植物源农药能诱导烟草的抗病效应。陈伟[7]研究发现,植物提取物WCT-Ⅱ能够诱导烟草SOD、POD、多酚氧化物酶(PPO)的活性上升,诱导过氧化氢酶积累和PR-1基因上调,从而对烟草系统的抗病性产生诱导作用。林中正[8]在30种植物源提取物中筛选出银杏、栀子、商陆、赤芍的提取物对TMV具有一定的抑制作用,经过复配,防效可达95.23%。景炳年[9]采用半叶枯斑法研究发现27个科48种54个植物粗提物对TMV具有良好的体外钝化活性,其中宽果红景天、糯米条、粗榧、牛心朴子草、臭椿和雷丸对TMV的预防和增殖具有抑制作用;雷丸提取物对植物源抗病毒剂VBF水剂还表现出明显的增效作用。陈启建[10]研究发现从金鸡菊与小白菊分离的化合物对TMV的侵染有抑制作用,对TMV的增殖也有明显抑制作用;复配后可提高烟草中PPO、POD、SOD和苯丙氨酸解氨酶(PAL)的活性及叶绿素的含量。
芦苇(Phragmites australis)是多年水生或湿生的高大禾草,属于禾本科芦苇属,是湿地环境中生长的主要植物之一,分布广,在世界各地均有生长,其抗性强,是重要的药用植物,芦叶、芦花、芦茎、芦根、芦笋均可入药[11]。研究表明,芦苇提取物对细菌和霉菌具有一定的抑制作用[12]。芦苇提取物对番茄早疫病菌、小麦赤霉病菌和瓜类枯萎病菌等的抑制率可达85%[13]。芦苇提取物中的黄酮类物质还具有抗氧化作用,因此研究芦苇提取物抗病毒作用具有重要的现实意义。在我国的植物源农药中,植物病毒抑制剂的研发速度远不及杀虫剂、杀菌剂和除草剂,其主要原因在于植物源提取物抗病毒机制尚不明确,并且植物源抗病毒抑制剂的筛选还存在着盲目、重复等问题,为此,应加大对植物源产物的筛选力度,完善其抗病毒体系。本研究以本氏烟为试验材料研究芦苇提取物对马铃薯X病毒(PVX)、马铃薯Y病毒(PVY)和芜菁花叶病毒(TuMV)的抑制作用,旨在为植物源病毒抑制剂的筛选和研发提供数据支持。
HTML
-
供试植物:本氏烟在22 ℃的温室中,光照16 h和黑暗8 h条件下进行培养,选取3~5叶期、长势均一的植株进行试验。
植物源提取物:90%芦苇提取物、98%鱼腥草提取物、95%芦荟多糖,西安金润生物科技有限公司;宁南霉素,德强生物股份有限公司。
供试病毒:PVX、TuMV的侵染性克隆和PVY的毒源均由内蒙古农业大学生物农药创制与资源利用内蒙古自治区高等学校重点实验室提供,其中TuMV中融合了GFP基因,命名为TuMV-GFP;PVY中融合了Rosea1基因,命名为PVYros。
主要仪器及试剂:ransScript® One-Step gDNA Removal and cDNA Synthesis Super Mix试剂盒,TransGen Biotech;TB Green® Premix Ex TaqTM Ⅱ试剂盒,TARAKA;SOD、PPO和POD酶活性检测试剂盒,北京盒子生工科技有限公司;化学发光成像系统(Odyssey® Fc),美国莱科公司;便携式植物营养测定仪,杭州绿博仪器有限公司。
-
将PVX和TuMV-GFP的侵染性克隆通过液氮冻融法转化到农杆菌C58C1中,并通过农杆菌浸润法接种到本氏烟植株上;PVYros通过摩擦接种法接种到本氏烟植株上。待植株发病后,采集症状明显的系统叶片在液氮中研磨成粉,作为毒源置于-80 ℃超低温冰箱内保存备用。
-
鱼腥草提取物、芦苇提取物和芦荟多糖的质量浓度均为5 mg/mL,以无菌水作为对照。先将其均匀涂抹在本氏烟的第3、4片叶上,在温室中培养6 h后,将PVX接种在涂抹了植物源提取物的叶片上,每个处理接种6株本氏烟,观察并记录发病情况。
-
将200 mg/mL的芦苇提取物涂抹在本氏烟第3、4片叶上,以宁南霉素水剂和无菌水为对照,6 h后分别接种PVYros和TuMV-GFP;接种后的植株继续在温室中培养,每个处理接种6株本氏烟,观察并记录发病情况。
-
病情分级标准为[14]:0级:全株无病;1级:心叶脉明或轻微花叶,或上部1/3叶片花叶,但不变形,植株无明显矮化;2级:1/3至1/2叶片花叶,或少数叶片变形,或主脉变黑,植株矮化为正常株高的2/3以上;3级:1/2至2/3叶片花叶,主侧脉坏死或变形,植株矮化为正常株高的1/2至2/3;4级:整株叶片花叶,严重变形或坏死,病株矮化为正常株高的1/3至1/2。病情指数(D)及相对防效(E)计算公式为[15]:
式中:S为各级病株数;L为相应级别;T为调查总株数;M为最大级别。
式中:DCK为空白对照病情指数;Dh为处理病情指数。
-
通过RT-qPCR对PVX CP的表达量进行检测。采集接种PVX后8 d各处理本氏烟的系统叶,在液氮中研磨成粉后通过TRNzol法提取总RNA,并进行逆转录,获得cDNA。根据PVX CP序列设计特异性引物,由生工生物工程(上海)股份有限公司合成。上游引物为PVX CP (el)-F(5′-CACAGCCCATAGGGTCAACT-3′),下游引物为PVX CP (el)-R(5′-GCCTCAATCTTGCTGAGGTC-3′)。以NtUB1基因作为内参[16],上游引物为NtUB1-F(5′-TCCAGGACAAGGAGGGTATCC-3′),下游引物为NtUB1-R(5′-GTCAGCCAAGGTCCTTCCATCC-3′),用于qPCR检测,采用2-ΔΔCt方法计算PVX CP的相对表达量[17]。
-
在接种PVYros和TuMV-GFP后12 d采集各处理系统叶片,在液氮中研磨成粉后提取总蛋白进行Western Blot检测[16]。PVYros和TuMV-GFP分别对PVY CP和GFP进行检测以确定病毒积累量。提取的总蛋白经12% SDS-PAGE电泳后,转至PVDF膜并进行封闭;分别用PVY CP(一抗1∶1 000,二抗1∶5 000)和GFP(一抗1∶500,二抗1∶5 000)特异性抗体进行孵育后,加入适量ECL化学发光液显色,并进行信号检测。
-
叶绿素含量和氮含量测定:在本氏烟接种PVYros和TuMV-GFP 12 d后,使用便携式植物营养测定仪对本氏烟叶片叶绿素(以SPAD值表示)和氮含量进行检测,测定时间为上午9-11时,检测每株第3系统叶片,每叶片检测3次后求平均值[18]。在本氏烟接种PVYros和TuMV-GFP 12 d后,采集系统叶并在液氮中研磨成粉后用于植物抗病相关酶SOD、PPO和POD活性的检测,具体检测方法见试剂盒说明书。
1.1. 试验材料
1.2. 试验方法
1.2.1. 病毒毒源的制备
1.2.2. 芦苇提取物对PVX的抑制作用
1.2.3. 芦苇提取物对PVY和TuMV的抑制作用
1.2.4. 病情分级标准及防效计算
1.2.5. RT-qPCR检测PVX表达量
1.2.6. Western Blot检测PVY和TuMV的积累量
1.2.7. 接种病毒后本氏烟植株生理指标测定
1.2.8. 芦苇提取物化学成分分析
-
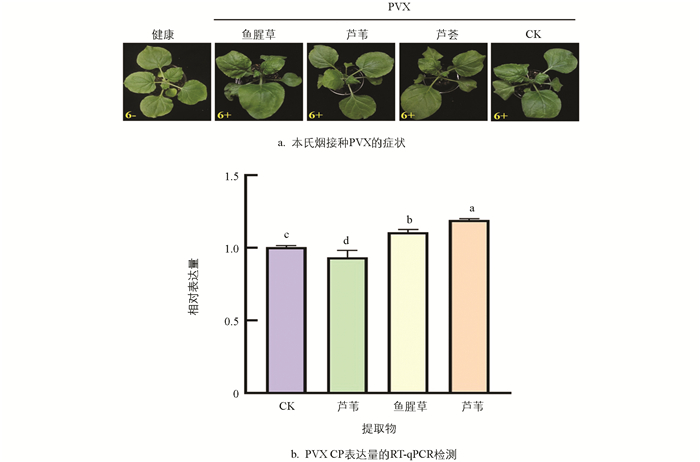
将芦苇提取物涂抹于本氏烟上,6 h后接种PVX,研究芦苇提取物对PVX的抑制作用。结果表明,接种PVX 6 d,各处理植株开始出现PVX的症状,其中芦苇提取物处理的本氏烟发病最轻,接种的6株本氏烟中有4株出现症状,且病情指数最低,平均病情指数为25.00,相对防效达到了50.00%;其次是鱼腥草提取物,与无菌水处理(CK)一样,处理的6株本氏烟中均有5株出现症状,但其平均病情指数为33.33,相对防效为33.34%,无菌水处理的本氏烟平均病情指数为50.00;芦荟提取物处理的6株本氏烟全部出现症状,且平均病情指数为54.17。随着接种时间的增加,各处理的发病株数和病情指数逐渐增加,相对防效逐渐降低,但芦苇提取物的病情指数始终低于其他处理,同时,相对防效始终高于其他处理(表 1)。接种PVX 8 d,各处理植株全部出现症状(图 1a),芦苇提取物处理的本氏烟的平均病情指数为62.50,相对防效为16.67%;而鱼腥草提取物和芦荟提取物对PVX均无防效。对接种PVX 8 d各处理本氏烟进行RT-qPCR检测,结果显示,与无菌水处理相比,经芦苇提取物处理的本氏烟中PVX CP相对表达量显著降低(图 1b)。
-
采用圆形滤纸法对芦苇提取物中的化学成分进行检测,酸性成分检测包括酚类和生物碱,结果均呈阳性(+)。此外,pH试纸测定显示芦苇提取物的pH值为7.5~9.0,表明其整体呈弱碱性,可能与生物碱的富集有关。黄酮及强心苷检测均呈阳性。有机酸通过pH试纸间接验证,表明芦苇提取物中酸性成分与碱性成分共存。结果表明,芦苇提取物中所含有的化学成分包括酚类、生物碱、黄酮、强心苷和有机酸(表 2)。
-
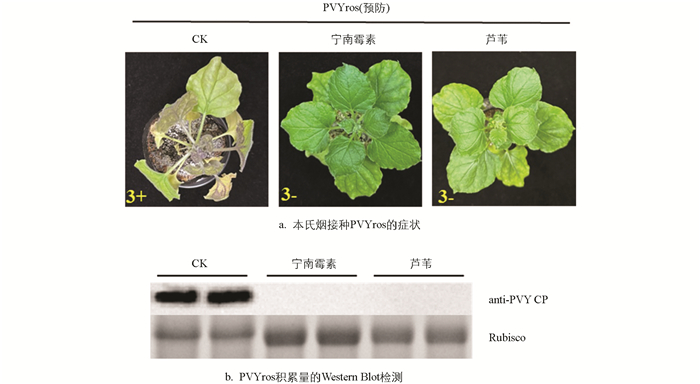
将芦苇提取物涂抹于本氏烟上,6 h后接种PVYros,研究芦苇提取物对PVY的抑制作用,对各处理本氏烟的症状进行观察并统计病情指数。结果表明,接种PVYros 8 d,无菌水处理(CK)的本氏烟开始出现PVY的症状,接种的6株本氏烟中有3株发病,其平均病情指数为12.50;芦苇提取物和宁南霉素处理的本氏烟均未发病。随着接种时间的增加,无菌水处理的本氏烟的发病株数和病情指数逐渐增加。接种PVYros 10 d,无菌水处理的6株本氏烟全部发病,其平均病情指数为50.00;接种PVYros 11~12 d,无菌水处理的本氏烟症状逐渐加重,平均病情指数分别为79.17和87.50(表 3)。芦苇提取物和宁南霉素处理的本氏烟始终未出现PVY的症状(图 2a),与无菌水处理相比,芦苇提取物对PVYros的侵染具有较好的抑制作用,且相对防效能够达到100%。在接种PVYros 12 d时,通过Western Blot对各处理PVYros积累量进行检测,无菌水处理的本氏烟中检测到了PVY CP,而宁南霉素和芦苇提取物处理均未检测到PVYros的积累(图 2b)。
-
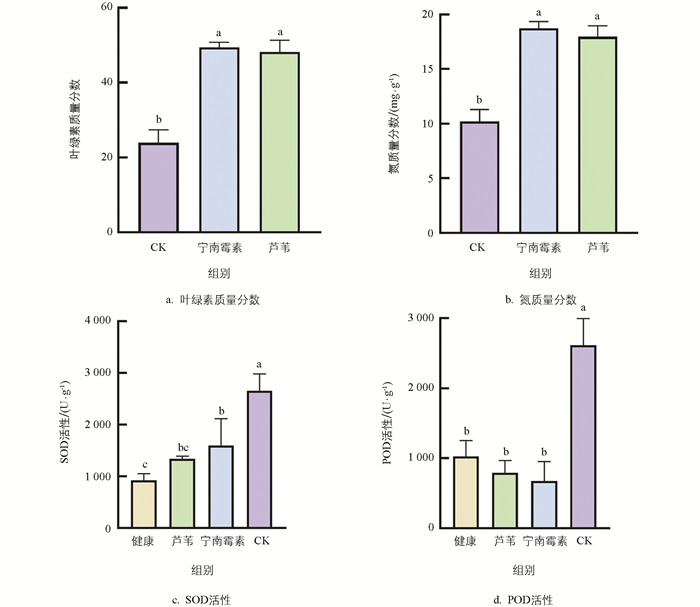
对接种PVYros 12 d的本氏烟中叶绿素、氮含量及抗性相关酶SOD和POD活性进行检测,结果表明,芦苇提取物和宁南霉素处理本氏烟叶片的平均叶绿素质量分数(分别为48.22和49.45)显著高于无菌水处理(23.92,p<0.05)(图 3a)。芦苇提取物和宁南霉素处理的本氏烟叶片的平均氮质量分数(分别为17.96 mg/g和18.73 mg/g)也显著高于无菌水处理(10.21 mg/g,p<0.05),其变化趋势与叶绿素基本一致(图 3b)。芦苇提取物处理的本氏烟中SOD活性(1 338.36 U/g)较无菌水处理(2 652.93 U/g)显著降低(p<0.05),但与健康植株和宁南霉素处理(分别为925.77 U/g和1 595.64 U/g)相比,差异无统计学意义(图 3c)。芦苇提取物处理的本氏烟中POD活性(793.33 U/g)较无菌水处理(2 613.33 U/g)显著降低(p<0.05),但与健康植株和宁南霉素处理(分别为1 026.67 U/g和673.33 U/g)相比,差异无统计学意义(图 3d)。
-
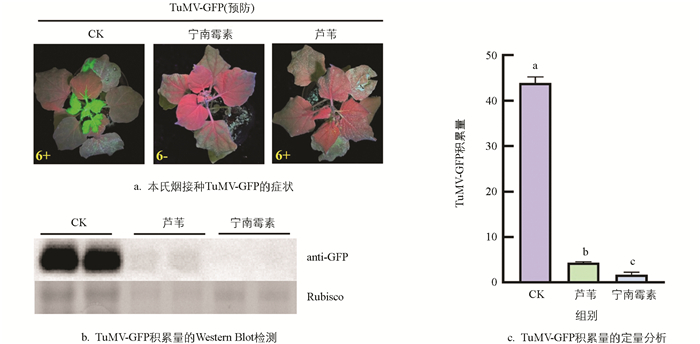
将芦苇提取物涂抹于本氏烟上,6 h后接种TuMV-GFP,研究芦苇提取物对TuMV的抑制作用。结果表明,接种TuMV-GFP 5 d,无菌水处理(CK)的本氏烟开始出现TuMV的症状,在紫外灯下可以观察到荧光;接种的6株本氏烟中有3株发病,其平均病情指数为16.67;而芦苇提取物和宁南霉素处理的本氏烟均未发病。接种TuMV-GFP 7 d,芦苇提取物处理的本氏烟开始出现TuMV的症状,接种的6株本氏烟中有4株发病,其平均病情指数为16.67;此时,无菌水处理的本氏烟平均病情指数为54.17。随着接种时间的增加,无菌水和芦苇提取物处理的本氏烟发病株数和病情指数逐渐增加,芦苇提取物的防效逐渐降低。接种TuMV-GFP 11 d,芦苇提取物处理的6株本氏烟全部发病,其平均病情指数为54.17,相对防效为31.58%;接种TuMV-GFP 12 d,其平均病情指数增加到62.50,相对防效降低到28.57%(表 4)。
由图 4a可知,宁南霉素处理的本氏烟始终未见症状。在12 d时,通过Western Blot对各处理TuMV-GFP积累量进行检测,结果表明,芦苇提取物和宁南霉素处理的本氏烟中TuMV-GFP积累量显著低于无菌水处理(图 4b,4c)。
-
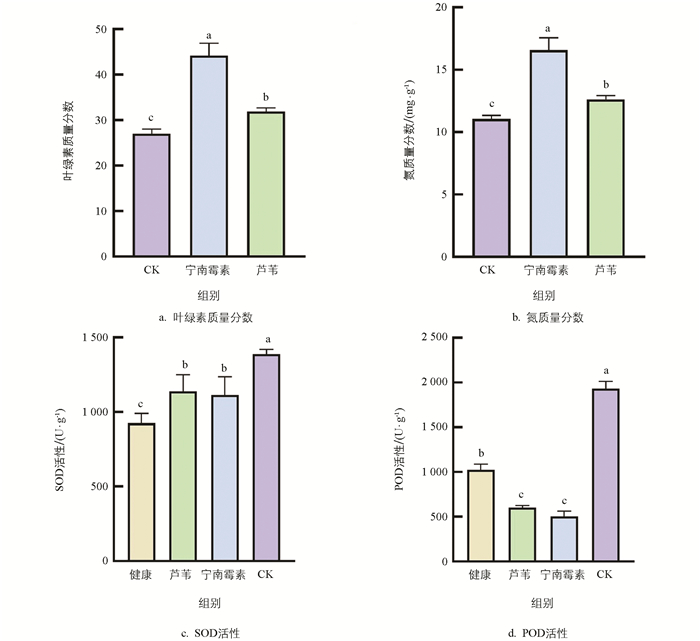
对接种TuMV-GFP 12 d的本氏烟叶绿素、氮含量及抗性相关酶SOD和POD活性进行检测,结果表明,芦苇提取物处理的本氏烟叶片的平均叶绿素质量分数(31.89)显著高于无菌水处理(27.01,p<0.05),显著低于宁南霉素处理(44.18,p<0.05,图 5a)。芦苇提取物处理的本氏烟叶片的平均氮质量分数(12.62 mg/g)也显著高于无菌水处理(11.06 mg/g,p<0.05),同时显著低于宁南霉素处理(16.59 mg/g,p<0.05),其变化趋势与叶绿素基本一致(图 5b)。芦苇提取物处理的本氏烟中SOD活性(1 138.85 U/g)较无菌水处理(1 389.76 U/g)显著降低(p<0.05),同时显著高于健康植株(925.77 U/g,p<0.05),与宁南霉素处理(1 113.75 U/g)相比,差异无统计学意义(图 5c)。芦苇提取物处理的本氏烟中POD活性(603.92 U/g)较无菌水处理(1 932.55 U/g)显著降低(p<0.05),同时显著低于健康植株(1 026.67 U/g,p<0.05),与宁南霉素处理(503.27 U/g)相比,差异无统计学意义(图 5d)。
2.1. 芦苇提取物对PVX的抑制作用
2.2. 芦苇提取物化学成分预试结果
2.3. 芦苇提取物对PVY的抑制作用
2.4. 接种PVYros后不同处理本氏烟中叶绿素、氮含量及抗性相关酶SOD和POD活性检测
2.5. 芦苇提取物对TuMV的抑制作用
2.6. 接种TuMV-GFP后不同处理本氏烟中叶绿素、氮含量及抗性相关酶SOD和POD活性检测
-
随着化学病毒抑制剂安全问题的逐渐显现,社会各界对具有低毒、高效、广谱等性质的植物源农药的关注也越来越多[21]。结构独特、环境友好的天然抗病毒物质已成为绿色农药开发领域的重要研究对象。植物中抗病毒活性物质含量丰富、种类繁多,其结构独特,且相互之间存在着极其复杂的互作关系,无论是用无机溶剂还是有机溶剂提取又或者是植物精油,都表现出对目标以外的生物毒副作用小、不会造成环境污染等优点[22],因此,植物界是发现低毒、低残留、高效及环境和谐的新抗病毒剂和新抗病毒化合物最好的自然资源宝库。从首次在商陆中发现能够有效抑制TMV活性的物质[23]以来,人们逐渐将注意力集中于从植物中寻找天然抗病毒的活性物质。20世纪80年代后,越来越多的人选择使用低残留、对人畜无害、对环境污染小的植物农药[24]。如植物源抗病毒剂VFB可以预防、治疗和钝化多种植物病毒,并且可以提高作物的抗病性、刺激其生长、提高产量[4]。杜春梅等[25]研究发现,在591种对真菌或细菌具有拮抗作用的植物源提取物中,有173种具有抗病毒活性,其中金钟柏提取物能够显著抑制西瓜花叶病毒(watermelon mosaic virus,WMV)的侵染,使WMV的CP表达量受到抑制[26]。有研究发现,WCT-Ⅱ不仅对TMV线粒体具有体外钝化作用,还能诱导植物产生病程相关蛋白,提高烟草抵抗TMV侵染的能力[27]。芦苇作为多年生禾草,全株都有药用作用,其提取物可在一定程度上抑制细菌和霉菌,并且具有明显的抗氧化作用[12]。芦苇中的活性物质可以抑制铜绿微囊藻细胞的增加[28]。芦苇丙酮粗提物可以在一定程度上抑制小麦赤霉病菌、番茄灰霉病菌和苹果炭疽病菌[29]。本研究发现芦苇提取物对PVX、PVY和TuMV的侵染均有一定的抑制作用。
本研究对接种PVYros和TuMV-GFP的本氏烟叶片中的叶绿素和氮含量进行了检测,结果表明,芦苇提取物处理的本氏烟在接种PVYros和TuMV-GFP后,其叶绿素和氮含量显著高于无菌水处理。植物叶片叶绿素含量和氮含量是衡量植物健康状况及其光合作用和生理代谢的重要指标,与植物抗病性密切相关[30-31]。氮是构成叶绿素的主要元素之一,氮含量直接影响光合作用的效率和光合产物的形成。植物叶片叶绿素和氮含量越高,通常表明植物的光合作用能力越强,生长发育越好,如丁香酚可通过促进叶绿素的合成,增强烟草体内抗性基因的转录[32]。有研究发现,百合无症病毒(lily symptomless virus,LSV)侵染可以抑制百合PSⅡ的光化学活性[33]。抗病毒化合物2005196可以诱导植株叶绿素含量的增加,提高植株的抗病性[34]。芦苇提取物在一定程度上提高了植株叶片的氮含量并保护植株叶绿体不被破坏,从而增强了植株对PVY和TuMV的抵抗能力。
SOD和POD在生物体内扮演着重要的角色,发挥着抗氧化和防御作用,帮助生物体应对各种内外部的压力和挑战,是植物抗病反应的重要指标。烟草喷施抗TMV的混配提取物后,其体内PPO、POD、PAL和SOD的活性均有不同程度的提高[10]。植物源病毒抑制剂VBF可提高烟草中SOD、CAT等细胞防御的酶活性,从而增强寄主植物的抗病性[4]。丁香酚能够激发烟草叶片中活性氧的产生,提高PAL、POD和SOD的活性,诱导系统获得抗性从而抗TMV[31]。本研究对接种PVYros和TuMV-GFP的本氏烟叶片中的抗性相关酶SOD和POD的活性进行了检测,发现芦苇提取物处理后接种PVYros和TuMV-GFP 12 d,本氏烟叶片中的SOD和POD活性显著低于无菌水处理,推测其可能与测定时间在病毒发病后期有关。有研究表明,植物抗病相关酶在植物体内的活性经不同处理诱导呈现出不同的变化趋势。林中正[8]研究发现商陆、银杏和栀子提取物复配与TMV混合接种烟草,其叶片内的POD活性变化趋势为先上升后下降,最高值在48 h时出现;只接种TMV时,POD活性变化趋势则为先下降后上升;对照在6~72 h内POD活性无明显变化。
此外,本研究还对芦苇提取物中化学成分进行了检测,初步检测到芦苇提取物中含有酚类、生物碱、黄酮、强心苷、有机酸。有研究表明,黄酮类化合物和多糖类化合物作为芦苇中的主要有效成分具有多种生理活性[35]。应用高效液相色谱法,戴军等[36]将9种黄酮类化合物从芦苇中成功分离出来。叶小齐等[37]利用GC-MS方法对芦苇正丁醇萃取物进行分析,发现糖类、醇类、有机酸类、酮类、酰胺类和脂类这些主要成分均可抑制小麦幼苗生长。赵小霞[38]从芦苇石油醚萃取物、乙酸乙酯萃取物和正丁醇萃取物中分离鉴定出了β-谷甾醇、对羟基苯甲醛、麦黄酮、麦黄酮7-O-β-吡喃葡萄糖苷和单棕榈酸甘油酯等化合物,这些化合物部分对血管紧张素Ⅰ转换酶具有抑制活性。从中药天仙子中发现的天仙子新碱能够激发植物自身产生免疫应答反应,具有良好的免疫诱抗活性并兼具植物生长调节功能[39]。这些成分多与抗病毒作用相关,从芦苇的化学成分中筛选具有抗病毒活性的物质,为植物源抗病毒制剂的开发与利用奠定了基础,但芦苇中的活性成分及其作用机理还有待进一步研究。
-
本研究以本氏烟为试验材料,分别接种PVX、PVYros和TuMV-GFP,在接种后观察发病情况并记录病情指数,检测PVX CP表达量和PVYros、TuMV-GFP积累量,并对接种PVYros和TuMV-GFP各处理下本氏烟的叶绿素、氮含量,抗性相关酶SOD和POD活性进行了检测,结果表明:1) 芦苇提取物对PVX、PVYros和TuMV-GFP的侵染均有一定的抑制作用。芦苇提取物处理本氏烟后,接种PVX、PVYros和TuMV-GFP的病情指数较无菌水处理均显著降低,且本氏烟中的PVX CP表达量、PVYros和TuMV-GFP的积累量均显著低于处理。2) 芦苇提取物处理本氏烟可使植株中叶绿素和氮含量升高。对接种PVYros和TuMV-GFP的本氏烟叶片中的叶绿素和氮含量进行检测,结果表明,芦苇提取物处理的本氏烟在接种PVYros和TuMV-GFP后,其叶片中叶绿素和氮含量显著高于无菌水处理。3) 芦苇提取物可诱导本氏烟中抗性相关酶的变化。对接种PVYros和TuMV-GFP的本氏烟叶片中的抗性相关酶SOD和POD的活性进行检测,发现芦苇提取物处理后接种PVYros和TuMV-GFP 12 d,本氏烟叶片中的SOD和POD活性显著低于无菌水处理。4) 对芦苇提取物中化学成分进行检测,初步检测到芦苇提取物中含有酚类、生物碱、黄酮、强心苷和有机酸。





 DownLoad:
DownLoad: