-
开放科学(资源服务)标识码(OSID):

-
番茄(Solanum lycopersicum)是茄科模式植物[1],中国目前番茄种植面积和产量均位居世界前列,已成为国际番茄贸易的主要力量[2]。近年来番茄病毒病的频发,已成为影响番茄产量和品质的重要因素,严重影响着番茄产业的健康发展。因此,明确中国不同番茄产区病毒病的病原种类,为早期精准诊断提供可靠依据,并根据其传播特点制定有效的防控策略至关重要。
病毒病侵染番茄后会导致植株矮化,叶片出现花叶、曲叶、黄化、坏死等症状。目前报道有22科39属312种病毒病的病原可以侵染番茄[3],在我国番茄上发生的病毒种类也高达44种[4],其中黄瓜花叶病毒(cucumber mosaic virus,CMV)[5-7]、南方番茄病毒(southern tomato virus,STV)[8-14]、番茄褪绿病毒(tomato chlorosis virus,ToCV)[15-23]、番茄花叶病毒(tomato mosaic virus,ToMV)[24]、番茄斑萎病毒(tomato spotted wilt virus,TSWV)[25-28]、番茄黄化曲叶病毒(tomato yellow leaf curl virus,TYLCV)[29-36]已在国内番茄产区普遍发生。此外,烟草丛顶病毒(tobacco bushy top virus,TBTV)、番茄斑驳花叶病毒(tomato mottle mosaic virus,ToMMV)、番茄褐色皱纹果病毒(tomato brown rugose fruit virus,ToBRFV)、新德里番茄曲叶病毒(tomato leaf curl New Delhi virus,ToLCNDV)近年来被首次报道后发展和传播迅速,且对番茄品质造成了严重影响,现已成为国内番茄重要病毒病的病原防控对象[37-40]。
内蒙古作为我国番茄主产区之一,设施番茄发展迅速,病毒病病原的威胁也日益严重。目前内蒙古番茄产区的病毒病病原种类及其分类地位尚不完全明确,已然成为番茄生产上的一大隐患。本研究于2021-2024年对内蒙古包头、巴彦淖尔、赤峰、鄂尔多斯、呼和浩特5个市辖番茄产区进行病毒病病原种类的调查和鉴定,对克隆到的病毒基因组序列运用MEGA-X、SDTv1.2等生物信息学分析软件对其进行核苷酸序列一致性分析、系统发育分析,旨在明确侵染内蒙古5个市辖番茄产区的主要病毒病病原种类、发生情况以及分类地位,为内蒙古番茄病毒的检测与防控提供数据支撑。
HTML
-
2021-2024年,在内蒙古包头、巴彦淖尔、赤峰、鄂尔多斯、呼和浩特5个市辖番茄产区共采集表现为斑驳、花叶、黄化、坏死等疑似病毒侵染的番茄叶片样品224份(2021年34份,2022年98份,2023年60份,2024年32份),经液氮速冻保存于-80 ℃冰箱中备用。
-
TaKaRa MiniBEST Plant RNA Extraction Kit、E.coli JM109感受态细胞,宝生物工程(大连)有限公司;Plant Genomic DNA Kit试剂盒、普通琼脂糖凝胶DNA回收试剂盒,天根生化科技(北京)有限公司;ABScript Ⅲ RT Master Mix for qPCR,武汉爱博泰克生物科技有限公司;M5超光速mix(无需提取基因组DNA)、M5 HiClear DL2000 DNA marker,北京聚合美生物科技有限公司;零背景pTOPO-TA/Blunt通用克隆试剂盒,北京艾德莱生物科技有限公司。
-
按照TaKaRa MiniBEST Plant RNA Extraction Kit、Plant Genomic DNA Kit试剂盒操作步骤分别提取番茄样品中的总RNA和DNA,经微量分光光度计检测浓度和纯度,琼脂糖凝胶电泳检测完整性,合格后保存于-80 ℃冰箱中备用。
-
对于RNA病毒,以提取番茄样品中的总RNA为模板,使用cDNA一链合成预混液ABScript Ⅲ RT Master Mix for qPCR进行反转录。反转录反应体系(20 μL):5× ABScript Ⅲ RT Master Mix(4.0 μL)、总RNA(1 000 ng)、Nuclease-free ddH2O补足至20 μL。混合均匀,瞬时离心,置于PCR仪55 ℃反应15 min、85 ℃反应5 min。反转录合成的cDNA保存于-20 ℃冰箱中备用。
对于DNA病毒,以提取番茄样品中的总DNA为模板,按浓度比例稀释至10~15 ng/μL,总DNA稀释液保存于-20 ℃冰箱中备用。
-
以反转录合成的cDNA和总DNA稀释液为模板,使用已报道的侵染番茄的病毒特异性检测引物(表 1)分别扩增目标片段。PCR反应体系(20 μL):2× M5超光速mix(10.0 μL)、10 μmol/L上游引物(1.0 μL)、10 μmol/L下游引物(1.0 μL)、cDNA或总DNA稀释液(2.0 μL)、Nuclease-free ddH2O补足至20 μL。PCR反应条件:95 ℃预变性3 min;94 ℃变性30 s,根据表 1的退火温度退火30 s,72 ℃延伸(1 000 bp/min),35个循环;72 ℃终延伸10 min;4 ℃保存。PCR扩增产物于1.0%琼脂糖凝胶电泳25 min,割取检测到病毒的目标片段,按照普通琼脂糖凝胶DNA回收试剂盒操作步骤纯化回收目标片段。
-
纯化的回收产物连接pTOPO-TA载体,连接产物转化E.coli JM109感受态细胞,涂板并37 ℃过夜培养,单菌落克隆经菌液PCR鉴定后,随机挑选3个阳性克隆菌液送至生工生物工程(上海)股份有限公司北京测序部进行Sanger测序。
-
通过NCBI GenBank数据库BLASTn程序的比对结果和国际病毒分类委员会(The International Committee on Taxonomy of Viruses,ICTV)的分类标准明确病毒种类。使用SDTv1.2软件中的Muscle序列比对程序对本研究获得的病毒分离物基因组序列以及NCBI GenBank数据库中下载的各病毒代表分离物基因组序列进行核苷酸序列一致性分析。利用MEGA-X软件中的最大似然法(Maximum likelihood,ML)对本研究所获得的各病毒分离物基因组序列以及NCBI GenBank数据库中下载的各病毒代表分离物基因组序列进行系统发育树的重建,其中MODLES程序确定建树参数,自展值设置为1 000。
1.1. 供试材料
1.1.1. 样品来源
1.1.2. 试剂
1.2. 试验方法
1.2.1. 总核酸提取
1.2.2. 反转录合成cDNA和总DNA稀释
1.2.3. RT-PCR、PCR扩增和琼脂糖凝胶电泳检测
1.2.4. 基因克隆和测序
1.2.5. 序列一致性分析和系统发育分析
-
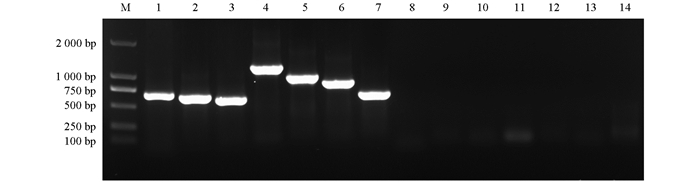
对番茄样品进行RT-PCR和PCR检测,结果显示,224份番茄样品中有67份检测出了病毒,检出率为29.91%(67/224),共检测到7种病毒,其中RNA病毒为AMV、CMV、STV、ToMMV、ToMV、TSWV,DNA病毒为TYLCV(图 1、表 2)。AMV总检出率为0.45%(1/224),番茄样品来源于2023年鄂尔多斯市准格尔旗,检出率为10.00%(1/10)。CMV总检出率为5.80%(13/224),番茄样品主要来源于2022年呼和浩特市玉泉区,检出率为13.70%(10/73)。STV总检出率为6.70%(15/224),样品主要来源于2021、2022年呼和浩特市玉泉区,检出率为9.35%(10/107)。ToMMV总检出率为10.71%(24/224),样品来源于2021、2022年呼和浩特市玉泉区,检出率为22.43%(24/107)。ToMV总检出率为20.54%(46/224),样品主要来源于2021、2022年呼和浩特市玉泉区,检出率为39.25%(42/107)。TSWV总检出率为1.79%(4/224),样品主要来源于2022年呼和浩特市玉泉区,检出率为4.11%(3/73)。TYLCV总检出率为2.68%(6/224),样品主要来源于2023、2024年包头市东河区,检出率为13.64%(3/22)。
-
67份检出病毒性病原的番茄样品中复合侵染现象较为普遍,总体复合侵染率为52.24%(35/67)。复合侵染类型共计12种(表 3),其中2种病毒复合侵染类型为CMV+STV(1.49%,1/67)、CMV+ToMV(2.99%,2/67)、CMV+TSWV(1.49%,1/67)、STV+TYLCV(2.99%,2/67)、STV+ToMV(10.45%,7/67)、ToMMV+ToMV(22.39%,15/67);3种病毒复合侵染类型为CMV+STV+ToMV(1.49%,1/67)、CMV+STV+TSWV(1.49%,1/67)、CMV+ToMMV+ToMV(2.99%,2/67)、CMV+ToMV+TSWV(1.49%,1/67)、STV+ToMMV+ToMV(1.49%,1/67);4种病毒复合侵染类型为CMV+STV+ToMMV+ToMV(1.49%,1/67)。
-
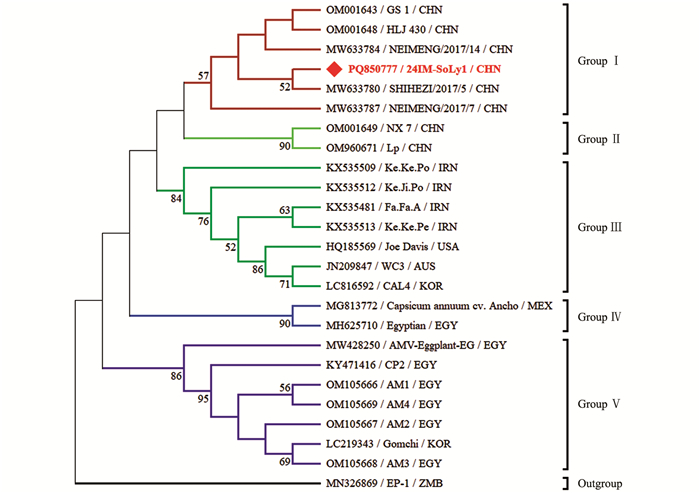
本研究获得的内蒙古番茄AMV分离物24IM-SoLy1(GenBank登录号:PQ850777)与23个AMV代表分离物核苷酸序列一致性为92.9%~99.1%。24IM-SoLy1与埃及马铃薯(Solanum tuberosum)AMV分离物CP2(KY471416)、埃及罗勒(Ocimum basilicum)AMV分离物Egyptian(MH625710)核苷酸序列一致性最低,为92.9%;与我国苜蓿(Medicago sativa)AMV分离物SHIHEZI/2017/5(MW633780)核苷酸序列一致性最高,为99.1%。
针对获得的内蒙古番茄AMV分离物的完整外壳蛋白(Coat protein,CP)基因核苷酸序列构建系统发育树,MODELS程序判定最佳进化模型为K2+G。结果表明,基于24个AMV分离物CP基因所重建的系统发育树可分为5个分支,其中24IM-SoLy1与我国苜蓿AMV分离物SHIHEZI/2017/5位于同一分支上,亲缘关系最近,被分在Group Ⅰ(图 2)。
-
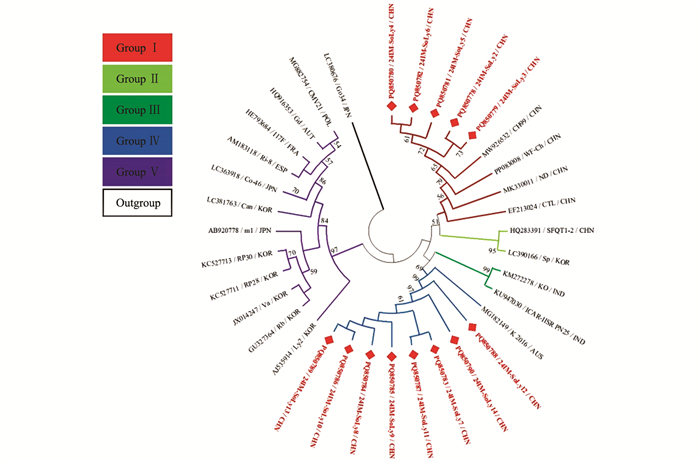
本研究获得的内蒙古番茄CMV分离物24IM-SoLy2~24IM-SoLy14(GenBank登录号:PQ850778~PQ850790)核苷酸序列一致性为92.8%~99.8%,与21个CMV代表分离物核苷酸序列一致性为89.8%~99.2%。24IMSoLy6(PQ850782)与日本烟草(Nicotiana tabacum)CMV分离物m1(AB920778)、韩国二色金光菊(Rudbeckia hirta)CMV分离物Rb(GU327364)核苷酸序列一致性最低,为89.8%,24IM-SoLy2(PQ850778)、24IM-SoLy5(PQ850781)与我国甜瓜(Cucumis melo)CMV分离物CH99(MW926532)核苷酸序列一致性最高,为99.2%。
针对获得的内蒙古番茄CMV分离物的部分RNA依赖RNA聚合酶(RNA-dependent RNA polymerase,RdRp)基因核苷酸序列构建系统发育树,MODELS程序判定最佳进化模型为K2+G。结果表明,基于34个CMV分离物部分RdRp基因所重建的系统发育树可分为5个分支,其中24IM-SoLy2~24IM-SoLy6与我国甜瓜CMV分离物CH99(MW926532)位于同一小分支上,亲缘关系最近,被分在Group Ⅰ;24IM-SoLy7(PQ850783)~24IM-SoLy14(PQ850790)与澳大利亚番茄CMV分离物K 2016(MG182149)位于同一小分支上,亲缘关系最近,被分在Group Ⅳ(图 3)。
-
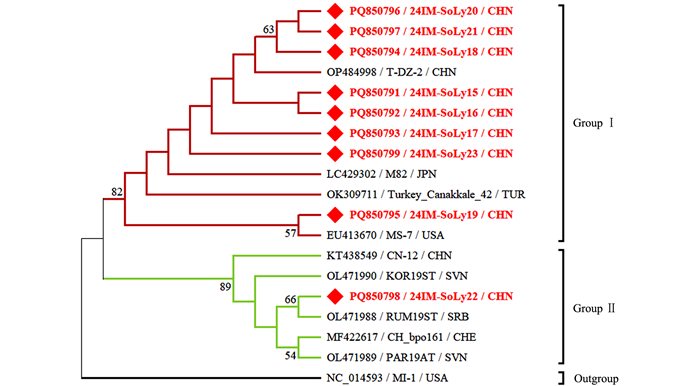
本研究获得的内蒙古番茄STV分离物24IM-SoLy15~24IM-SoLy23(GenBank登录号:PQ850791~PQ850799)核苷酸序列一致性为97.8%~99.8%,与9个STV代表分离物核苷酸序列一致性为97.9%~99.8%。24IM-SoLy22(PQ850798)与土耳其番茄STV分离物Turkey_Canakkale_42(OK309711)核苷酸序列一致性最低,为97.9%;24IM-SoLy15(PQ850791)与美国番茄STV分离物MS-7(EU413670)、日本番茄STV分离物M82(LC429302)、海南省儋州市番茄STV分离物T-DZ-2(OP484998)核苷酸序列一致性最高,为99.8%。
针对获得的内蒙古番茄STV分离物的部分融合蛋白(Fusion protein,FP) p122基因核苷酸序列构建系统发育树,MODELS程序判定最佳进化模型为HYK+I。结果表明,基于18个STV分离物部分FP p122基因所构建的系统发育树可分为2个分支,其中24IM-SoLy15(PQ850791)~24IM-SoLy17(PQ850793)、24IM-SoLy23(PQ850799)被分在Group Ⅰ;24IM-SoLy18(PQ850794)、24IM-SoLy20(PQ850796)、24IM-SoLy21(PQ850797)与海南省儋州市番茄分离物T-DZ-2位于同一小分支上,亲缘关系最近,也被分在Group Ⅰ;24IM-SoLy19与美国番茄STV分离物MS-7(EU413670)位于同一小分支上,亲缘关系最近,同样被分在Group Ⅰ。24IM-SoLy22与塞尔维亚番茄STV分离物RUM19ST(OL471988)位于同一小分支上,亲缘关系最近,被分在Group Ⅱ(图 4)。
-
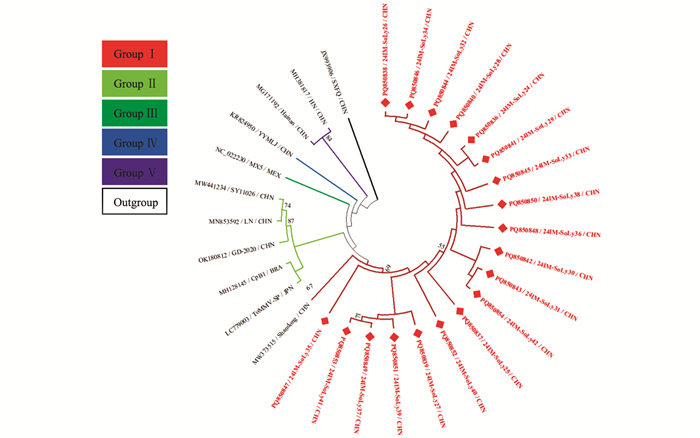
本研究获得的内蒙古番茄ToMMV分离物24IM-SoLy24~24IM-SoLy42(GenBank登录号:PQ850836~PQ850854)核苷酸序列一致性为98.4%~99.9%,与10个ToMMV代表分离物核苷酸序列一致性为97.6%~99.9%。24IM-SoLy37(PQ850849)与日本辣椒ToMMV分离物ToMMV-SP(LC779003)核苷酸序列一致性最低,为97.6%;24IM-SoLy27(PQ850839)与山东省番茄ToMMV分离物Shandong(MW373515)核苷酸序列一致性最高,为99.9%。
针对获得的内蒙古番茄ToMMV分离物的部分RdRp、运动蛋白(Movement protein,MP)基因核苷酸序列构建系统发育树,MODELS程序判定最佳进化模型为TN93。结果表明,基于29个ToMMV分离物部分RdRp、MP基因所重建的系统发育树可分为5个分支,其中24IM-SoLy24~24IM-SoLy42与山东省番茄ToMMV分离物Shandong(MW373515)位于同一分支上,亲缘关系最近,被分在Group Ⅰ(图 5)。
-
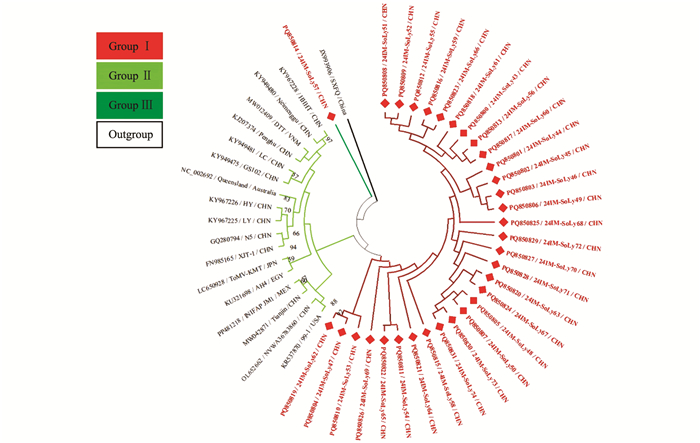
本研究获得的内蒙古番茄ToMV分离物24IM-SoLy43~24IM-SoLy74(GenBank登录号:PQ850800~PQ850831) 核苷酸序列一致性为98.8%~99.9%,与17个ToMV代表分离物核苷酸序列一致性为98.4%~99.7%。24IM-SoLy64(PQ850821)、24IM-SoLy74(PQ850831)与呼和浩特市番茄ToMV分离物HHHT(KY967228)、天津市番茄ToMV分离物Tianjin(MW042871)、墨西哥番茄ToMV分离物INIFAP JM1(PP481218)核苷酸序列一致性最低,为98.4%;24IM-SoLy57(PQ850814)与澎湖县番茄ToMV分离物Penghu(KJ207374)、澳大利亚番茄ToMV分离物Queensland(NC_002692)核苷酸序列一致性最高,为99.7%。
针对获得的内蒙古番茄ToMV分离物的部分RdRp基因核苷酸序列构建系统发育树,MODELS程序判定最佳进化模型为T92+G。结果表明,基于49个ToMV分离物部分RdRp基因所重建的系统发育树可分为3个分支,其中24IM-SoLy43(PQ850800)~24IM-SoLy56(PQ850813)、24IM-SoLy58(PQ850815)~24IM-SoLy74(PQ850831)位于同一分支上,被分在Group Ⅰ;24IM-SoLy57(PQ850814)单独构成Group Ⅲ(图 6)。
-
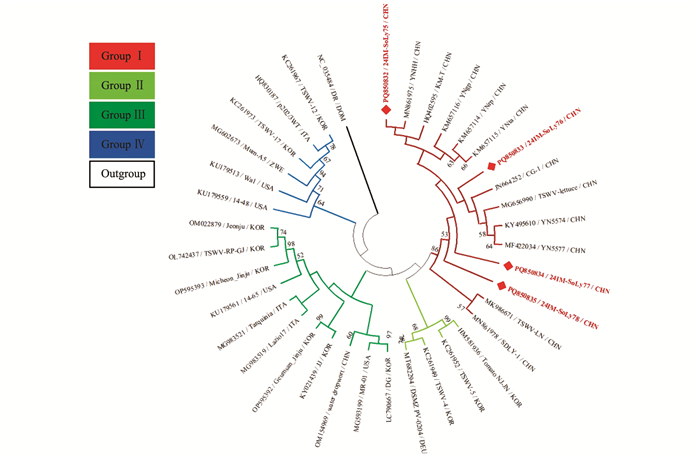
本研究获得的内蒙古番茄TSWV分离物24IM-SoLy75~24IM-SoLy78(GenBank登录号:PQ850832~PQ850835)核苷酸序列一致性为99.2%~99.7%,与32个TSWV代表分离物核苷酸序列一致性为97.0%~99.9%。24IM-SoLy75(PQ850832)与意大利辣椒(Capsicum annuum)TSWV分离物p202/3WT(HQ830187)、津巴布韦野菊(Chrysanthemum indicum)TSWV分离物Mum-A5(MG602673)核苷酸序列一致性最低,为97.0%;24IM-SoLy78(PQ850835)与我国番茄TSWV分离物KM-T(HQ402595)核苷酸序列一致性最高,为99.9%。
针对获得的内蒙古番茄TSWV分离物的部分核衣壳蛋白(Nucleocapsid protein,N)基因核苷酸序列构建系统发育树,MODELS程序判定最佳进化模型为T92+I。结果表明,基于36个TSWV分离物部分N基因所重建的系统发育树可分为4个分支,其中24IM-SoLy75(PQ850832)与我国烟草TSWV分离物YNHH(MN861975)位于同一小分支上,亲缘关系最近,被分在Group Ⅰ;24IM-SoLy76(PQ850833)与我国莴苣(Lactuca sativa)TSWV分离物CG-1(JN664252)、TSWV-lettuce(MG656990)、党参(Codonopsis pilosula) TSWV分离物YN5574(KY495610)、旱金莲(Tropaeolum majus)TSWV分离物YN5577(MF422034) 位于同一小分支上,亲缘关系较近,被分在Group Ⅰ;24IM-SoLy77(PQ850834)、24IM-SoLy78也被分在Group Ⅰ(图 7)。
-
本研究获得的内蒙古番茄TYLCV分离物24IM-SoLy79~24IM-SoLy82(GenBank登录号:PQ850773~PQ850776)核苷酸序列一致性为99.4%~99.8%,与19个TYLCV代表分离物核苷酸序列一致性为96.6%~99.8%。24IM-SoLy79与格林纳达番茄TYLCV分离物Grenada:Hermitage:2007(FR851297)核苷酸序列一致性最低,为96.6%;24IM-SoLy80(PQ850774)与广东省广州市番茄TYLCV分离物Bns71(PP438342)核苷酸序列一致性最高,为99.8%。
针对获得的内蒙古番茄TYLCV分离物的部分CP基因核苷酸序列构建系统发育树,MODELS程序判定最佳进化模型为K2+G。结果表明,基于23个TYLCV分离物部分CP基因所构建的系统发育树可分为2个分支,其中24IM-SoLy79(PQ850773)~24IM-SoLy82(PQ850776)与广州市番茄分离物Bns71(PP438342)位于同一小分支上,亲缘关系最近,被分在Group Ⅰ(图 8)。
2.1. 侵染番茄的病毒种类检测与鉴定
2.2. 复合侵染类型
2.3. 基因组序列分析
2.3.1. AMV的基因组序列分析
2.3.2. CMV的基因组序列分析
2.3.3. STV的基因组序列分析
2.3.4. ToMMV的基因组序列分析
2.3.5. ToMV分离物基因组序列分析
2.3.6. TSWV的基因组序列分析
2.3.7. TYLCV的基因组序列分析
-
在我国不同番茄产区病毒病的病原种类分布及其流行趋势均有差异,在新疆地区番茄上,检测到STV、TYLCV、ToCV[22];在云南地区番茄上,主要发生的病毒有番茄环纹斑点病毒(TZSV)、辣椒脉斑驳病毒(ChiVMV)、STV[13]。2022年宁夏地区番茄主要受到TYLCV、ToCV、STV、TSWV 4种病毒的侵染[23];2024年,ToMMV、TSWV、STV为主要发生的病毒,其中ToMMV为当地优势毒源[14],因此宁夏地区番茄病毒病的病原种类呈动态变化趋势。2021-2024年,本研究运用RT-PCR、PCR技术对内蒙古包头、巴彦淖尔、赤峰、鄂尔多斯、呼和浩特5个市辖番茄产区开展番茄病毒病病原种类的调查和鉴定,检测了25种RNA病毒、2种DNA病毒,其中鉴定到AMV、CMV、STV、ToMMV、ToMV、TSWV、TYLCV等7种病毒,检测结果也表明5个市辖番茄产区中复合侵染现象普遍存在。2021年,呼和浩特地区番茄上检测到STV、ToMMV、ToMV,2022年在该地区番茄上又检测到CMV、TSWV;2023年,包头地区番茄上检测到TYLCV(次年检测又发现了STV)、鄂尔多斯地区检测到AMV。由此可见,内蒙古番茄产区病毒病病原种类的动态变化与国内其他地区存在差异,可能与当地气候干燥,蚜虫、蓟马等传毒媒介的种群优势相关。内蒙古地区干旱、少雨的气候利于蚜虫、蓟马等传毒媒介季节性暴发,可通过在设施温室通风口安装40~60目防虫网,并在温室内悬挂黄、蓝色板诱杀传毒媒介。
AMV为雀麦花叶病毒科(Bromoviridae)苜蓿花叶病毒属(Alfamovirus)的成员,截至2025年,本研究是继西班牙[55]、塞尔维亚、伊朗、埃及[56]后在第5个国家首次发现该病毒对于番茄的危害,该植株果实变褐,严重影响番茄的品质,考虑到调查样品采自于当地番茄种植户,生产上是否流行有待进一步研究。在我国AMV种群中,不同省份、生物气候区的AMV分离物在核苷酸序列水平上存在显著差异[57]。内蒙古是我国苜蓿的主要生产地之一,本研究获得的内蒙古番茄AMV分离物24IM-SoLy1与内蒙古苜蓿分离物NEIMENG/2017/14(NW633784)核苷酸序列一致性较高,且基于CP基因构建的系统发育树也表明其亲缘关系较近。因此,番茄生产上或需加强对AMV的监测预警。
CMV为雀麦花叶病毒科黄瓜花叶病毒属(Cucumovirus)的成员,是已知的寄主范围最多、分布最广的植物病毒之一,主要通过蚜虫以非持久性的方式传播[58]。温智浩等[7]鉴定发现银川、徐州市采集的番茄样品中存在CMV+TSWV复合侵染,而赤峰市采集的番茄样品中存在CMV+ToMV复合侵染,但未检测到TSWV。本研究在2022年呼和浩特市玉泉区采集的番茄样品中也发现了这两种复合侵染类型。TSWV属于番茄斑萎病毒科(Tospovirus)正番茄斑萎病毒属(Orthotospovirus),主要由西花蓟马传毒[23],是世界10大严重危害性植物病毒之一[59],杨菲等[25]证实TSWV已在内蒙古赤峰地区发生。本研究在2024年赤峰市元宝山区采集的番茄样品中未检测到TSWV,而在2022年呼和浩特市玉泉区、赛罕区采集的番茄样品中鉴定到TSWV,且玉泉区采集的番茄样品中发现CMV+ToMV+TSWV复合侵染类型。
STV为混合病毒科(Amalgaviridae)混合病毒属(Amalgavirus)的成员,经常与其他病毒复合侵染番茄,除种子、花粉传毒外,尚未发现其他传播途径[12],Xu等[60]研究认为STV已成为我国番茄上流行的第4大病毒。先后有研究者鉴定发现CMV+STV、STV+ToMV、CMV+STV+ToMV、STV+ToMMV+ToMV等复合侵染类型[5, 14],本研究在2021、2022年呼和浩特市玉泉区、2024年巴彦淖尔市临河区采集的番茄样品中发现有STV+ToMV复合侵染;2022年呼和浩特市新城区采集的番茄样品中发现CMV+STV、玉泉区采集的番茄样品中发现STV+ToMMV+ToMV复合侵染;2022年玉泉区采集的番茄样品中还存在CMV+STV+TSWV、CMV+STV+ToMMV+ToMV两种复合侵染;2024年包头市东河区、赤峰市元宝山区采集的番茄样品存在STV+TYLCV复合侵染,本研究未检测到STV单独侵染番茄的样品,因此STV在内蒙古5个市辖番茄产区田间单独侵染的症状还无法描述。
ToMMV、ToMV为帚状病毒科(Virgaviridae)烟草花叶病毒属(Tobamovirus)的成员。ToMMV可通过种子、土壤、机械传播,比ToMV的寄主范围更广,侵染性更强[61]。2021、2022年呼和浩特市玉泉区采集的番茄样品中均鉴定到ToMMV、ToMV,且2022年呼和浩特市新城区采集的番茄样品中也鉴定到了ToMV。呼和浩特市ToMMV检出率为18.18%(24/132),ToMV检出率为32.58%(43/132),由此可见ToMV是侵染呼和浩特市设施番茄的优势病毒,ToMMV+ToMV(22.39%,15/67)为优势复合侵染类型。
TYLCV为双生病毒科(Geminiviridae)菜豆金色花叶病毒属(Begomovirus)的成员,主要通过传毒媒介烟粉虱以持久性的方式传播,一旦获毒终身传毒[33]。2024年包头市东河区、赤峰市元宝山区采集的番茄样品中存在STV+TYLCV复合侵染。目前关于复合侵染对TYLCV传播影响的研究较少,罗瑞雪等[62]研究发现,与取食TYLCV单独侵染的番茄植株相比,取食ToCV+TYLCV复合侵染番茄植株的烟粉虱对TYLCV的传毒率更高,且番茄植株、烟粉虱中的病毒积累量也显著提高。刘晨等[63]为明确陕西省番茄产区TYLCV侵染的寄主范围,对产区周边作物、杂草进行检测,鉴定到黄瓜(Cucumis sativus)、辣椒、茄子(Solanum melongena)等中间寄主,病毒越冬宿主清除难度大。本研究在2023年包头市东河区一家番茄种植区周边的曼陀罗上检测到了TYLCV,次年该产区未种植番茄,但仍在该地区的曼陀罗上检测到TYLCV,故TYLCV可能在曼陀罗上传种,因此,生产中应将其作为重点监测和防控的对象,以免TYLCV逐年传播。
本研究运用RT-PCR、PCR技术鉴定了危害内蒙古5个市辖番茄产区的6种RNA病毒和1种DNA病毒,明确了内蒙古5个市辖番茄产区病毒病的病原种类及其发生情况,分析了7种病毒82个内蒙古分离物与各病毒代表分离物之间的亲缘关系,为内蒙古番茄病毒病的监测预警提供了理论支撑,并为我国番茄产区病毒病的传播路径、制定防控策略研究提供了理论基础。






 DownLoad:
DownLoad: