-
开放科学(资源服务)标识码(OSID):

-
鲟鱼隶属于硬骨鱼纲(Osteichthyes)、鲟形目(Acipenseriformes)、鲟科(Acipenseridae)、鲟属(Acipenser),是地球上现存最古老的鱼类之一,其鱼卵制成的鱼子酱享有“黑色黄金”的美誉[1-3]。鲟鱼个体庞大,生长迅速,肉质优良,鲟鱼皮既可食用也可制作成优质皮革,软骨可提炼硫酸软骨素,具有极高的经济价值[4-5]。据《2024中国渔业统计年鉴》数据统计显示,2023年我国鲟鱼产量达到14.94万t,创历史最高生产量[6]。在全球鲟鱼养殖国家中,我国产量已位居榜首,且呈现逐年递增趋势。大力发展鲟鱼绿色养殖产业,在创新冷水鱼养殖模式、引领和助推乡村振兴中起到带头作用。
目前鲟鱼养殖模式主要有流水养殖、微流水养殖、工厂化养殖等几种,其中流水养殖充分利用天然流水资源,具有集约化程度高、便于管理等优势,成为鲟鱼养殖的主要方式[2]。但该模式在养殖过程中存在较高频率的水体交换,直接或者间接影响鱼类的生存环境、免疫功能和疾病发生。近年来,由于鲟鱼养殖产业设施化、规模化和集约化程度不断提升,养殖密度加大,致使鲟鱼养殖过程中疾病频发,其中细菌性疾病是造成生产上鲟鱼暴发性死亡的主要原因,造成巨大经济损失的同时还严重阻碍了鲟鱼产业的绿色健康可持续发展[7]。其中肠杆菌科(Enterobacteriaceae)[8-10]及弧菌科(Vibrionaceae)[11-12]已有鲟鱼感染致病的案例。同样在水体和沉积物中,微生物也是水域生态系统的重要组成部分,其微生物群落组成与水质状况关系紧密[13-14],鲟鱼体表也有一定的微生物集中,由体表黏液中的共生细菌和机会性细菌种群组成[15],可直接影响鱼体健康,是鱼体天然免疫的重要组成部分[16-18]。体表菌群对鱼类健康的敏感性表明,菌群也可以作为鱼类的微生物标记物,用于评估养殖鱼类的质量[13, 19]。当前,关于鲟鱼体表微生物群落结构的季节性变化研究尚显匮乏[20-21],因此,认识水体、沉积物和水产动物体表中微生物的结构组成,有助于掌握养殖水域生态规律,为构建鱼类健康养殖防控体系提供理论依据。
本研究采集不同季节养殖环境及鱼体样本,基于高通量测序技术解析养殖鲟鱼多生境(体表、水体及沉积物)微生物组的结构特征与多样性分布,探究其与养殖环境理化因子的互作机制;对养殖过程中因环境改变而引发的机会致病菌进行季节性研究,以期阐明流水养殖鲟鱼菌群周年变化规律,找寻影响菌群结构的关键因子,分析环境因子对环境菌群的调控作用,为不同季节鲟鱼健康养殖及养殖环境调控、不同环境下鲟鱼体表微生物生理学提供参考。
HTML
-
单个养殖池长24 m,宽4.5 m,水深1.5 m,养殖池内水体平均每3 h交换一次。2022年1月,每个池内投入6 000尾西杂鲟(西伯利亚鲟Acipenser baerii♀×施氏鲟A.schrenckii♂)鱼苗,每尾鱼全长为(39.44±0.49) cm,质量为(176.54±6.76) g。试验用鱼购于重庆市彭水某鲟养殖基地,试验期间以3%左右的日粮水平进行投喂。
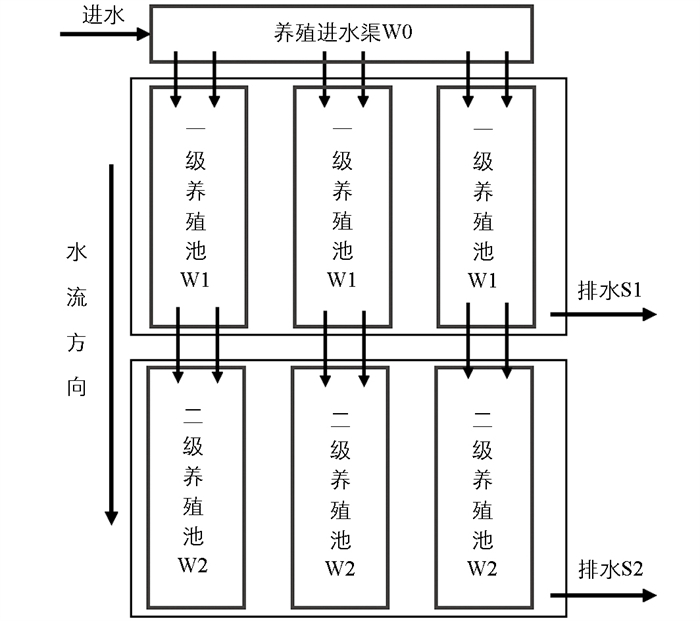
分别于2022年2月、5月、8月和11月对水体、沉积物与鲟体表面菌群进行采样。按水流方向设置进水渠、一级养殖池、二级养殖池,每个池塘设3个平行养殖池(图 1)。利用采水器采集水体中下层水样,纱布滤除水体中较大的颗粒性杂质后分别获得水体样本W0、W1、W2;采集一级养殖池底管道出水(排水S1)与二级养殖池底管道出水(排水S2),使用5 μm孔径的滤膜将不可溶解的颗粒杂质滤去后沉积物样本。用装有0.22 μm微孔滤膜的真空抽滤装置对水体及沉积物样本进行抽滤,取出滤膜置于灭菌离心管中,每组样本3个平行,-80 ℃保存待测。体表样本的采集取每级养殖池3个平行位点鲟鱼各3尾,经麻醉后,在无菌状态下用0.9%的灭菌生理盐水反复冲洗鲟鱼体表,收集生理盐水,用装有0.22 μm微孔滤膜的真空抽滤装置进行抽滤,取出滤膜于灭菌离心管中(F1)。取一根无菌拭子,从鲟鱼头背部开始向后翻滚,分别擦拭背部、侧面、腹部,重复以上步骤3次,每次取完分别放入离心管中(F2),采集完样品均于-80 ℃保存备测。
-
水质测定方法见表 1。
-
根据DNA提取试剂盒(FastDNA©SPIN Kit)(MP Biomedicals,美国)说明书进行总DNA抽提,DNA浓度和纯度利用NanoDrop 2000进行检测。利用1%琼脂糖凝胶电泳检测DNA的提取质量;采用341F(3′-CCTAYGGGRBGCASCAG-3′)和806R(5′-GGACTACNNGGGTATCTAAT-3′)引物对V3~V4片段进行PCR扩增,产物经回收、纯化后进行处理,应用Illumina MiSeq平台完成高通量测序。
-
对测序所得原始序列进行拼接、过滤,得到有效序列,然后基于有效数据进行分类单元(operational taxonomic unit,OTUs)聚类和物种分类分析,利用Mothur软件计算Alpha多样性指数;使用IBM SPSS Statistics 25进行正态分布检验、单因素方差分析和单变量一般线性模型拟合。为避免样品间测序深度的影响,采用phyloseq对OTU进行抽平处理,采用冗余分析(redundancy analysis,RDA)探究环境因子与水体、体表微生物群落组成变化的关联性,并通过蒙特卡罗检验法对分析结果的统计学显著性进行验证。
1.1. 试验材料及样品采集
1.2. 水质指标测定
1.3. 基因组DNA提取及测序文库构建
1.4. 数据处理及生物信息学分析
-
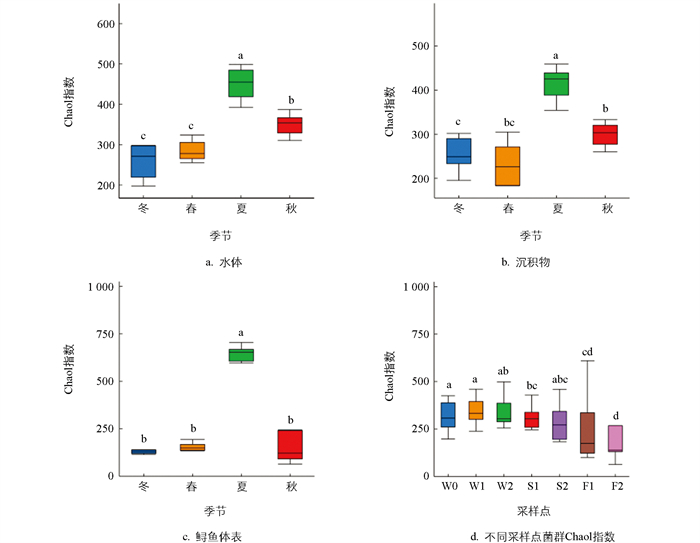
本研究共采集到水体样品共36个、沉积物样品共24个、鲟鱼体表样品共24个。水体样品测序共获得3 442 426对Reads,每个样品平均产生95 251条Clean Reads,共得到21门、34纲、80目、163科、333属、403种微生物。沉积物样品测序共获得2 265 521对Reads,每个样品平均产生94 040条Clean Reads,共得到20门、37纲、86目、164科、337属、401种细菌。鲟鱼体表样品测序共获得3 314 936对Reads,每个样品平均产生137 690条Clean Reads,共得到21门、38纲、94目、191科、368属、441种细菌。基于测序数据,对微生物群落进行Alpha和Beta多样性分析。Chao1指数分析结果显示(图 2),水体及沉积物菌群在不同季节具有显著差异(p<0.05),采样点对沉积物细菌群落存在显著的影响。春、秋、冬季之间鲟鱼体表菌群无显著差异,夏季与其他季节之间均呈现显著性差异。采样点因素进行单因素方差分析结果表明,Chao1指数在养殖池之间存在差异性。
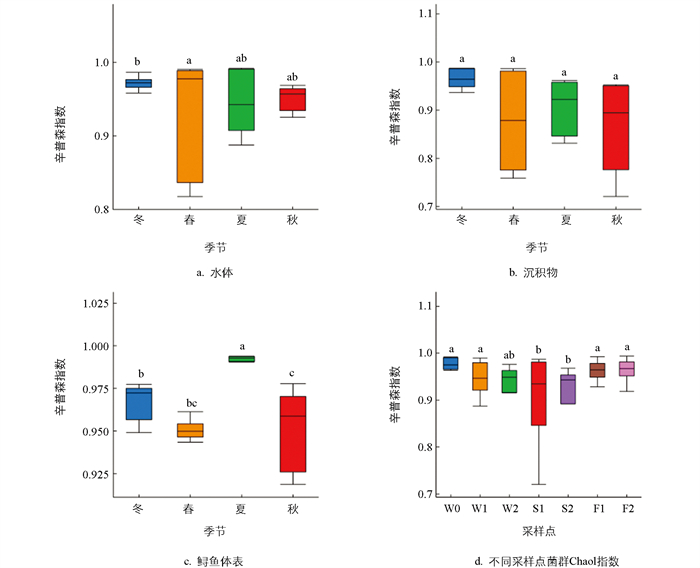
Simpson指数分析显示,不同季节和采样点对水体菌群结构丰富度和均匀度具有交互作用,其变化是由二者共同作用的结果;而沉积物和鲟鱼体表菌群丰富度和均匀度主要受季节性变化影响,但不同季节沉积物菌群间无显著性差异;不同采样点在总体水平上存在显著性影响(p<0.05)(图 3)。
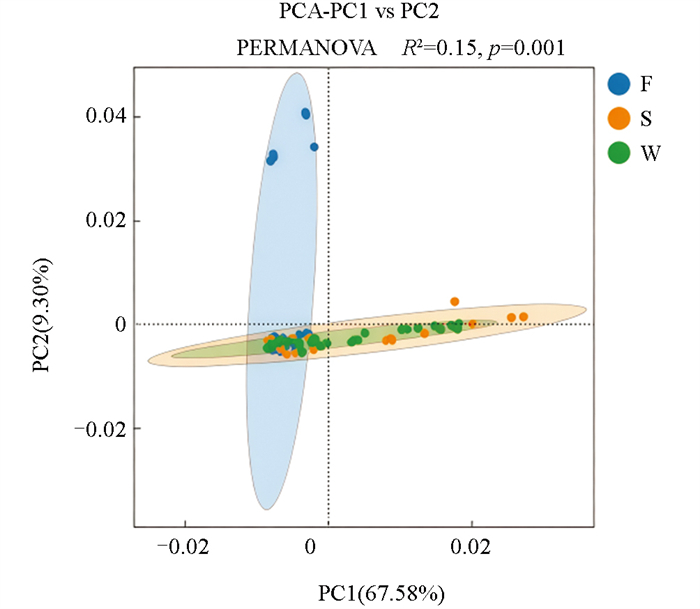
分别对水体(W)、沉积物(S)和鲟鱼体表(F)来源样品进行主成分分析。PCA分析结果显示水体菌群与沉积物菌群重叠,鲟鱼体表菌群与其部分重叠,说明鲟鱼养殖池塘水体菌群主要来源于沉积物菌群,而鲟鱼体表菌群仅有小部分来源于水环境,大部分均是由自身生长活动形成的(图 4)。同时,对不同样本进行permanova检验,PC1和PC2对样品的贡献率分别为67.58%和9.30%,利用PCA分析可以将样品中有效细菌和其他具有相似性的细菌区分开(R2=0.15,p<0.01)。对各样本间添加95%置信椭圆显示,水体菌群样本被沉积物样本包含在内,说明水体菌群与沉积物菌群相似度较高;鲟鱼体表样本与水体和沉积物样本存在交叉关系,但仍有部分细菌在PC2上距离水体和沉积物菌群较远,即鲟鱼体表菌群具有特殊性,部分菌群来源于水体环境,部分菌群来源于自身的生长繁殖。
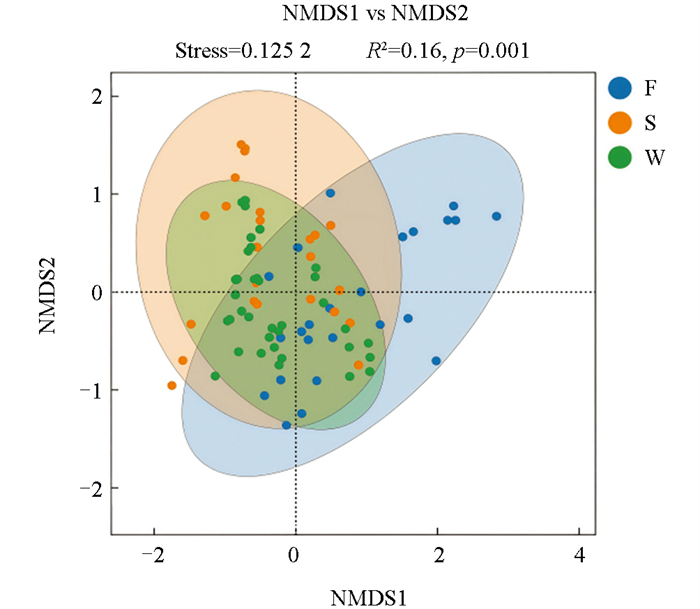
同样对水体、沉积物和鲟鱼体表样OTU进行基因系统发育树的weighted unifrac非度量多维标定法分析(Non-MetricMulti-Dimensional Scaling,NMDS),结果显示permanova检验R2=0.16、p<0.01,stress=0.125 2,NMDS分析对水体、沉积物和鲟鱼体表细菌同样具有一定的区分度。与PCA分析结果类似,沉积物细菌样本包含水体细菌样本,而鲟鱼体表细菌样本与水体和沉积物细菌样本存在较大部分的重叠,说明鲟鱼体表菌群很大程度来源于环境菌群(图 5)。
-
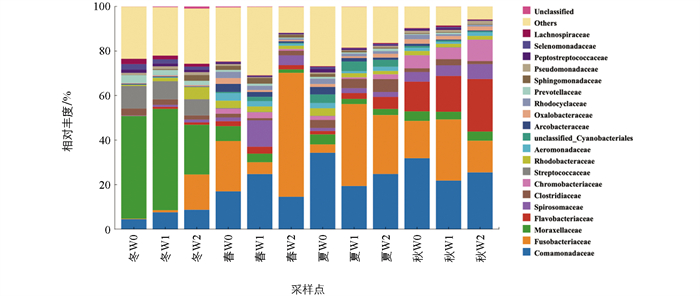
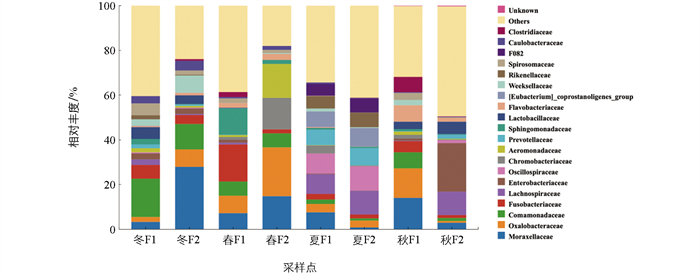
水体中冬季优势菌科为隶属于变形菌门(Proteobacteria)的莫拉氏菌科(Moraxellaceae,37.73%)及厚壁菌门(Firmicutes)的链球菌科(Streptococcaceae,8.55%)。各采样点相比,莫拉氏菌科随水流方向相对丰度呈下降趋势(W0:46.11%;W2:22.34%)。春季水体中优势菌科是梭杆菌门(Fusobacteria)的梭杆菌科(Fusobacteriaceae,16.93%)及变形菌门的丛毛单胞菌科(Comamonadaceae,19.04%)。作为冬季第一优势菌群的莫拉氏菌科在春季相对丰度显著低于冬季(p<0.01)。变形菌门的螺状菌科(Spirosomaceae)也在采样点中表现出较高的相对丰度。常被认为是潜在致病菌的气单胞菌科(Aeromonadaceae,2.24%)成为优势菌科。夏季优势菌科为丛毛单胞菌科(26.12%)及梭杆菌科,总体上,进水渠与养殖池塘中丛毛单胞菌科相对丰度呈现下降趋势。将其相对丰度进行对比,发现W1、W2水体中梭杆菌科相对丰度显著高于W0(p<0.01),说明养殖活动对其有正面的影响。莫拉氏菌科相对丰度持续出现下降,说明温度升高可能对其生长繁殖产生抑制作用。与春季相比,气单胞菌科仍属于夏季的优势菌群,对鲟鱼生长具有潜在威胁。秋季优势菌科为丛毛单胞菌科(26.35%)及梭杆菌科(19.53%)。与春夏季节相似,秋季水体气单胞菌科同样表现出较高的相对丰度,可达到1.32%(图 6)。
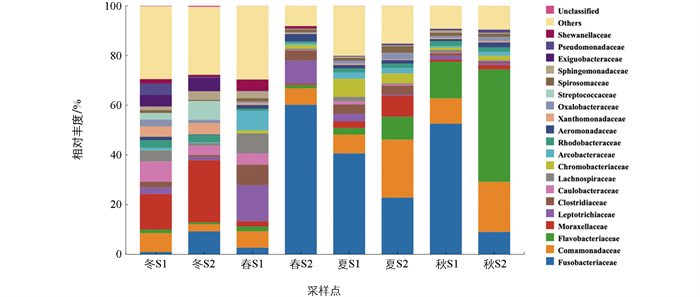
沉积物菌群优势菌科与水体菌群菌科大致相似,冬季优势菌科为莫拉氏菌科(17.99%)、柄杆菌科(Caulobacteraceae)和丛毛单胞菌科。春季优势菌种为梭杆菌科(31.40%)、纤毛菌科(Leptotrichiaceae,11.92%)。W2中梭杆菌科相对丰度高达60.14%,高于对应养殖池塘水体中梭杆菌科相对丰度,说明沉积物中更适合其生长。与水体相同,春季沉积物中同样检测出气单胞菌科(2.24%)的细菌,而且与水体中气单胞菌科不同;与W1相比,沉积物中气单胞菌相对丰度在W2(2.95%)中表现出升高,说明沉积物中气单胞菌科细菌生长繁殖更为迅速。夏季优势菌科为梭杆菌科(31.80%)、丛毛单胞菌科(15.46%),与夏季水体优势菌群变化趋势相同,黄杆菌科(Flavobacteriaceae)在养殖池塘内呈上升趋势,说明该菌适应养殖活动而进行生长繁殖,而丛毛单胞菌科相对丰度变化趋势与水体优势菌群相反。秋季优势菌科为梭杆菌科(30.57%),黄杆菌科(45.38%)是W2中的第一优势菌科,在沉积物中的变化趋势与春夏季节相同(图 7),说明黄杆菌科适合在较高营养盐浓度的沉积物中生活,且秋季环境下适合黄杆菌科生长繁殖。秋季气单胞菌科(1.42%)细菌相对丰度上升至第五优势菌科,气单胞菌在养殖池塘内表现为上升趋势,即秋季高温季节沉积物中气单胞菌科细菌易出现大量繁殖。
鲟鱼体表菌群优势菌科在不同季节差异较大,冬季优势菌科为丛毛单胞菌科(14.90%)和莫拉氏菌科(12.88%),与水体不同,鲟鱼体表莫拉氏菌科细菌呈上升趋势,可能是由于水体中细菌附着导致。威克斯氏菌科(Weeksellaceae,5.48%)隶属于拟杆菌门(Bacteroidetes),位于鲟鱼体表优势菌科第3位,该菌在沉积物前二十菌科中未出现,说明其更倾向于在鲟鱼体表进行生长活动。梭杆菌在鲟鱼体表呈下降趋势,在鲟鱼体表生长受到压制。在鲟鱼体表前二十菌科中检测到气单胞菌科(1.22%)细菌,但在冬季水体和沉积物中都不属于前二十菌科,说明潜在致病菌在冬季也存在于养殖动物的环境中。春季为变形菌门的草酸杆菌科(Oxalobacteraceae,14.66%)和莫拉氏菌科(11.10%),与春季水体和沉积物梭杆菌科细菌不同,鲟鱼体表梭杆菌门相对丰度呈下降趋势,可能是鲟鱼运动过程中将梭杆菌科细菌散发到环境中。与冬季相比,鲟鱼气单胞菌科细菌上升到鲟鱼体表的第4优势菌群,W2气单胞菌科细菌相对丰度高达15.34%,推测春季鲟鱼已感染气单胞菌科细菌。夏季优势菌科为厚壁菌门的颤螺菌科(Oscillospiraceae,9.96%)和厚壁菌门的毛螺菌科(Lachnospiraceae,9.69%),颤螺菌科在水体和沉积物前二十菌科中均发现,为鲟鱼体表特有的特征菌群。秋季优势菌种为肠杆菌科(11.34%)和莫拉氏菌科(8.48%)。此外,在不同的季节,养殖环境中都存在假单胞菌科(Pseudomonadaceae)、气单胞菌科和肠杆菌科等潜在致病菌,且致病菌相对丰度出现明显的季节性变化(图 8)。
-
各采样点不同季节水环境因子变化见表 2,养殖水体pH值为7.96~9.31,溶解氧为5.56~10.04 mg/L,均在鲟鱼可以生存的范围内。
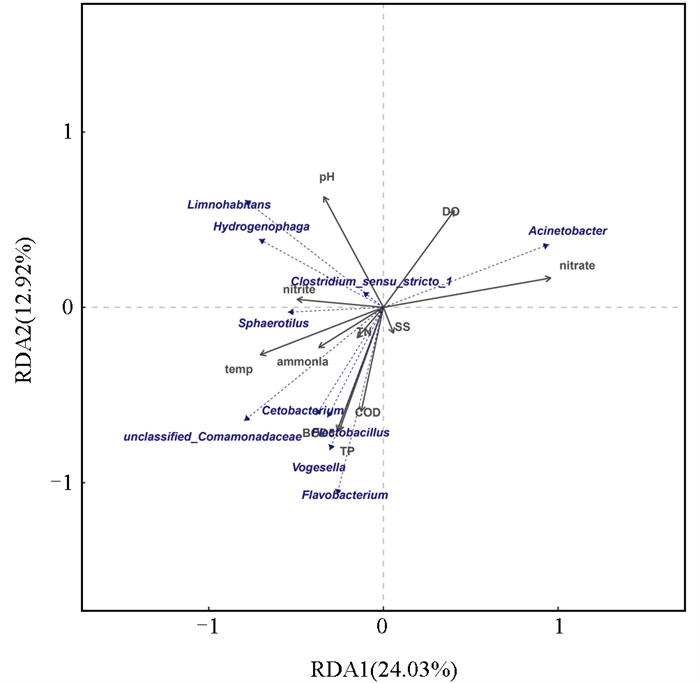
在不同季节,选择了菌属水平相对丰度前10位的菌属进行水体及体表菌群与环境因子之间的关系分析。属水平上的水体菌群与环境因子之间的RDA结果表明,横轴能解释的物种变量为24.03%,纵轴能解释的物种变量为12.92%(图 9)。水体的硝酸盐氮对水体菌群分布的影响较大。蒙特卡洛置换检验结果表明,温度、pH值、总氮、总磷、生化需氧量与水体菌群结构变化呈极显著负相关(p<0.01),氨氮和亚硝酸盐与水体菌群结构变化呈显著负相关(p<0.05),溶氧、硝酸盐氮与水体菌群结构变化呈极显著正相关(p<0.01),总氮和悬浮物含量与水体菌群结构相似性较低。
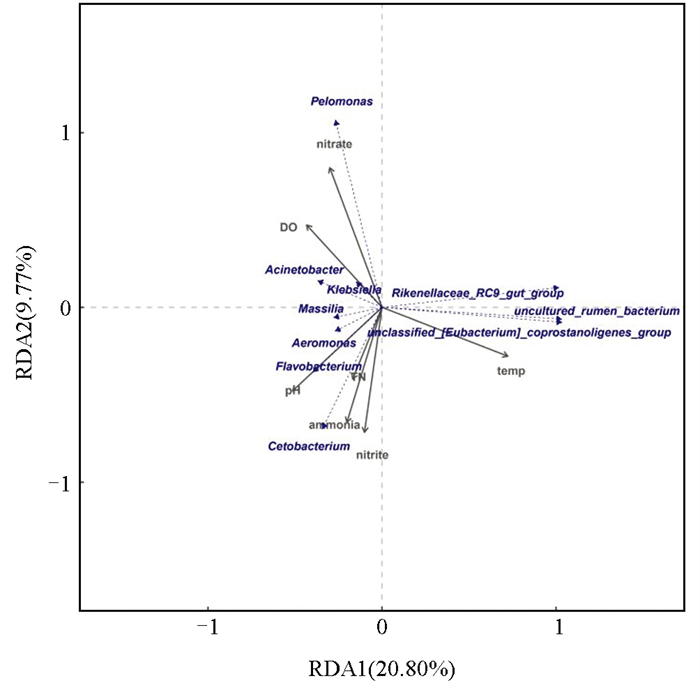
不同季节属水平下的鲟鱼体表菌群相对丰度与环境因子之间的RDA结果表明,横轴能解释的物种变量为20.80%,纵轴能解释的物种变量为9.77%(图 10)。环境因子硝酸盐氮及温度对不同季节下鲟鱼体表菌群分布的影响较大。蒙特卡洛置换检验表明,环境因子硝酸盐氮对鲟鱼体表菌群的影响最大。温度和总磷对鲟鱼体表菌群结构呈显著负相关(p<0.05),总氮、五日生化需氧量和悬浮物含量与鲟鱼体表菌群结构未显示出明显的相关性,其他环境因子均与鲟鱼体表菌群结构呈极显著正相关(p<0.01)。
2.1. 16S rRNA基因测序结果
2.2. 基于科学水平的细菌群落结构
2.3. 环境因子对菌群分布的影响
-
微生物作为养殖池塘生态系统的生产者和分解者,对维系生态系统平衡具有重要作用[22]。相关研究报道显示,沉积物菌群是水体菌群的主要来源,水体菌群结构一定程度上受到沉积物菌群的影响[23]。本研究中,水体菌群结构与沉积物菌群结构更为相似,且可与鱼类体表菌群分开来,与上述研究结果相同。鲟鱼体表菌群是抵御外界病原微生物入侵的第一道屏障,体表黏液为微生物提供了生长环境,鱼类体表黏液根据自身需要建立特定菌群,存在一些特殊的微生物,并在特定发育时期保持相对稳定,这些因素可能使体表菌群与环境菌群表现出一定的差异性[24-25]。许多研究表明,环境微生物与养殖动物疾病的发生有关[26],养殖环境微生物多样性的降低,致病菌或机会致病菌丰富度增加,均会增加水产动物疾病的发生概率[27]。
莫拉氏菌科细菌包括不动杆菌属和莫拉氏菌属,本研究中主要为不动杆菌属,不动杆菌属中包括一些潜在病原菌,如寄鱼不动杆菌(Acinetobacter piscicola)[28]、鲍曼不动杆菌(Acinetobacter baumannii)等[29]。本研究莫拉氏菌科细菌在水体之间呈下降趋势,但在沉积物中为上升趋势,造成这样的原因可能是水体中莫拉氏菌科细菌黏附于沉积物中,总体来看莫拉氏菌科主要来自水源。气单胞菌科细菌是鱼类的常见致病菌之一,主要包括嗜水气单胞菌(Aeromonas hydrophila)、温和气单胞菌(Aeromonas sobria)、维氏气单胞菌(Aeromonas veronii)等,其中温和气单胞菌[30]、维氏气单胞菌[12]和点状气单胞菌(Aeromonas punctata)[31]感染鲟鱼的案例已有相关研究。本研究中水体和沉积物中均检测到气单胞菌科细菌存在,且常年相对丰度常达1%以上,此时养殖生物已有感染细菌致病的风险。对各季节不同样本中气单胞菌科细菌相对丰度进行比较,发现春季气单胞菌相对丰度为四季中最高,此季节为细菌大量繁殖的时期。假单胞菌科细菌同样是鱼类的常见致病菌之一,在鲟鱼上已有感染荧光假单胞菌(Pseudomonas fluorescens)[32]和恶臭假单胞菌(Pseudomonas putida)[33]的案例。本研究中沉积物和鲟鱼体表前二十菌科中均检测出假单胞菌科细菌,相对丰度较气单胞菌科细菌较低,但当鲟鱼体质过弱时仍具有被感染的风险。肠杆菌科细菌在鲟鱼体表菌群中起重要作用。研究显示,肠杆菌科细菌并不是所有细菌对寄主都是致病的,但其下属的埃希氏菌属(Escherichia)、爱德华氏菌属(Edwardsiella)[9]、柠檬酸杆菌属(Citrobacter)、志贺氏菌属(Shigella)[10]、耶尔森氏菌属(Yersinia)[34]都是能导致水产动物细菌性疾病的致病菌。因此,在秋季有必要加强对肠杆菌科潜在致病菌的预防,以免造成较大的经济损失。
-
在生态环境中,细菌群落由少数优势类群和大量稀有种组成,其中优势种群分布广泛,个体总量多,其在细菌群落中的相对丰度往往较大,是进行生物化学循环的主要参与者[35]。在门的水平上,虹鳟(Oncorhynchus mykiss)体表以变形菌门和拟杆菌门为主[36];小头裸裂尻鱼(Schizopygopsis microcephalus)体表优势菌门为放线菌门(Actinobacteria)和变形菌门[37]。本研究发现,鲟鱼体表的优势菌群为厚壁菌门、变形菌门、拟杆菌门等,与上述研究的结论存在一些差异,推测可能是不同组织来源以及不同种类的微生物菌群由于宿主及养殖模式的不同,导致优势菌群的构成出现变化。同时,随着季节变化,鲟鱼体表优势菌群产生动态变化,说明鲟鱼体表菌群结构不仅受到环境的影响,还受到温度变化及自身日常代谢的影响。
在门水平上对水体及沉积物菌群进行研究,本研究发现水体及沉积物中优势菌门表现出较高的相似性,优势菌门均为变形菌门、梭杆菌门、拟杆菌门、厚壁菌门等,辽宁长海刺参(Apostichopus japonicus)养殖水体[38]及凡纳滨对虾(Litopenaeus vannamei)异养、自养型生物絮团[39]优势菌门均由变形菌门和拟杆菌门组成;鲟鳇网箱养殖水体菌门以变形菌门、放线菌门和拟杆菌门等为主[40],与本次研究结果类似。变形菌门作为第一优势菌门,主要原因是变形菌门在原核生物分子生物学分类或表型分类中占据了绝对的数量优势[41],具有利用碳源、去除氮与磷、降解有机物等作用[42-43]。拟杆菌作为次优势菌门,是浮游细菌的重要组成部分,其可产生能够降解生物大分子的胞外水解酶,同时,拟杆菌门还能发酵碳水化合物及分解纤维细胞壁的多糖[44],这些有机物也是水体碳循环的重要组成部分,在物质循环中具有极其重要的作用[45]。本研究发现养殖水体会随受外界环境因素影响呈现动态变化。冬季厚壁菌门细菌在3个池塘中均占有一定比例,3月份开始比例均减少,环境温度越低,水体中厚壁菌门细菌相对丰度越大。这可能是因为厚壁菌门下的芽孢杆菌纲大部分微生物,能够形成抗逆性极强的芽孢,从而产生极强的环境适应性[46]。同时,隶属于厚壁菌门的枯草芽孢杆菌(Bacillus subtilis)可以有效降低养殖水体中的硝酸盐和亚硝酸盐含量,能有效改善鲟鱼养殖水体水质,提高机体消化酶和非特异性免疫酶活性[47],从而促进鲟鱼生长发育,提高免疫力,推测此菌与冬季水体中亚硝酸盐含量较低存在一定关联。
-
水质变化会影响水体微生物的群落组成[48-49]。针对不同养殖水体,环境因子对微生物群落和功能结构的影响也不尽相同。举例来说,在凡纳滨对虾的大棚养殖池塘中,溶解氧、pH值、高锰酸盐指数和总氮是对微生物群落结构有显著影响的几个环境因子,其中pH值的影响最为突出[50]。然而,另有研究指出,在凡纳滨对虾的养殖水体环境中,氨氮、高锰酸盐指数和总氮对微生物群落结构的影响较为显著,且氨氮的影响最为显著[51]。这表明,即便是对于同一种养殖对象,影响微生物群落结构的环境因子也可能存在差异。同样有研究表明,总氮和总磷是水体微生物群落结构的主要影响因子[40, 52]。金笑等[53]研究鄱阳湖不同区域的沉积物,探讨细菌群落结构与功能的变化及其与环境因子之间的关联,结果指出,TN浓度对细菌分布的影响最为显著,而pH值则显著地影响微生物代谢的多样性。此外,陆洋等[54]的研究揭示了总磷、总氮、硝酸盐氮和氨氮等因素对养殖池塘水体细菌群落分布的影响。邱楚雯等[14]的研究进一步发现,总悬浮物、总磷以及总酸等水质因子能够影响细菌群落的构成。在本研究中,温度、总磷、硝酸盐氮对养殖水体细菌群落影响最为显著。由此可见,环境因子均有可能影响水质,参与到水体的物质循环。与张旭等[55]研究结果相似,本研究发现,总氮和氨氮对微生物群落结构和功能组成变化的影响并不显著,但仍有研究结果认为该因素为水体中微生物群落结构的主要影响因素[56]。
氮源是微生物生长的重要营养因子,微生物在生长繁殖过程中会主动吸收外界营养盐来补充能量及合成自身物质;其中硝化细菌能够进行硝化作用,将氨氮和亚硝酸盐转化为硝酸盐氮;反硝化细菌能够进行反硝化作用,将硝酸盐氮转化为氮气逸出水体环境[57-59]。本研究中,硝酸盐氮对水体及体表菌群影响均较大,而总氮和氨氮对菌群结构影响较小,说明在菌群生长繁殖过程中会吸收水体中的氮源物质,此时随着菌群数量的增加,水体氨氮和亚硝酸盐氮含量会减少。水体和沉积物中菌群与水体中硝酸盐氮含量呈显著正相关,鲟鱼体表菌群与水体中硝酸盐氮呈显著负相关,说明水体和沉积物中菌群进行硝化作用将水体中的氨氮和亚硝酸盐氮转化为硝酸盐氮,从而导致水体中硝酸盐氮含量上升[60]。鲟鱼体表菌群主要用于抵御外界潜在致病菌的侵袭,不进行硝化作用或者硝化效率极低,所以产生的硝酸盐氮较少。
-
鲟鱼流水养殖水体菌群结构多样性季节性变化明显,组间差异分析结果显示沉积物是水体菌群的主要来源,鲟鱼体表菌群大部分来源于环境菌群,其他部分菌群是鲟鱼自身生理活动的结果。流水养殖系统中均存在假单胞菌科、气单胞菌科和肠杆菌科等潜在致病菌,且致病菌相对丰度出现明显的季节性变化。影响养殖水体和鲟鱼体表菌群结构的主要环境因子为温度和硝酸盐氮,而五日生化需氧量、总磷、酸碱度、溶氧、化学需氧量、亚硝酸盐氮和氨氮对菌群结构也有一定的相关性。





 DownLoad:
DownLoad: