-
开放科学(资源服务)标识码(OSID):

-
榨菜以青菜头茎瘤芥为原料经腌制发酵而成[1],以其独特的风味和口感深受消费者喜爱。涪陵榨菜作为世界三大名腌菜之一,其产业是重庆市农村经济的支柱产业,年产量巨大,消费市场广阔。
发酵蔬菜风味物质的形成与发酵过程中微生物代谢活动密切相关[2-3],且涉及多种代谢途径,包括糖苷代谢、碳水化合物代谢、蛋白质水解代谢和脂肪酸代谢等[4]。有研究表明,乳酸菌和魏斯氏菌参与的碳水化合物代谢会促进醛酮类物质生成,抑制烯烃类物质,从而影响泡菜风味的形成[5]。榨菜发酵过程中,丰富的微生物群落将通过多种生化反应来塑造其独特的风味,这些风味物质将直接影响消费者的接受度[6]。近年来,关于榨菜发酵的研究主要集中在微生物多样性和风味物质的检测。文献[7]利用高通量测序技术探究了榨菜中原核微生物群落的演替,结果表明,发酵过程中乳杆菌属是其绝对优势属,而明串珠菌属主要存在于发酵初期。文献[8]的研究表明,榨菜发酵的熟成由不同种类乳酸菌的交替变化共同促进。文献[9]利用GC-MS技术从榨菜原料、成品中共鉴定出37种挥发性风味物质,主要为异硫氰酸烯丙酯、异硫氰酸环丙酯和对丙烯基茴香醚。文献[10]的研究表明,随着榨菜发酵的进行,其醇类、酯类、醛类、酮类等化合物含量呈增加趋势,异硫氰酸酯类物质含量呈减少趋势。目前尚未有榨菜发酵过程中微生物与挥发性风味物质间的相关性研究。
分子生物学技术和代谢组学技术的快速发展为解析食品发酵过程中微生物与风味物质的相关性提供了有力工具。文献[11]采用Pacbio SMRT测序技术和GC-IMS技术研究了酸汤中微生物的多样性和挥发性风味物质间的关系。文献[12]利用高通量测序技术、气相色谱离子迁移技术,通过Pearson相关性分析揭示了香肠的微生物优势菌群与挥发性风味物质的相关性。因此,通过高通量测序技术结合代谢组学技术全面分析传统发酵食品中微生物与挥发性风味物质的关系完全可行。
本研究拟采用高通量测序技术、顶空固相微萃取-气相色谱-质谱联用技术分析榨菜发酵过程中微生物菌群结构和挥发性风味物质的变化,探究主要优势微生物菌属与挥发性风味物质成分种类间的相关性,为阐明榨菜风味形成机制、优化传统生产工艺、提升产品品质提供理论依据。
HTML
-
榨菜原料(青菜头)购自重庆市涪陵区某农户。
正十五烷-d32:分析纯,上海麦克林生化科技股份有限公司;正构烷烃混标(C10-C25):标准品,LGC集团公司;MagAtrract PowerSoil Pro DNA Kit:试剂盒,德国凯杰(qiagen)生物公司;快速Pfu聚合酶:扩增速度4 kb/min,北京全式金生物技术有限公司。
-
气相色谱-质谱联用仪:7697A-8890-7000D,安捷伦科技有限公司;PCR仪:T100 Thermal Cycler,美国BIO-RAD公司;电泳仪:JY600C,北京君意东方电泳设备有限公司。
-
新鲜青菜头去筋。一盐用盐量4%(质量比),在塑料大桶一层菜一层盐腌制15 d后,捞起青菜头,倒掉废盐水;二盐再补加盐量5%(质量比),在塑料大桶一层菜一层盐腌制,于25 ℃密封发酵。补加二盐后第0、4、8、12、16个月取样,每次取腌制桶上、中、下层样品混合,依次记为ZX4_0、ZX4_4、ZX4_8、ZX4_12、ZX4_16。
-
参照文献[13]的测序方法稍作修改。根据微生物群落总基因组DNA试剂盒提取样品总DNA,采用引物338F_806R和IT1F_IT2R,扩增细菌16S rRNA基因V3-V4可变区、真菌的ITS-V1区。采用Illlumina MiSeq平台和MiSeq Reagent Kit v3进行双端2×250 bp测序,测序由上海美吉生物医药科技有限公司完成。
-
参照文献[14]的测序方法稍作修改。取2 g样品置于20 mL顶空瓶,加入内标2.0 μL(正十五烷-d32 100 μg/mL)立即密封顶空瓶。温度80 ℃,平衡20 min,SPME萃取头样品吸附时间20 min,样品解吸时间2 min。
气相色谱条件:毛细管柱为25 m×0.25 mm×0.20 μm(Agilent CP9204),压力为100.00 kPa。进样口温度240 ℃,载气为高纯氦气,载气流速1.50 mL/min,隔垫吹扫流速3 mL/min,不分流进样。升温程序:初始温度40 ℃,平衡0 min;然后以15 ℃/min的速度升至150 ℃;再以5 ℃/min的速度升至230 ℃,并维持5 min;最后运行230 ℃,维持2 min。
质谱条件:电子轰击离子源(EI),传输线温度为280 ℃,离子源温度230 ℃,四极杆温度150 ℃,电子能量70 eV。扫描方式为全扫描模式(SCAN),质量扫描范围为50~500 m/z,扫描频率为3.2 Hz。
-
每个试验样本设定3个重复,结果以 x±s表示,数据采用SPSS 17.0软件进行处理。用内标法对挥发性风味化合物进行定量,利用Origin软件和美吉生物云平台绘图。微生物群落与挥发性风味物质种类采用皮尔逊(Pearson)相关分析方法,利用R语言绘图。
1.1. 材料与试剂
1.2. 仪器与设备
1.3. 实验方法
1.3.1. 榨菜样品的制备
1.3.2. 菌群结构高通量测序分析
1.3.3. 挥发性风味物质分析
1.4. 数据处理
-
榨菜发酵过程中微生物群落的丰富度和多样性如表 1所示,随着发酵的进行,细菌Chao1指数、Shannon指数逐渐增大,Simpson指数逐渐减小,说明榨菜细菌的丰富度和多样性程度逐渐增加;真菌Chao1指数和Shannon指数在ZX4_12组达到最大值,说明榨菜发酵至12个月时真菌的丰富度和多样性程度最高,随后真菌丰富度和多样性程度迅速降低,可能是由于发酵后期酸度较高,抑制了部分不耐酸的真菌的生长繁殖,从而造成真菌丰富度和多样性程度降低[15]。
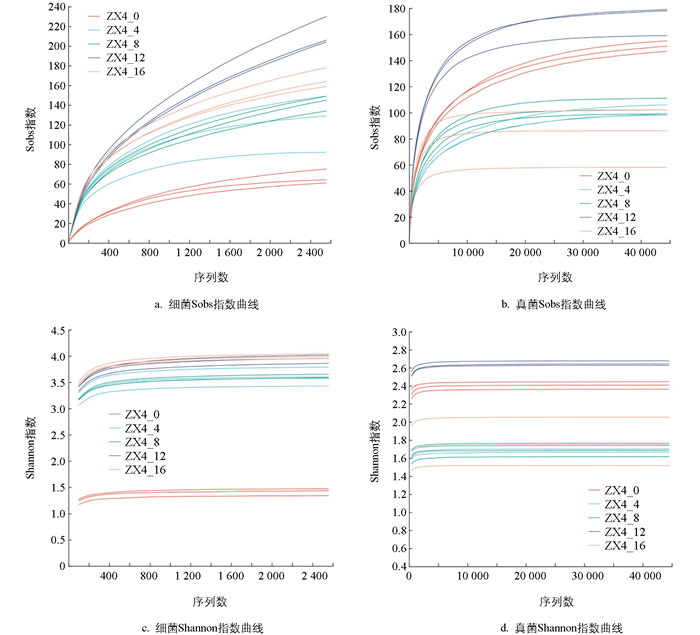
榨菜样品细菌和真菌稀释曲线(Sobs指数)和Shannon曲线(Shannon指数)如图 1所示,随着序列数的增加,曲线趋于平缓,表明样品测序量充分,足以反映各组榨菜样品情况。
-
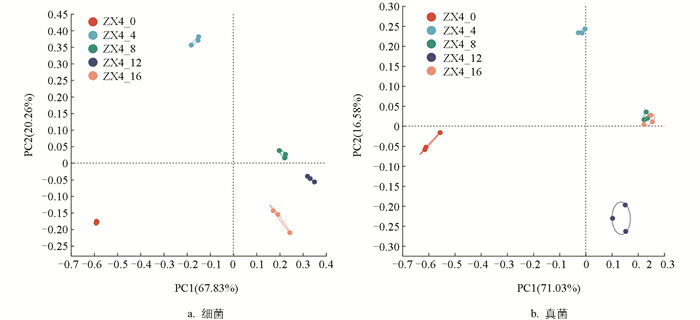
对榨菜发酵过程中样品细菌和真菌的ASV数据进行主坐标分析,研究榨菜样品在组间和组内群落的相似性或差异性,结果如图 2所示。细菌主坐标分析中PC1贡献率为67.83%,PC2贡献率为20.26%;真菌主坐标分析中PC1贡献率为71.03%,PC2贡献率为16.58%,证明图 2具有较好的解释效果。ZX4_0、ZX4_4、ZX4_8组细菌和真菌均处于不同象限,细菌ZX4_12、ZX4_16组处于同一象限,真菌ZX4_12、ZX4_16组处于相邻象限,说明榨菜发酵前期(0到4个月)微生物群落差异较大,中后期(8到16个月)差异较小。其中PC1是影响微生物群落结构的最主要因素的投影方向,PC2是影响微生物群落结构的第二重要因素的投影方向。
-
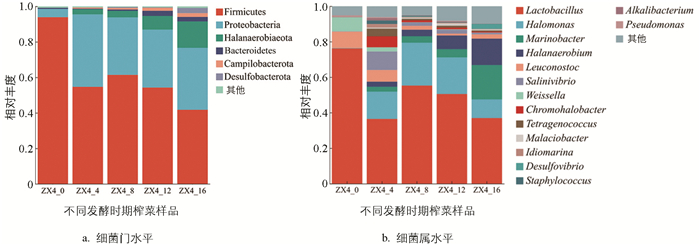
榨菜样品在门水平共检测出6个优势细菌门(相对丰度大于1%),分别为厚壁菌门(Firmicutes)、变形杆菌门(Proteobacteria)、盐厌氧菌门(Halanaerobiaeota)、拟杆菌门(Bacteroidetes)、弯曲菌门(Campilobacterota)、脱硫杆菌门(Desulfobacterota)。榨菜二盐初期(0个月)厚壁菌门为绝对优势菌门,占比93.96%;随着发酵的进行,厚壁菌门和变形杆菌门成为主要优势菌门,这两个菌门是绝大多数发酵蔬菜的优势细菌门(图 3a)。
榨菜样品在属水平共检测出15个优势细菌属(相对丰度大于1%),主要为乳杆菌属(Lactobacillus)、盐单胞菌属(Halomonas)、海洋杆菌属(Marinobacter)、盐厌氧菌属(Halanaerobium)、明串株菌属(Leuconostoc)、嗜盐菌属(Salinivibrio)、魏斯氏菌属(Weissella)、色盐杆菌属(Chromohalobacter)、四联球菌属(Tetragenococcus)等。发酵初期(0个月)主要优势菌属为乳杆菌属、明串株菌属和魏斯氏菌属,与泡菜优势菌群一致[13],可能是由于榨菜一盐腌制用盐量(质量比4%)与泡菜发酵用盐量较相似,均为低盐发酵,导致细菌属类似,二盐再加5%盐后,随着发酵的进行,乳杆菌属占比由76.24%减少至55.3%,盐单胞菌属占比由0.21%增加至24.13%,明串株菌属(9.24%)和魏斯氏菌属(7.96%)分别减少至2.16%、0.22%。到发酵后期(16个月)主要优势菌属变为乳杆菌属、盐单胞菌属、海洋杆菌属和盐厌氧菌属(图 3b)。有研究表明耐盐菌属为用盐量质量比10%的蔬菜的优势菌属[16]。乳杆酸菌属作为整个发酵过程的主要优势菌属,对发酵产品风味的形成有重要作用[17-18]。盐单胞菌属于耐盐菌,能发酵葡萄糖产酸,分泌丰富的酶系,产生多种风味物质,使泡菜风味更饱满[19]。
-
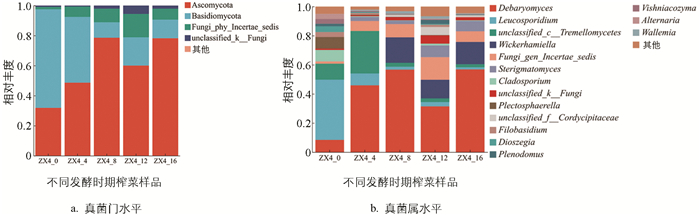
在门水平共检测出4个优势真菌门(相对丰度大于1%),分别为子囊菌门(Ascomycota)、担子菌门(Basidiomycota)、Fungi_phy_Incertae_sedis、unclassified_k Fungi。榨菜发酵初期(0个月)担子菌门为其主要优势菌门,中后期(8到16个月)子囊菌门为主要优势菌门(图 4a)。
在属水平共检测出16个优势真菌属(相对丰度大于1%),主要为德巴利氏酵母属(Debaryomyces)、白冬孢酵母属(Leucosporidium)、未分类的银耳属(unclassified_c Tremellomycetes)、拟威克酵母属(Wickerhamiella)、嗜盐梗孢酵母属(Sterigmatomyces)、枝孢属(Cladosporium)、unclassified_k_Fungi等。发酵初期(0到4个月)主要真菌属为德巴利氏酵母属、白冬孢酵母属、未分类的银耳属,中后期(8到16个月)主要真菌属为德巴利氏酵母属、拟威克酵母属(图 4b)。白冬孢酵母属主要存在蔬菜表面且嗜冷性极强,其在榨菜发酵早期大量存在,可能与榨菜主要在冬季收获、腌制有关;银耳属在大头菜发酵期也被大量检出[20];德巴利氏酵母属和拟威克酵母属主要存在于发酵中后期,其具有一定的耐酸耐盐特性,能利用多种碳源,促进醇类、酯类和其他代谢产物的形成[21-22],有利榨菜发酵后期风味的形成。
-
榨菜发酵过程中挥发性风味物质成分顶空固相微萃取-气相色谱-质谱联用检测结果见表 2,挥发性风味物质成分分类含量和种类数见表 3。
由表 2、表 3所示,共鉴定出120种挥发性风味物质成分,包括酯类33种、醇类16种、酸类12种、有机硫化物类8种、醚类6种、烃类9种、醛类14种、酮类8种、酚类5种、胺类4种、其他类5种。在榨菜整个发酵过程中,挥发性风味物质总含量呈先减少后增加趋势,由689.35 μg/kg下降至405.58 μg/kg再上升至540.28 μg/kg。在发酵初期0个月,主要为有机硫化物类、酯类和醇类;发酵4到8个月,主要为酯类、醇类和酸类;发酵后期12到16个月,主要为酯类、酸类和醇类,其次为醚类、有机硫化物类以及烃类物质。这些物质共同赋予涪陵榨菜独特的风味。
酯类物质作为香气骨架成分,主要由酸类和醇类物质酯化反应产生[23]。在榨菜整个发酵过程中,酯类物质由113.06 μg/kg(21种)增加至348.22 μg/kg(29种),是发酵后期的主要风味物质,约占总量的64.45%,其中亚麻酸乙酯、2-甲基己酸甲酯和棕榈酸甲酯含量较高,是榨菜的主要挥发性酯类物质,这与文献[24]的研究结果相似。到发酵末期16个月时,主要增加了乙酸乙酯(苹果香气)、丁酸乙酯(菠萝甜香)、乳酸丙酯(奶油风味)、9-十六烯酸乙酯(花香)、顺-9-十八烯酸丙酯等,能赋予榨菜更多水果香、花香和甜香[25-26]。
醇类物质的合成途径主要为氨基酸代谢、乳糖代谢、亚麻酸和亚油酸降解,其对酯类、醛类和酮类物质的产生至关重要,是发酵食品风味形成不可或缺的成分[27]。榨菜醇类物质主要存在于发酵4到8个月,其含量最高85.83 μg/kg,其中2-丙醇、1-辛烯-3-醇、芳樟醇等随着发酵的进行含量逐渐减少,可能是由于其参与了发酵后期的酯化发应[28]。醇类物质中,异戊醇和正戊醇呈果香、醇香,1-辛烯-3-醇呈蘑菇香,5-降冰片烯-2-醇呈松木香且略带清凉感,苯乙醇具有新鲜面包香、清甜的玫瑰香,其在榨菜发酵中常被检出[29]。
酸类物质是发酵食品风味形成的重要物质,具有维持和协调香气的作用[30]。发酵初期0个月,仅检测到草酸和正辛酸,总量38.20 μg/kg(2种)。随着发酵的进行,酸类物质种类和含量逐渐增加,到发酵结束时(16个月),检测出酸类物质总量64.66μg/kg(11种),而文献[24]的研究表明,榨菜发酵过程中酸类物质含量逐渐减少,与本研究结果相反,可能与加工工艺和用盐量不同有关。到榨菜发酵后期主要增加了乙酸、正戊酸、正丁酸、棕榈油酸等。
榨菜发酵过程中的有机硫化物类主要为异硫氰酸酯类,异硫氰酸酯类是榨菜原料青菜头辛辣味的主要来源,在榨菜腌制过程中其辛辣味逐渐消失[31]。在发酵初期0个月,有机硫化物类含量为372.08 μg/kg,占该时期挥发性风味物质成分总量的53.98%,随着发酵的进行,其含量迅速减少,发酵4个月时,其含量仅57.51 μg/kg,到发酵16个月时,为12.63 μg/kg,占总量的2.34%。
随着发酵的进行,榨菜中醚类物质含量逐渐增加,到发酵末期为24.38 μg/kg,其中,丙烯基茴香醚又称茴香脑,是其主要醚类物质,呈鲜茴香、甜香、辛香的口感,对于榨菜形成特有的辛香味具有重要作用[32];醛类物质含量和种类数均降低,可能与发酵系统酸度增加和微生物群落的变化有关。烃类、酮类和酚类物质在整个发酵过程中含量和种类数变化不大。
-
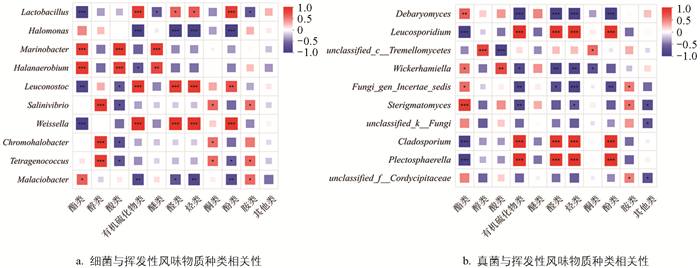
榨菜挥发性风味受原料、微生物和工艺条件等诸多因素的影响,微生物对其挥发性风味物质的形成至关重要。为了研究不同微生物与榨菜挥发性风味物质成分之间的相关性,采用Pearson相关性分析探究了各挥发性风味物质种类和优势微生物菌属(相对丰度排名前10)之间的相关关系,结果如图 5所示。大部分主要细菌属与挥发性风味物质种类呈正相关。乳杆菌属、明串株菌属和魏斯氏菌属与挥发性风味物质种类的相关性较一致,均与榨菜有机硫化物类、醛类、烃类和酚类呈显著正相关(p<0.05),其中,与有机硫化物类高度显著正相关(p<0.001),而与酯类呈极显著负相关(p<0.01)。乳杆菌属、魏斯氏菌属常在泡菜以及酒类发酵过程中被检出,与风味的形成密切相关[33-34]。盐单胞菌属与有机硫化物类、醛类、烃类、酚类呈高度显著负相关(p<0.001)。海洋杆菌属和盐厌氧菌属均与酯类、酸类以及醚类极显著正相关(p<0.01)。嗜盐菌属、色盐杆菌属和四联球菌属与醇类呈高度显著正相关(p<0.001),与酮类呈显著正相关(p<0.05)。德巴利氏酵母属作为榨菜发酵中后期的主要优势真菌属,与大部分挥发性风味物质种类呈高度显著负相关(p<0.001),文献[35]的研究表明德巴利氏酵母属与豆瓣酱风味呈正相关,这与本文研究结果相反,可能与发酵原料、发酵工艺不一致有关。白冬孢酵母属、枝孢属和癣襄腔菌(Plectosphaerella)属,均与酯类呈高度显著负相关(p<0.001),与有机硫化物类、醛类、烃类以及酚类呈高度显著正相关(p<0.001);拟威克酵母属与大部分挥发性风味物质种类呈明显负相关,与酯类呈显著正相关(p<0.05),与酸类呈极显著正相关(p<0.01);嗜盐梗孢酵母与酯类呈高度显著正相关(p<0.001)。说明榨菜独特风味的形成是由多种微生物共同作用产生。根据实际生产,可通过调节榨菜发酵过程中微生物种类来改善榨菜风味。
2.1. 榨菜发酵过程中微生物群落多样性
2.1.1. α多样性分析
2.1.2. β多样性分析
2.2. 榨菜发酵过程中细菌和真菌的群落结构
2.2.1. 细菌群落结构
2.2.2. 真菌群落结构
2.3. 榨菜发酵过程中挥发性风味物质
2.4. 挥发性风味物质成分种类与微生物之间的相关性
-
采用高通量测序技术和顶空固相微萃取-气相色谱-质谱联用技术研究了涪陵榨菜发酵过程中微生物群落、挥发性风味物质成分的变化以及两者间的相关性。榨菜发酵初期,主要优势菌属为乳杆菌属、明串株菌属、德巴利氏酵母属和白冬孢酵母属;到发酵中后期,演变为乳杆菌属、盐单胞菌属、海洋杆菌属、德巴利氏酵母属以及拟威克酵母属。发酵过程中共检测到120种挥发性风味物质,主要挥发性风味物质为有机硫化物类、酯类、醇类和酸类,含量较高的风味物质为全异硫氰酸酯、2-甲基己酸甲酯、5-降冰片烯-2-醇、亚麻酸乙酯和草酸。微生物与挥发性风味物质成分相关性表明,优势细菌属与大部分挥发性风味物质种类呈正相关,其中,乳杆菌属、明串株菌属和魏斯氏菌属均与有机硫化物类、醛类、烃类和酚类显著正相关(p<0.05);海洋杆菌属和盐厌氧菌属均与酯类、酸类以及醚类极显著正相关(p<0.01)。嗜盐菌属、色盐杆菌属和四联球菌属与醇类呈高度显著正相关(p<0.001)。优势真菌属对榨菜风味的形成也至关重要,德巴利氏酵母属与大部分挥发性风味物质种类呈高度显著负相关(p<0.001),而白冬孢酵母属、枝孢属、癣襄腔菌属,均与大部分挥发性风味物质种类呈高度显著正相关(p<0.001)。本研究有助于解析菌群结构对涪陵榨菜风味形成的关系,并为改进榨菜加工工艺及调控产品品质提供了一定理论基础。





 DownLoad:
DownLoad: