-
开放科学(资源服务)标识码(OSID):

-
核桃(Juglans regia L.)为胡桃科(Juglandaceae)胡桃属(Juglans)小乔木,是我国重要的经济林木之一。核桃果实可食用,也可榨油,核桃油是一种药用价值很高的植物油[1]。自2015年以来,核桃已在我国多个省(区、市)推广种植。随着种植面积的不断扩大及苗木调运的日益频繁,核桃中各类病害的发生与危害程度也呈加重趋势。目前已报道的核桃病害种类繁多,包括核桃细菌性黑斑病、炭疽病、褐斑病、白粉病、溃疡病、腐烂病、枝枯病等[2-5]。其中,核桃细菌性黑斑病、褐斑病与炭疽病发病率高、危害严重,是核桃的三大主要病害。
核桃细菌性黑斑病是一种由多种细菌引起的病害,已知的病原菌包括野油菜黄单胞菌(Xanthomonas campestris)、树生黄单胞菌(Xanthomonas arboricola)以及成团泛菌(Pantoea agglomerans)等。该病害在世界各核桃产区均有发生,优势病原种群因地域而异[6-8]。核桃的叶片、果实及茎秆等部位均可能受病原菌侵染。叶片染病后,多形成多角形黑色病斑,部分病斑周围伴有黄色晕圈,潮湿条件下呈水渍状;枝条受侵染后,皮层发黑并逐渐腐烂;果实染病后,表面出现大型黑色病斑,中央略凹陷。病害严重时,可导致枝叶组织腐烂坏死,果实提前脱落[9-10],给核桃生产造成严重损失。例如,2017年,济南市南部山区0.34万hm2核桃感染该病害,导致产量损失约40%,经济损失达2500余万元[11]。
目前,核桃细菌性黑斑病仍以化学防治为主,农业防治和生物防治为辅。怀婷婷等[12]指出,强化田间栽培管理、合理间作豆科植物,能够有效降低病害发生概率。在植株展叶及落花后,可喷施波尔多液进行预防;发病期可使用代森锰锌+春雷霉素、甲基托布津+春雷霉素组合喷施防治;成团泛菌单独侵染时,中生菌素和春雷霉素防控效果较好。王英杰等[13]提出了一套综合防治措施:越冬期清理果园,减少病原菌栖息场所;萌芽前喷洒石硫合剂,降低越冬菌源;展叶期交替使用噻唑锌、喹啉铜等药剂;6月结合田间发病情况,施用甲基托布津、二氯异氰尿酸钠与波尔多液,实现炭疽病与细菌性黑斑病混发危害的协同防控。此外,病害发生前应以预防为主,降低初始菌量,阻断病原菌的侵入,如越冬期使用5%的波尔多液将树干涂白,幼果期喷施代森锰锌和氢氧化铜。病害发生后,可喷施具有强效杀菌作用的抗生素类药剂和铜锌制剂进行应急防控。室内药效试验结果表明,杀菌剂中的四霉素、乙蒜素和噻霉酮对野油菜黄单胞菌和成团泛菌抑菌活性较高[14-15]。
尽管化学防治是当前较为有效的防控手段,但仍存在诸多亟待解决的问题[16]。例如,长期单一使用某类药剂(尤其是铜制剂)易筛选出抗性菌株,导致药剂防效下降;部分化学药剂对生态环境存在潜在风险,长时间使用会造成有害物质残留;病害发生受环境影响较大(尤其是湿度),若施药时机不当或天气条件不适宜,会显著降低防治效果。
因此,针对重庆市核桃细菌性黑斑病特定的病原菌组成,开展本地化的高效药剂筛选,对于制定精准有效的化学防治方案、延缓病原菌抗药性、保障该地区核桃产业健康发展具有重要意义。基于此,以该病害的2种主要病原菌,即野油菜黄单胞菌(X. campestris)和成团泛菌(P. agglomerans)为研究对象,进行室内药剂筛选试验,旨在明确常用杀菌剂对2种本地病原菌的抑菌活性,筛选出高活性药剂并分析其毒力差异,以期为该病害在重庆市科学用药策略的制定及绿色防控体系的构建提供核心数据与理论依据。
HTML
-
供试菌株:实验室前期研究中所分离的重庆市核桃细菌性黑斑病病原菌成团泛菌分离株(BSL-1-c)、野油菜黄单胞菌分离株(SZL-2-a-6)[17]。
培养基:营养琼脂(NA)培养基、Luria-Bertani(LB)培养基。
供试药剂:选用11种商品杀菌剂作为供试药剂,包括铜制剂、抗生素及植物源杀菌剂等,其有效成分含量、剂型、生产厂商等信息见表 1。
-
将成团泛菌菌株和野油菜黄单胞菌菌株分别制备成浓度为1×108 CFU/mL的菌液。培养基与菌液体积比为20∶1,向约50 ℃的NA培养基中加入相应体积的菌液,充分摇匀。为保证含菌培养基厚度一致,用移液器精确吸取10 mL含菌培养基注入直径为90 mm的培养皿中,于超净工作台中冷却凝固。
-
用镊子将直径为6 mm的灭菌滤纸片等距置于含菌培养皿上,使其呈三角形排布。为排除溶剂干扰,用无菌去离子水将待测药剂配制成相应质量浓度的药液,吸取10 μL药液均匀滴加在滤纸片上。将接种后的培养皿置于28 ℃培养箱中恒温培养24 h,观察并记录抑菌圈产生情况。
-
将初筛得到的有效药剂配置成等比质量浓度梯度,以滴加等量(10 μL)无菌去离子水的滤纸片作为阴性对照(CK)。按照1.3节所述方法进行滤纸片抑菌活性测定,每个质量浓度处理设置3个重复。培养结束后,采用十字交叉法测量抑菌圈直径。
药剂的抑菌活性以抑菌率表示,计算公式如下:
抑菌率=(处理组抑菌圈直径-对照组抑菌圈直径)/处理组抑菌圈直径×100%。
阴性对照未产生抑菌圈,以滤纸片直径6 mm为对照值,处理组抑菌圈直径与对照组抑菌圈直径之差记为有效抑菌圈直径。
-
利用SPSS 25.0软件,根据药剂质量浓度与相对抑菌率建立杀菌剂的毒力回归方程,并计算EC50。同时,对抑菌圈直径测定数据进行统计分析。采用单因素方差分析检验不同处理组间的差异显著性,若差异有统计学意义(p < 0.05),则进一步采用Duncan’s新复极差法进行多重比较。通过比较各药剂的EC50值,筛选出对2种病原菌具有强抑菌活性的药剂,并确定其有效抑菌圈直径范围。
1.1. 实验材料
1.2. 含菌培养基制备
1.3. 有效杀菌剂筛选
1.4. 杀菌剂抑菌率测定
1.5. 毒力回归方程的建立与EC50分析
-
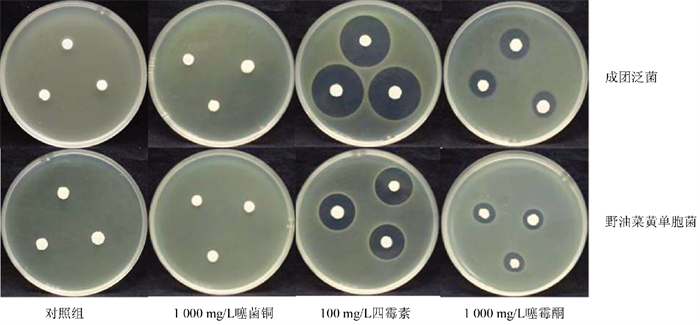
选用噻菌铜等11种市售常用杀菌剂,分别以成团泛菌和野油菜黄单胞菌作为指示菌,设置10、100、1 000 mg/L 3个质量浓度梯度,以初步判断各药剂的最低抑制质量浓度范围(预实验中发现四霉素活性极高,100 mg/L已能产生非常明显的抑菌圈,且显著优于其他供试药剂在1 000 mg/L下的抑菌效果,因此未设置更高质量浓度)。将灭菌后的滤纸片等距呈三角形放置于含菌培养皿上,分别吸取10 μL各质量浓度梯度药剂滴加在滤纸片上,将培养皿在28 ℃培养箱培养24 h。经培养发现,药剂质量浓度在1 000 mg/mL以下时,只有四霉素、中生菌素、乙蒜素、噻霉酮、春雷霉素5种药剂出现明显抑菌圈,部分药剂室内抑菌试验结果如图 1所示。
-
对初筛获得的5种有效杀菌剂进行定量抑菌活性测定,结果如表 2所示。四霉素在100 mg/L质量浓度下对2种病原菌的抑菌效果均显著优于其他供试药剂(p < 0.05)。对于成团泛菌(P. agglomerans),四霉素(100 mg/L)的有效抑菌圈直径为2.52 cm,抑菌率为80.8%,显著优于其他药剂;噻霉酮(1 000 mg/L)、中生菌素(1 000 mg/L)和乙蒜素(1 000 mg/L)对成团泛菌的抑菌率无显著差异,但均显著高于春雷霉素(1 000 mg/L)。对于野油菜黄单胞菌(X. campestris),四霉素(100 mg/L)的有效抑菌圈直径达1.60 cm,抑菌率为72.7%,显著优于其他药剂;各药剂在该病原菌上的抑菌活性排序为:四霉素(100 mg/L)>乙蒜素(1 000 mg/L)>噻霉酮(1 000 mg/L)>中生菌素(1 000 mg/L)>春雷霉素(1 000 mg/L)。此外,在测试质量浓度范围内,噻菌铜、噻唑锌、喹啉铜、氢氧化铜、宁南霉素及氯溴异氰尿酸对2种病原菌均未表现出抑菌活性(抑菌圈直径为0)。
-
根据抑菌率数据建立毒力回归方程并计算各药剂的EC50值(表 3)。由表 3可知,四霉素对2种病原菌的EC50值均最低,表现出最强的抑菌活性。综合EC50值与95%置信区间分析,供试药剂对2种病原菌的抑菌活性排序如下:对成团泛菌,抑菌活性依次为四霉素>中生菌素>噻霉酮>乙蒜素>春雷霉素;对野油菜黄单胞菌,抑菌活性依次为四霉素>中生菌素>乙蒜素>噻霉酮>春雷霉素。春雷霉素的EC50值显著高于其他4种药剂,抑菌活性最弱。
2.1. 有效杀菌剂筛选
2.2. 有效杀菌剂活性测定
2.3. 毒力回归方程的建立与EC50分析
-
本研究通过室内毒力测定,筛选出四霉素、中生菌素、噻霉酮、乙蒜素和春雷霉素5种对重庆市核桃细菌性黑斑病病原菌(野油菜黄单胞菌和成团泛菌)具有抑制活性的药剂。其中,四霉素对2种病原菌均表现出最强的抑菌毒力,其EC50值显著低于其他供试药剂,可作为防治该病害的首选或核心药剂,优先开展后续田间验证。中生菌素、噻霉酮和乙蒜素表现出中等强度的抑菌活性,而春雷霉素的EC50值较高,室内抑菌效果相对较弱。
本研究的室内筛选结果为田间防治药剂的科学选择提供了直接依据。首先,明确了抗生素类(四霉素、中生菌素)和植物源杀菌剂(乙蒜素)对本地病原菌的高活性,为减少传统铜制剂依赖、推动杀菌剂多元化使用提供了可行选项。其次,本研究所获得的EC50值范围,可为田间试验的初始质量浓度设置提供关键参考,避免盲目用药。尤为重要的是,研究揭示了不同作用机理药剂间的活性差异,这为制定“以四霉素为核心,轮换或复配使用中生菌素、噻霉酮等不同作用机理药剂”的田间抗性治理策略提供了理论支撑,有助于延缓抗药性的发展。
本研究中以噻菌铜为代表的铜制剂未显示抑菌活性,这与诸多田间报道其具有良好防效的结果相悖。这一现象凸显了室内筛选与田间应用的差异:铜制剂多为保护性杀菌剂,其药效依赖在植物体表形成保护膜或经内吸传导后激发的系统性防御,而非直接接触杀菌[18]。因此,室内筛选结果不能否定铜制剂的田间应用价值,但提示其可能不适用于以快速抑制菌量为目标的治疗性施药场景。未来的田间试验应综合考虑保护性与治疗性药剂的科学搭配,以提升整体防治结果。
此外,本研究与谯天敏等[19]的报道一致,均证实四霉素对核桃细菌性黑斑病病原菌具有突出的抑菌效果,进一步增强了该药剂应用的可信度。但室内试验的理想条件与田间复杂的生态环境存在巨大差异,药剂在实际应用中的防效还受施药技术、气候条件、核桃生育期及树体健康状况等多重因素影响。因此,将本研究筛选出的高活性药剂(尤其是四霉素)在重庆本地核桃产区进行规范的田间药效试验,是后续研究不可或缺的关键环节。
综上所述,本研究明确了针对重庆市核桃细菌性黑斑病的优选药剂序列,并为后续田间防治策略的设计提供了关键毒力参数和应用思路。建议未来在此基础上开展盆栽幼苗防治试验,进一步探索高活性药剂的复配增效作用,为构建绿色、高效、可持续的综合防控技术体系奠定坚实基础。




 DownLoad:
DownLoad: