-
开放科学(资源服务)标识码(OSID):

-
近年来全球糖尿病患者数量持续增长,每年因糖尿病死亡的人数高达数百万,糖尿病的早期预防和诊断引起了人们的高度重视. 糖尿病患者体内高浓度的血糖会影响人体的新陈代谢,导致全身器官功能障碍甚至衰竭,因此在初期对糖尿病患者血液中葡萄糖浓度的检测和控制显得尤为重要. 不仅如此,葡萄糖浓度的准确高效检测在食品工业、环境检测以及生物医学等多个领域也有广泛的应用[1],这进一步凸显了研究高灵敏度、高稳定性、低成本的葡萄糖电化学传感器的重要性. 电化学传感器是一种感应化学物质并将其浓度转化为电信号进行检测的仪器,可分为酶传感器和无酶传感器. 传统的酶修饰传感器因酶的活性不稳定,易受外界温度、溶液pH值等因素的影响而导致其稳定性较差,在实际应用领域有一定的局限性. 与酶传感器相比,无酶电化学传感器就显得更具优势,随着科研工作者的深入研究,目前的无酶传感器具有灵敏度高、稳定性好、响应快、选择性好、成本低、制备简单等优点[2-3].
电极材料参与电化学催化氧化反应,作为电化学传感器的重要组成部分,其研究一直备受科研人员关注. 常见的电极材料包括贵金属、过渡金属以及过渡金属氧化物等. 由于贵金属价格昂贵且容易被溶液中阴离子所毒化,所以难以大规模应用;而过渡金属在溶液或者空气中不够稳定,容易发生反应生成化合物,因此科研人员大量研究了过渡金属Fe、Co、Ni、Cu、Zn等的氧化物形态、功能以及在电化学催化领域的应用. 黄小梅等[4]利用室温、水溶剂法在玻碳电极上生长了CuO/CoO纳米颗粒材料,制备的无酶葡萄糖传感器对葡萄糖的检测具有良好的催化活性和较高的灵敏度. 韩枫等[5]以泡沫镍为基底,采用水热法和煅烧合成了多级花状Co3O4/Ni金属复合物的高性能无酶葡萄糖传感器. 由此可见,过渡金属氧化物因其成本低、响应快、灵敏度高等优点,在电化学传感器的应用方面备受关注,有很好的发展前景.
电极的形态也是影响传感器性能的一个重要因素,传统的常用基底有泡沫镍[6-7]、碳布[8-9]、玻碳电极[10-11]等材料. 相比而言,金属细丝电极由于直径细小,且具有更强的电子转移能力和更高的电流密度[12],有助于提高电化学传感器对检测物质的灵敏度. 此外金属细丝电极不仅可检测各种溶液和环境中的物质,还可为开发刺入式或微流控式的葡萄糖传感器提供电极基础[13-14]. 基于以上分析,本研究选择以刻蚀后的镍铬合金细丝为基底,刻蚀后的合金细丝表面呈现凹凸不平的孔洞结构,可增大附着材料的生长面积,且合金细丝相较单一金属强度更高,不易断裂,耐腐蚀性好[15]. 采用三电极体系,在金属细丝上沉积铜钴氧化物纳米颗粒,构建葡萄糖传感器. 通过铜钴金属氧化物纳米结构的协同作用,使传感器的电催化性能有明显提高,以期为新型葡萄糖传感器电极的研发提供参考.
全文HTML
-
仪器:电热恒温干燥箱(202-OOA)用于材料干燥,马弗炉用于高温退火,扫描电子显微镜(SEM,JSM 7100F)、透射电子显微镜(TEM,JEM-2010)、能量色散能谱仪(EDS,英国牛津仪器公司)和X射线光谱仪(XPS,ESCALAB 250,赛默飞世尔公司)用于样品形貌表征和成分分析. 恒电位沉积及电化学性能测试使用的均为三电极工作体系,制备的细丝电极为工作电极,铂丝为对电极,Ag/AgCl电极作为参比电极,电化学性能测试使用的是电化学工作站(CHI 660E,上海辰华仪器公司).
试剂:六水硝酸钴(Co(NO3)2·6H2O)、三水硝酸铜(Cu(NO3)2·3H2O)、氢氧化钠(NaOH)等药品购自重庆跃翔公司,葡萄糖(glucose)、抗坏血酸(AA)、多巴胺(DA)、尿酸(UA)、草酸(OA)、过氧化氢(H2O2)购自美国Sigma-Aldrich公司,葡萄糖饮品购自国内药店,实验中配置溶液所用的是实验室自制的去离子水.
-
本实验在镍铬合金细丝上电沉积合成铜钴氧化物复合纳米颗粒,经过系列对比实验后,得到优化后的实验流程如下. 首先将直径为0.2 mm的镍铬合金细丝进行预处理,将其用2 mol/L的盐酸浸泡12 h,以除去表面的氧化层. 因铬金属的活性比镍强,铬与盐酸反应更快,刻蚀后的金属细丝会出现疏松多孔的结构,以此增大纳米材料的生长面积,提升电极性能. 然后分别在无水乙醇和去离子水中超声清洗15 min,清洗完后放入干燥箱干燥1 h备用. 准确称量0.242 g(1 mmol)的三水硝酸铜和0.291 g(1 mmol)的六水硝酸钴置于烧杯中,加入50 mL去离子水,磁力搅拌后形成均匀澄清的溶液作为电解液. 采用三电极体系,以预处理的合金细丝作为工作电极,铂丝为对电极,Ag/AgCl电极为参比电极,用恒电位沉积法在合金细丝表面沉积Cu-Co纳米颗粒,沉积电压为-0.7 V,沉积时间为60 s,沉积温度为室温. 沉积完后将合金细丝取出冲洗并放入干燥箱中60 ℃干燥1 h,再将其放入马弗炉中300 ℃退火2 h后,得到铜钴氧化物修饰的合金细丝电极. 实验中分别制备了预处理后的镍铬合金细丝生长CuO纳米材料和生长CoO纳米材料的电极作为对照电极.
1.1. 实验仪器与试剂
1.2. 材料制备
-
对最佳实验条件下所制备合金细丝负载铜钴氧化物纳米材料进行了形貌表征,不同倍数的SEM图像如图 1所示. 从低倍的SEM图(图 1a)中可以看出,所用细丝直径约为200 μm,表面崎岖不平,存在较多的凹槽和刻痕. 从高倍的SEM图(图 1b,1c)中可以看出,在金属细丝表面生长有致密均匀的纳米颗粒,这些纳米颗粒的尺寸在30~70 nm之间,并且聚集在一起形成起伏的片状结构,同时颗粒之间又有细小的间隙,这样的纳米结构可增大电极材料的比表面积,呈现出更多的活性位点,使得纳米材料与反应物质能快速地反应并被检测,展现更好的电化学催化性能. 经过大功率超声处理后,对脱离下来的纳米颗粒进行了TEM观测,结果如图 2a,2b所示. 从图中可以更清楚地看出,这些颗粒的尺寸约为20~60 nm,相互连接和堆积,与扫描电镜观测结果一致. 图 2c~2e是纳米颗粒的高分辨图像,经过计算可知,晶面间距0.230 nm和0.137 nm分别对应于CuO的(111)晶面和(220)晶面,晶面间距0.196 nm则对应于Co3O4的(400)晶面,图 2f中的选区电子衍射图呈现出多个同心圆结构,相应晶面间距也分别与CuO和Co3O4的不同晶面相对应,结果表明在金属丝上成功制备了由CuO和Co3O4相复合的铜钴氧化物纳米颗粒.
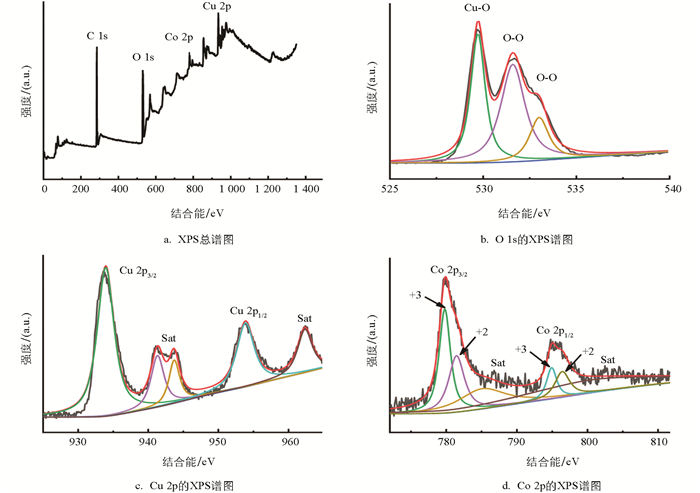
为了确认铜钴氧化物纳米颗粒的元素组成和价态,使用XPS对该材料进行测试分析,结果如图 3所示. 图 3a为总谱图,显示了Cu、Co、O元素的存在. 图 3b是O 1s的高分辨XPS谱图,结合能529.9 eV处的峰是由Cu-O的晶格氧所贡献,结合能531.5 eV和532.6 eV处的2个峰为吸附氧[16]. 图 3c是Cu 2p的高分辨XPS谱图,结合能在933.6 eV处的特征峰是Cu 2p3/2自旋轨道峰,它的2个卫星峰在941.1 eV和943.8 eV;结合能在953.7 eV处的特征峰是Cu 2p1/2自旋轨道峰,它的卫星峰在962.2 eV,这些卫星峰是由Cu2+所贡献,与文献[17-19]中一致. Co 2p的高分辨XPS谱图如图 3d所示,结合能在780.0 eV处的特征峰是Co 2p3/2自旋轨道峰,结合能在795.8 eV处的特征峰是Co 2p1/2自旋轨道峰,而且Co 2p1/2和Co 2p3/2特征峰之间的结合能相差15.8 eV,表面钴元素同时存在Co2+和Co3+2个价态[20]. 在786.1 eV和803.7 eV处是它的2个低卫星峰,在779.8 eV和794.8 eV处的峰由Co3+所贡献,在781.4 eV和796.0 eV处的峰由Co2+所贡献[21-22]. 综上所述,XPS测试结果再次说明在合金细丝上生长的纳米颗粒为铜钴氧化物复合材料.
-
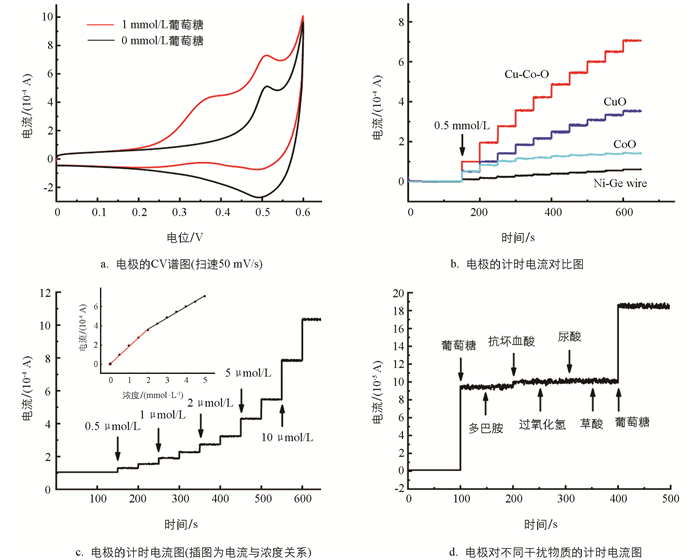
以0.2 mol/L NaOH溶液为空白底液,在0~0.6 V的电压范围内,扫描速度设定为50 mV/s,测试了加入1 mmol/L葡萄糖前后的CV曲线,结果如图 4a所示. 对比图中2条曲线可以看出,氧化峰电流在0.54 V左右明显增加,且加入葡萄糖后的CV曲线中氧化峰电流增加更明显,表明该电极材料与葡萄糖发生了氧化还原反应,且其具有良好的催化作用[23]. 为了研究细丝负载铜钴氧化物纳米颗粒修饰的无酶传感器的性能,采用计时电流法对该电极进行了测试. 在0.54 V的工作电位下,在持续均匀搅拌的0.2 mol/L NaOH溶液中每间隔50 s连续滴加0.5 mmol/L葡萄糖溶液,得到电流随时间的变化关系曲线,如图 4b所示. 未生长铜钴氧化物纳米材料的合金细丝在滴加葡萄糖溶液时,电流只发生了极其微弱的变化;相比之下,铜钴氧化物纳米颗粒修饰的电极在加入葡萄糖溶液后,电流迅速增加,且在3 s内达到稳定,电流响应呈现出较为平滑的阶梯式增强趋势,表明该电极材料在催化氧化葡萄糖的过程中,电子转移速度快,电流响应快且明显增加. 在相同的方法和条件下制备的单一材料氧化铜或氧化钴电极,对相同浓度的葡萄糖响应要低得多,这表明在铜钴氧化物纳米材料与葡萄糖发生氧化还原反应的过程中,Co和Cu的相互协同作用提高了该电极对葡萄糖的催化性能. 当添加0.5 μmol/L葡萄糖时,铜钴氧化物修饰的金属细丝电极表现出明显的电流响应,添加不同小浓度的葡萄糖溶液时,电流也得到相应增加,如图 4c所示. 将电流与葡萄糖浓度的关系进行拟合,得到电流与浓度的线性关系,如图 4c中插图所示. 葡萄糖浓度在0.001~2 mmol/L范围内,灵敏度为4 777 μA/(mmol·cm2);在2~5 mmol/L范围内,灵敏度为3 071 μA/(mmol·cm2). 其对应线性回归方程分别为I(μA)=0.032+1.808Cglucose(A)和I(μA)=1.328+1.157Cglucose (A),相关系数分别为0.998 58和0.997 70. 当信噪比为3时,可计算得出检测极限为0.1 μmol/L.
表 1列出了近期报道的由相近纳米材料制备的葡萄糖传感器的性能,相比之下,本研究制备的铜钴氧化物纳米颗粒修饰的葡萄糖传感电极具有更宽的线性范围、更高的灵敏度和更低的检测极限. 其原因可能得益于以下几个方面:第一,刻蚀后的合金细丝基底具有崎岖多孔结构,可增大基底表面积,有利于纳米颗粒嵌入式地生长,增加电极材料的生长面积;第二,相较于其他形状的纳米材料,铜钴氧化物纳米颗粒拥有更小的尺寸,提供更多孔隙和通道与反应物质接触,且纳米颗粒在基底上致密排布,并堆积呈立体的三维纳米片结构,材料的比表面积较大,能提供更多的活性位点,利于葡萄糖的催化反应,从而提高传感器的性能;第三,铜钴氧化物中2种材料的纳米颗粒相互交错,对葡萄糖的反应具有协同作用,因此电极材料有更高的灵敏度,氧化物相较于其他化合物也具有更高的稳定性,提高了其电化学性能.
为了探究铜钴氧化物纳米颗粒修饰的金属细丝电极的抗干扰性,在0.2 mol/L NaOH底液中加入其他干扰物质后对该电极进行了计时电流测试,包括多巴胺、抗坏血酸、过氧化氢、尿酸、草酸等多种干扰物质. 在人体血液中的葡萄糖浓度通常在3~8 mmol/L左右,是抗坏血酸、尿酸等干扰物质浓度的数十倍,远远高于干扰物质的浓度,因此选择加入的干扰物质浓度为0.05 mmol/L,均为葡萄糖浓度的1/10,其测试结果如图 4d所示. 从图 4d中可以看出,在0.2 mol/L NaOH溶液中加入0.5 mmol/L葡萄糖后电流明显增大,且快速达到稳定;当添加其他干扰物质时,电流几乎没有明显变化;当再次加入0.5 mmol/L的葡萄糖溶液后,电流再次明显地增大. 由此可见,制备的铜钴氧化物纳米颗粒修饰的细丝电极具有良好的抗干扰性. 稳定性测试结果表明,将电极放在干燥的空气中保存4周的时间,然后再次使用与之前相同的计时电流法测试电极对葡萄糖的电流响应. 在0.54 V的恒电压下,每隔50 s滴加0.5 mmol/L葡萄糖,经过灵敏度计算可得,放置4周后电极对葡萄糖的响应为初始值的95.2%,说明该电化学传感器具有优异的稳定性.
为了继续探究该葡萄糖传感器的实际应用,对葡萄糖饮品中的葡萄糖含量进行测定. 所用的葡萄糖饮品采购自国内药店,其标签显示每20 mL葡萄糖饮品中葡萄糖的含量为10 g,将其稀释为250 μmol/L. 采用标准取样法测试电极,标准溶液为实验室所配置的200 μmol/L葡萄糖溶液;采用加标法对制备电极进行测试,依次加入的标准葡萄糖含量分别为200 μmol/L,400 μmol/L,600 μmol/L,其结果如表 2所示. 电极的加标回收率为96.0%~98.6%之间,表明铜钴氧化物纳米颗粒修饰的合金细丝电极在实际葡萄糖的测试方面具有较好的应用价值.
2.1. 材料形貌与成分
2.2. 电化学性能
-
本文采用电沉积法和热处理技术相结合,在镍铬合金细丝上生长了均匀致密的铜钴氧化物纳米颗粒,该材料可作为无酶电化学传感电极用于探测葡萄糖的浓度. 利用SEM、TEM和XPS等方法对纳米颗粒的形貌和组分进行了表征和分析,并利用电化学分析仪测试了该无酶传感器对葡萄糖的催化性能. 结果表明,纳米颗粒的细小尺寸以及片状堆积结构提供了更大的比表面积,再加上2种金属氧化物间的协同作用,使得该电化学传感器具有更高的灵敏度、更低的检测极限、更宽的检测范围、更好的选择性和优异的稳定性等多种优点,且该电化学传感器制备简易,成本低,因此铜钴氧化物纳米颗粒修饰的合金细丝电极在葡萄糖传感器方面具有良好的应用前景.




 下载:
下载: