-
开放科学(资源服务)标识码(OSID):

-
黏土矿物是地球浅表沉积物中最丰富、分布最广的矿物,蒙脱石是典型的2∶1型层状硅酸盐黏土矿物,因其强大的吸附性,蒙脱石在各个领域都有着广泛的应用(例如污水处理[1]、医药[2]以及土壤污染修复[3-4]等)。蒙脱石的表面因同晶替代作用而带有大量的负电荷,为保持电荷平衡,蒙脱石层间往往会补偿一价或二价阳离子,层间阳离子的类型对蒙脱石的表面电场产生很大的影响。离子交换吸附是蒙脱石应用的基础,阳离子与蒙脱石的作用力类型和强弱深刻影响蒙脱石的性质和应用。一般认为金属离子主要通过静电作用吸附在蒙脱石表面[5-6]。然而,20世纪30年代,Jenny[7-8]就发现碱金属离子在带电黏土矿物上的吸附强度从强到弱依次为Li+、Na+、K+、Rb+、Cs+;Du等[9]通过低电解质浓度条件下(0.000 1~0.01 mol·L-1)紫色土表面吸附动力学试验重现了这一结果,并发现土壤表面电场导致离子产生了强烈的非经典极化效应,其产生额外势能(Hofmeister能)可能是离子在交换/吸附过程中离子特异性效应的重要原因[10]。国际著名土壤化学家Sposito[11]曾经指出土壤(矿物和有机物表面)电场的存在,对其中的离子/原子的电子云构象将产生很大改变,导致离子/原子极化,进而引发“极化诱导共价键”的形成。最新的研究发现,在强电场作用下,带电黏土矿物表面的离子/原子轨道通过非对称杂化可以引发离子极化诱导共价作用,并提出了非对称杂化轨道理论[12]。在此基础上,Li等[12]和Liu等[13]研究了Li+、Na+和Cs+在蒙脱石表面的吸附行为,发现静电相互作用能、非经典极化作用能、色散能和极化诱导共价相互作用能共同决定了离子在蒙脱石表面的吸附作用能。
蒙脱石表面的非对称电场会影响矿物表面O原子外层电子分布和能量,从而提高表面O原子孤对电子的活性;同时,该电场也会对吸附在表面的金属离子轨道产生不同程度的影响,从而改变离子与表面O原子的吸附作用力类型。当电解质浓度较低时,矿物表面电场强度较高,离子的极化率增大,与表面O原子之间的极化诱导共价作用成为可能;电解质浓度越高,屏蔽电场的能力越强,产生的新的作用力可能会逐渐减弱甚至消失。同时,蒙脱石颗粒表面离子吸附力越强,与表面O原子的作用力越强,对电场的屏蔽能力越强。蒙脱石表面O原子与表面的离子存在显著的电场依赖特性,因此,蒙脱石表面离子吸附力和能量的差异可能会导致不同电场强度下阳离子的不同动力学机制。
H+无核外电子,与其他阳离子相比,半径最小,因而能在土壤颗粒表面产生最强的静电吸附能;一价阳离子K+和二价阳离子Ca2+外层轨道均为3s3p;而Cs+外层轨道为5s5p,具有最大的离子半径,且极化率最高。化合价、离子半径以及离子的非对称杂化作用会导致离子交换过程中表面电场以及吸附能差异,而电场强度和表面O原子与不同离子的吸附力强弱的差异会引起吸附量以及蒙脱石表面的O—H键和Si—O键的振动频率的变化。本研究是从亚原子尺度揭示Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石颗粒表面的吸附力类型和强度,阐明极化效应对黏土矿物表面离子交换吸附的影响机制,并用SEM/EDS、FTIR等方法表征蒙脱石样品从而对试验结果进行验证,为进一步明确离子-带电表面相互作用机制提供可参考的理论依据。
全文HTML
-
本研究使用蒙脱石(购自物华天宝矿产资源有限公司,蒙脱石的表面电荷密度为0.153 1 C/m2)为试验材料,制备H+-、K+-、Ca2+-、Cs+-蒙脱石饱和样。以K+-蒙脱石饱和样为例,具体操作如下:取50 g蒙脱石颗粒置于三角瓶中,再加入1 L的0.1 mol· L-1 KCl溶液,摇匀使其分散后放入摇床振荡24 h(25 ℃),离心后去除上清液;重复上述步骤,反复3次,使蒙脱石颗粒表面被K+完全吸附饱和;然后用超纯水洗去土壤溶液中多余的游离K+离子;将离心后得到的样品放入70 ℃烘箱中,烘干后磨细过筛(0.25 mm),最后密封储存。H+-、Ca2+-、Cs+-蒙脱石饱和样以同样的方法制备。
-
采用静态恒流法进行Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石饱和样表面的吸附动力学试验,称取蒙脱石饱和样0.4 g左右,均匀地平铺在铺有滤纸的交换柱上。为了消除纵向浓度梯度引起的离子扩散的影响,样品应尽可能薄(约0.05 cm)。然后在298 K的恒温条件下,将浓度分别为0.000 1 mol/L、0.001 mol/L、和0.01 mol/L的MgCl2以1 mL/min的恒定流速通过交换柱上的待交换样品,用自动部分收集器按一定时间间隔收集从试验装置中流出的流动0液。利用原子吸收分光光度计测定原液和流出液中Mg2+的浓度。
-
土壤/黏土矿物颗粒表面带有大量电荷,这些电荷可在颗粒表面形成108~109 V/m的强电场,已有研究发展并建立了基于静电场的离子吸附动力学模型[14-16]。如果土壤/离子间存在强吸附力作用的快速吸附,则吸附过程存在零级动力学特征,其动力学方程为:
其中N(t)为阳离子吸附量(单位:mmol·kg-1);k(0)为离子的零级吸附速率常数,D0为离子在溶液中的扩散系数(单位:mmol·min-1);l为固定液膜的平均厚度(单位:m);S为样品的比表面积(单位:m2·kg-1);f0是本体溶液中的离子浓度(单位:mol·L-1);R和T分别为气体常数和绝对温度(单位:J·mol-1·K-1、K);F为法拉第常数(单位:C·mol-1);Z是阳离子的价态;φ(x)是在双电层中位置x处的电势(单位:mV)。
如果离子/表面间为弱吸附力相互作用,则离子吸附表现为慢速吸附,吸附过程存在一级动力学特征,其动力学方程为:
其中k(1)为离子的一级吸附速率常数;Neq为t接近∞(t→∞)时的阳离子吸附量或平衡吸附量。
根据界面反应理论可知,离子在界面反应总吸附能主要由静电作用、非经典极化作用、色散能等组成[10-11],即:
其中WT(0)是离子吸附于矿物颗粒表面的总能量;We(0)是离子吸附于矿物颗粒表面的静电能;Wp(0)是在离子吸附于矿物颗粒表面由阳离子非经典极化引起的作用能;Wd(0)源于阳离子和表面氧原子之间的色散能。
Mg2+在蒙脱石表面的交换吸附量可以近似为[17]:
其中a0为本体溶液中阳离子的活度,在x处的总吸附能WT(x)可表示为:
κ是Debye-Hückel常数,1/κ是德拜长度,
$1 / \kappa=\sqrt{\varepsilon_w R T /\left(8 \pi F^2 I\right)} $ ,εw是水的介电常数,εw=8.9×10-10,I是离子强度,其中:将方程(7)代入方程(6)可得:
当d=0时,表明离子已扩散至矿物表面,此时的平衡吸附量Neq按最大值CEC(蒙脱石CEC值为1 150 mmol·kg-1)计算。方程(9)改写为:
由方程(10)可求解出λ值,再代入(9)即可求解出d值。所以可以求出WT(d)为:
其中We=ZFφ0为平均静电能;γ是离子的表观电荷系数,Zhang经过胶体凝聚试验得到γMg2+/γNa+=1.47[19];而Li等估算了Na+在颗粒表面的γ值为1.18[20]。因此,通过计算得到γMg2+=1.47×1.18=1.73。
所以阳离子在矿物表面的静电吸附能可表示为:
当Mg2+在蒙脱石表面吸附时,Neq<CEC(CEC蒙脱石=1 150 mmol·kg-1)时,此时Wd(0)=0。所以Wp(0)可通过WT(0)-We(0)计算得到。
-
使用Spectrum Two傅里叶变换红外光谱分析仪测定H+-、K+-、Ca2+-、Cs+-蒙脱石在强电场和零电场下的红外光谱图。零电场的样品表面具有单层水分子,在378 K的烘箱中干燥48 h得到;强电场样品为含填充蒙脱石间隙的游离水的润湿样品。每次测量光谱波数在4 000~400 cm-1的范围内,分辨率为4 cm-1,信号累积量为32次。
-
采用JSM-6510LV10800的钨灯丝扫描电子显微镜能谱仪对饱和的蒙脱石样品和Mg2+交换后的蒙脱石进行定量微量分析,通过SEM-EDS面扫描分析得到相应的形貌图、能谱分析图及元素分布图。在样品的不同区域中进行至少3次测量以确定蒙脱石吸附前后不同元素的含量变化及分布情况。
1.1. 试验材料制备
1.2. 离子吸附动力学试验
1.3. 数据处理
1.4. 吸附前后样品表征
1.4.1. 红外光谱
1.4.2. 扫描电镜SEM/能量色谱EDS
-
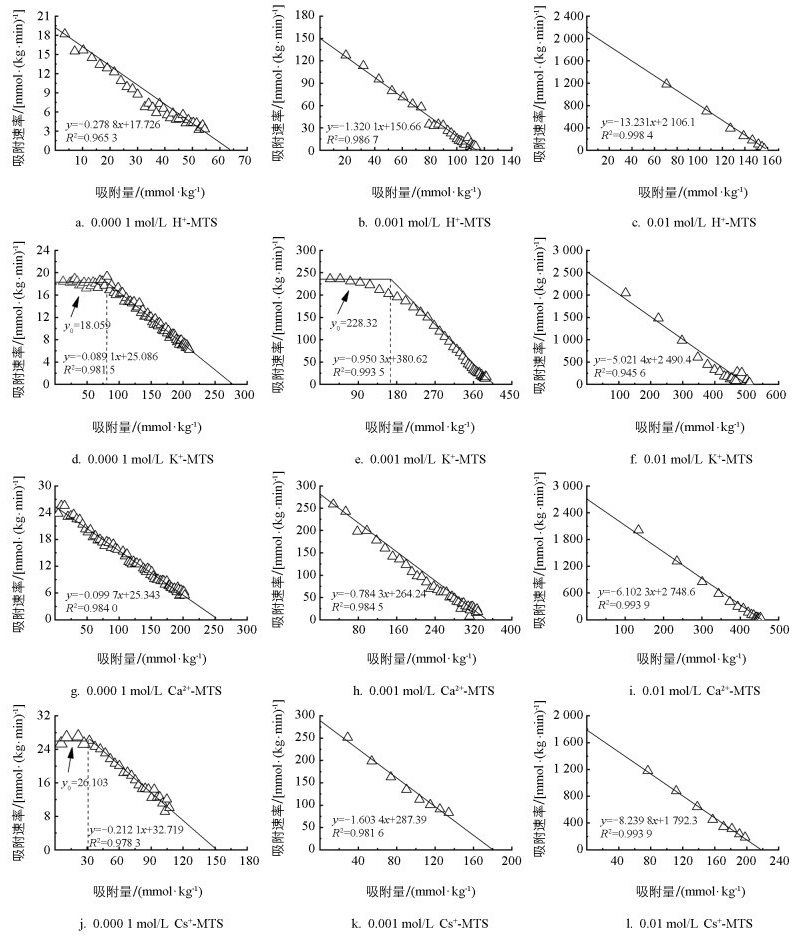
Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石表面吸附的dN(t)/dt≈[N(tm+1)-N(tm)]/(tm+1-tm)与N(t)≈N(tm+1/2)的动力学曲线与动力学参数如图 1、表 1所示。
由图 1可以看出,在电解质浓度较低时(浓度为0.000 1 mol/L和0.001 mol/L),Mg2+在K+-蒙脱石吸附的初始阶段均表现为零级动力学,之后转为一级动力学;Mg2+在Cs+-蒙脱石表面吸附时,仅在浓度为0.000 1 mol/L时的初始阶段出现零级强力吸附;而在所有电解质浓度下,Mg2+在H+、Ca2+-蒙脱石表面仅表现出一级动力学过程。Mg2+仅在交换K+和Cs+时出现了强吸附过程,这可能是因为K+和Cs+为一价阳离子,而一价阳离子屏蔽土壤表面电场的能力比高价阳离子弱,所以用一价离子制备的蒙脱石饱和样品才易于在土壤颗粒表面形成更强的负位能区,零级吸附过程易于表现出来[19]。
此外,随着电解质浓度的不断增大,Mg2+在不同离子饱和的蒙脱石表面的平衡吸附量、吸附速率常数也随之增大。离子吸附速率可以直接用相应的速率系数k值表征,例如当离子浓度分别为0.000 1 mol/L、0.001 mol/L和0.01 mol/L且Mg2+在H+-蒙脱石表面吸附时,吸附速率常数分别为17.7 mmol·kg-1·min-1、150.7 mmol·kg-1·min-1、2 106.1 mmol·kg-1·min-1。
图 1中一级速率方程中的截距与负斜率之比为Neq,所有电解质浓度下,Neq从大到小的顺序依次为K+、Ca2+、Cs+、H+-蒙脱石。值得注意的是,在所有交换试验过程中,Mg2+的浓度保持不变,理论上各种电解质浓度下的Mg2+均能将H+-、K+-、Ca2+-、Cs+-蒙脱石表面的饱和离子完全交换下来,并且其吸附量均等于蒙脱石的CEC值(1 150 mmol·kg-1),但Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石表面的Neq均小于1 150 mmol·kg-1,这表明在动力学试验中的吸附平衡并不是真正的平衡,而是一种亚稳平衡。亚稳平衡吸附量的差异与饱和离子在蒙脱石表面吸附能力大小有关,亚稳平衡吸附量越低,饱和离子与蒙脱石之间的吸附能力越强。因此不同离子在蒙脱石表面的吸附力从强到弱的顺序可能为H+、Cs+、Ca2+、K+。
π2D0/4l2可由式(3)、(4)来计算得到,其中D0是离子在土壤中的扩散系数,是由离子特性决定的,计算的浓度为0.000 1 mol/L时,Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石表面的π2D0/4l2值分别为-0.278 8、-0.089 1、-0.099 7、-0.212 1,而Mg2+在土壤中的扩散系数相同,因此π2D0/4l2绝对值越大,扩散距离l越短。Mg2+在4种不同表面的π2D0/4l2绝对值从大到小依次为H+-、Cs+-、Ca2+-、K+-蒙脱石,因此蒙脱石表面的扩散距离从大到小依次为K+-、Ca2+-、Cs+-、H+-蒙脱石,扩散距离越长,蒙脱石颗粒表面吸附位点越深,吸附时所要突破的能量势垒越大,这一趋势表明Mg2+在不同蒙脱石表面的吸附能可能表现出从小到大依次为H+-、Cs+-、Ca2+-、K+-蒙脱石的顺序。
以上试验结果均说明Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石表面吸附过程存在很大的差距,可能是因为H+、K+、Ca2+、Cs+与蒙脱石表面的结合情况影响了蒙脱石表面的表面电场,导致蒙脱石对离子的吸附能力改变,因而需要分析H+-、K+-、Ca2+-、Cs+-蒙脱石饱和样表面电化学性质对吸附过程的影响。
-
Mg2+浓度为0.001 mol/L时Neq较大,且此时电场对吸附过程的影响也较大。对浓度为0.001 mol/L的Mg2+在K+-、Ca2+-、Cs+-蒙脱石表面吸附前后的样品进行SEM/EDS扫描,部分结果如图 2所示。
由图 2可知,蒙脱石样品主要由Al、O、Si元素组成,被K+、Ca2+、Cs+饱和后,样品表面分别出现了K+、Ca2+、Cs+离子,并在蒙脱石颗粒表面分布均匀;Mg2+吸附后,Mg2+分布密度明显增大,并均匀地附着在蒙脱石颗粒表面,而K+、Ca2+、Cs+分布密度明显减小。这表明部分K+、Ca2+、Cs+已成功被Mg2+取代。
表 2显示了蒙脱石吸附前后主要元素含量,蒙脱石表面Al、O、Si含量从高到低依次为O、Si、Al,这表明蒙脱石主要由Al2O3、SiO2组成。由于同晶替代作用,Mg2+取代了蒙脱石铝氧八面体中的Al3+,使得测试结果中出现了少量Mg2+[21]。蒙脱石表面K+和Cs+含量相近,而Ca2+含量约为K+含量的1/2。这与理论值相符。
Mg2+在K+-、Ca2+-、Cs+-蒙脱石表面吸附后,Mg2+含量分别增加了1.31%、1.11%、0.88%,K+、Ca2+、Cs+的含量分别减少了2.51%、1.22%、1.66%。说明Mg2+分别以1∶2、1∶1以及1∶2的比例取代蒙脱石表面的K+、Ca2+、Cs+,并且在不同离子饱和蒙脱石表面的吸附量从多到少依次为K+-、Ca2+-、Cs+-蒙脱石。
-
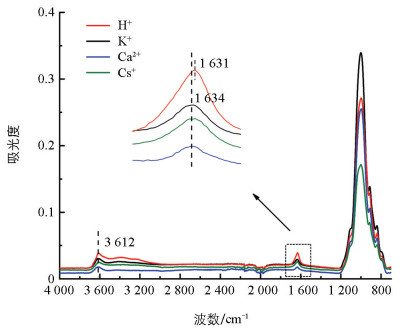
图 3为H+-、K+-、Ca2+-、Cs+-蒙脱石表面单层H2O的红外光谱图,谱带位于3 612 cm-1处为Al—OH和Si—OH的—OH谱带延伸[22],1 634 cm-1左右处的谱带与H—O—H弯曲振动有关。当4种阳离子吸附在蒙脱石表面时,水在蒙脱石表面的弯曲吸附带从H+、K+和Cs+的1 634 cm-1转变为Ca2+的1 631 cm-1。这一结果表明当不存在非对称电场时,表面阳离子主要以静电作用吸附在蒙脱石表面,此时Ca2+与蒙脱石的作用力最强[23]。
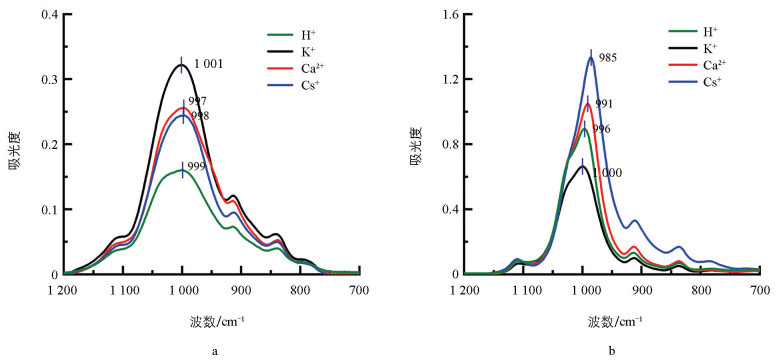
H+-、K+-、Ca2+-、Cs+-蒙脱石在零电场(a)和强电场(b)状态下Si—O的伸缩吸附带如图 4所示,Si—O—Si的振动峰值在1 000 cm -1左右,在零电场(a)中,蒙脱石的Si—O伸缩频率相差很小,这可能是因为在电场作用下产生新的作用力消失,此时只能通过静电作用吸附阳离子。而在强零电场(b)中,湿润的蒙脱石双电层内的强负电场会产生一个反向作用力,使得O原子上的电子云转移,导致Si—O键的力常数变大,因而使得吸收向高波数方向移动[24]。但H+-、K+-、Ca2+-、Cs+-蒙脱石在强电场下的Si—O伸缩频率低于电场为零时的Si—O伸缩频率,这可能是由于氢键的作用,使伸缩振动频率往低波数侧移动,吸收强度增大。在强电场中,蒙脱石的Si—O键伸缩频率从大到小依次为K+、H+、Ca2+、Cs+,这一顺序支持了阳离子与表面O原子的作用力从大到小依次为Cs+、Ca2+、H+、K+的结果[24]。H+、K+、Ca2+和Cs+ 4种离子在蒙脱石表面的主要吸附力类型为静电作用力,而H+是一种特殊的离子,它与表面氧原子之间不仅存在静电作用还存在共价作用。Liu等[13]也发现,一价的Cs+在蒙脱石表面的吸附力强于H+,但通过φ0的分析可知H+电场屏蔽能力大于Cs+,这可能是由于H+为点电荷,导致其可以到达Stern层,使得H+屏蔽电场的能力增强。这很好地解释了Mg2+在4种蒙脱石饱和样表面的Neq从多到少依次为K+-、Ca2+-、Cs+-、H+-蒙脱石的试验结果。
2.1. 蒙脱石表面的吸附动力学
2.2. 蒙脱石吸附前后SEM-EDS面扫描分析
2.3. 蒙脱石饱和样红外光谱分析
-
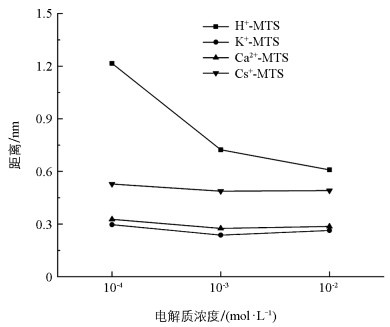
从试验结果可知Mg2+在蒙脱石表面的Neq均小于蒙脱石的CEC,因此达到吸附平衡时Mg2+并未完全到达蒙脱石颗粒表面,因此计算了达到吸附平衡时Mg2+到达蒙脱石表面的距离d值。
根据方程(6~10)求解出d值,结果如图 5所示。在相同电解质浓度下,达到平衡时Mg2+到H+-、K+-、Ca2+-、Cs+-蒙脱石表面的距离从长到短依次为dH+、dCs+、dCa2+、dK+,离子在矿物颗粒表面的吸附受土壤表面电场的影响,电场越强,Mg2+的极化率越强,与蒙脱石颗粒表面氧原子的结合能力越强,离子就越靠近矿物颗粒表面,那么d值也就越小,就越有利于阳离子将蒙脱石颗粒表面的离子交换下来,Neq也就会越大。Mg2+在H+-蒙脱石表面吸附时,d值随着浓度的增大而减小,这是因为随着电解质浓度的增大,双电层被压缩,体系的化学势增大,阳离子更容易扩散进入蒙脱石表面。在K+-、Ca2+-、Cs+-蒙脱石表面吸附时,d值表现为先减小后增大。电解质浓度从0.000 1 mol/L升高到0.001 mol/L时,Mg2+在K+-、Ca2+-、Cs+-蒙脱石表面的d值减小程度远小于在H+-蒙脱石表面的d值减小程度,比如Mg2+在H+-蒙脱石表面d值减小了0.492 nm,而在K+-、Ca2+-、Cs+-蒙脱石表面d值仅减小了0.059 9 nm、0.052 nm、0.040 7 nm。这可能是因为Mg2+在K+-、Ca2+-、Cs+-蒙脱石表面吸附时,随着电解质浓度的增大,体系的化学势增大,但表面电场随之减弱,导致Mg2+与蒙脱石表面氧原子的结合能力减弱,说明低电解质浓度条件下Mg2+在K+-、Ca2+-、Cs+-蒙脱石表面的吸附主要受表面电场的影响。而当浓度为0.01 mol/L时,Mg2+在K+-、Ca2+-、Cs+-蒙脱石表面吸附,双电层被压缩的程度更大,离子浓度的增加使单位距离里离子数量增多,导致其d值略增大。
由此可见Mg2+在蒙脱石表面的吸附受离子浓度、表面电场以及饱和离子类型共同影响。根据以上分析可以看出,离子与带电表面的结合情况深刻影响蒙脱石的电化学性质,从而影响表面电场,同时蒙脱石表面电场影响离子在蒙脱石颗粒表面扩散层中所能到达的位置,从而影响Mg2+在蒙脱石表面的吸附过程。这一结论与马倩等[25]发现紫色土因更高的表面电荷密度和电场强度对Mg2+吸附能力强于蒙脱石的研究结果相互佐证,共同深化了对矿物表面离子吸附机制的理解。
蒙脱石表面电化学性质深受颗粒表面饱和离子的影响,现根据离子吸附动力学的数据对H+-、K+-、Ca2+-、Cs+-蒙脱石表面的电化学参数进行计算[26]。
φd为距离矿物表面d位置处的电位值。当d=0时,即为矿物的表面电位φ0:
βi为蒙脱石饱和离子的表观电荷系数,βK[18]、βCa[27]、βCs[18]分别为1.942,1.96、2.354。
根据Stern理论,电势由表面到Stern层呈线性下降趋势,反离子到达带电表面的最近距离受到离子半径的限制,其中心电荷无法进入Stern层,而作为点电荷的H+则可以进入Stern层[28]。
此时:
其中σHs是Stern层中氢离子的吸附密度,r是Stern层的厚度,
$r=\sqrt{\varepsilon_w R T /\left(8 \pi F^2 I\right)} $ ,φs是Stern层的平均介电常数,φs≈ 6.67×10-11 C2·J-1·dm-1,aH0是氢离子的活度。其中σHd是扩散层中氢离子的吸附密度,2∶1电解质溶液中的M=
$\sqrt{3} $ [29],而φs/φ0=7.09[30],因此可求出φ0。σd为距离矿物表面d处的电荷密度(C·m-2)。
Ed为距离矿物表面d处的电场强度(V·m-1),ε为水的介电常数。
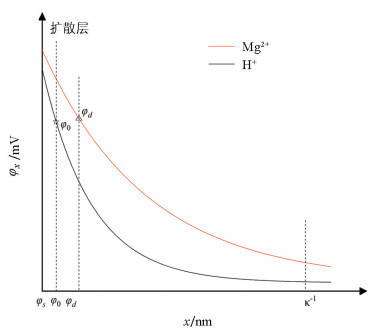
计算结果:①随着电解质浓度的增大,蒙脱石表面电位φ0逐渐减弱,Mg2+浓度越高,屏蔽电场的能力就越强;相同电解质浓度下,H+-、K+-、Ca2+-、Cs+-蒙脱石表面φ0的绝对值从大到小依次为K+-、Ca2+-、Cs+-、H+-蒙脱石,说明4种离子屏蔽电场的能力从大到小依次为H+、Cs+、Ca2+、K+,并且φ0的绝对值越大,吸附的反离子受到的非对称杂化效应就越强。② Mg2+在K+-、Ca2+-、Cs+-蒙脱石表面φd的绝对值均小于该体系下φ0的绝对值,并且φd的绝对值与φ0的绝对值之间的差距随着浓度的增大而增大;而在H+-蒙脱石表面吸附时φ0的绝对值小于φd的绝对值,如图 6所示,由于H+可以到达Stern层,所以H+屏蔽电场的能力远大于其他离子,而Mg2+交换后距离表面位置d处的φd主要由Mg2+决定。③吸附平衡时离子距离表面位置d处的电荷密度σd和电场强度Ed随着电解质浓度升高而增大,当电解质溶液浓度升高时,双电层厚度被压缩,阳离子达到吸附平衡时距离土壤/矿物表面的d值更小,这导致对应位置的电荷密度σd和电场强度Ed增大(表 3)。表 3中Ed数据表明4种蒙脱石表面电场均可达107~108 V·m-1,并且所有电解质浓度下表面电场从强到弱依次为K+-、Ca2+-、Cs+-、H+-蒙脱石,这一结果与2.1节中关于这4种离子在蒙脱石表面的吸附力顺序的推论结果相一致。本研究进一步说明了固/液界面交换体系的确处在强电场中,并且离子吸附过程受到矿物颗粒表面电场的强烈影响。
-
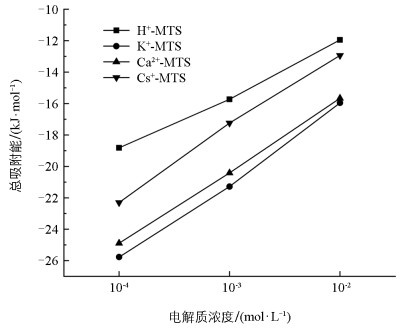
根据方程(7~11)可计算出Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石表面的总吸附能,再根据方程(12~13)分别计算出Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石表面的各类型的吸附能,相应结果列于表 4。
从表 4中可以看出,浓度为0.000 1 mol/L时,Mg2+在4种不同蒙脱石表面的WT从大到小依次为K+-、Ca2+-、Cs+-、H+-蒙脱石。随着电解质浓度增加,Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石表面的总吸附能WT、静电作用能We和非经典极化能Wc都呈现出减小的趋势。这是因为,随着电解质浓度的增加,离子对表面电场的屏蔽能力增强,蒙脱石表面电场强度减弱,所以Mg2+在蒙脱石表面的Wp减小,并且随着浓度的增加Mg2+取代矿物表面饱和离子的能量势垒减小,所以WT减小。非经典极化作用和静电作用共同决定了Mg2+在蒙脱石表面的吸附能,并且静电作用能对总吸附能的贡献更大。
对不同电解质浓度的Mg2+在H+-、K+-、Ca2+-、Cs+-蒙脱石表面的总吸附能作图,结果见图 7。① Mg2+在K+-、Ca2+-蒙脱石表面吸附能大小相近,并且在浓度为0.01 mol/L时差距最小,离子浓度越高,电场屏蔽能力越强,电场越弱,电场对Mg2+的影响越小;这一结果表明,相比于离子价态,电场是影响Mg2+在K+-、Ca2+-蒙脱石表面吸附的主要因素。② Mg2+在H+-、Cs+-蒙脱石表面吸附能大小相近,随着浓度的增大,吸附能的差距逐渐减小。如上文分析可知,这可能是由于H+为点电荷,导致其能够大量在蒙脱石表面聚集,使得H+屏蔽电场的能力增强,所以Cs+-蒙脱石表面的电场更强。在强电场的作用下,相比于H+,Cs+更易被代换下来。以上结果表明蒙脱石的吸附特性受制于表面吸附阳离子类型与带电黏土表面轨道非对称杂化效应的深度耦合作用,二者协同影响离子吸附过程。这一发现与皮水平等[31]针对高岭石体系的研究形成理论呼应,后者揭示碱金属离子的离子极化作用受扩散双电层位置与有效电荷数的双重调控,进而影响颗粒表面电位与吸附行为。尽管两项研究分别聚焦蒙脱石与高岭石、碱土金属离子与碱金属离子,但均从微观电子结构与离子化学特性层面,揭示了黏土矿物表面离子吸附本质上是多因素协同、跨尺度影响的复杂过程,为深入理解矿物-离子界面作用机制提供了全新视角。
-
离子交换吸附是土壤中重要的物理化学过程,蒙脱石作为典型黏土矿物,其表面的离子交换吸附行为对土壤特性影响显著。本研究通过吸附动力学试验和FTIR、EDS等表征方法进行验证,结果发现,蒙脱石表面饱和阳离子类型显著影响其电化学性质,进而改变离子吸附行为;Mg2+仅在K+-蒙脱石和Cs+-蒙脱石表面存在强吸附,且随着电解质浓度升高,Mg2+平衡吸附量增加,在4种蒙脱石表面的平衡吸附量从多到少依次为K+-、Ca2+-、Cs+-、H+-蒙脱石。FTIR结果显示,不同阳离子与蒙脱石表面O原子的作用力从小到大依次为Cs+、Ca2+、H+、K+,由于H+在表面聚集增强了屏蔽电场能力,致使Mg2+在K+-蒙脱石表面吸附最弱。综上,Mg2+在蒙脱石表面的吸附受离子浓度、表面电场强度及饱和离子类型的共同调控。



 下载:
下载: